卡培他濱聯合放療治療局部進展期直腸癌的療效觀察
帖曉靜,田永巍,高 嶺,李 寧,劉培杰,徐志巧
直腸癌是消化系統高發惡性腫瘤之一,發病率呈逐年上升趨勢。術前放化療逐漸成為局部進展期直腸癌的標準治療模式,可提高腫瘤局部控制率及手術切除成功率,有助于提升患者生活質量。卡培他濱是一種具有腫瘤選擇性的新型口服氟尿嘧啶甲氨酸鹽,對直腸癌有顯著臨床療效[1]。我院近年應用卡培他濱聯合放療治療局部進展期直腸癌取得較好療效,現報道如下。
1 資料與方法
1.1 一般資料 選擇我院2007年6月—2010年6月收治的局部進展期直腸癌患者共52例,均經結腸鏡、胸腹盆腔CT、組織病理學檢查確診,臨床分期為T3/T4期且無遠處轉移,美國東部腫瘤協作組(ECOG)評分≤2分。將患者按照治療方法分為對照組25例和觀察組27例,兩組患者的性別、年齡、臨床分期比較,差異均無統計學意義(P>0.05,見表1),具有可比性。治療前均經患者及家屬同意,簽署放化療知情同意書。
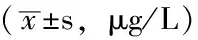
表2 兩組患者治療前后CEA水平比較Table 2 Comparison of CEA levels between the two groups before and after treatment
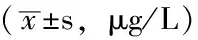
表3 不同臨床療效患者治療前后CEA水平比較Table 3 Comparison of CEA levels in patients with different efficacy before and after treatment
表1 兩組患者一般資料比較
Table1 Comparison of general information between the two groups
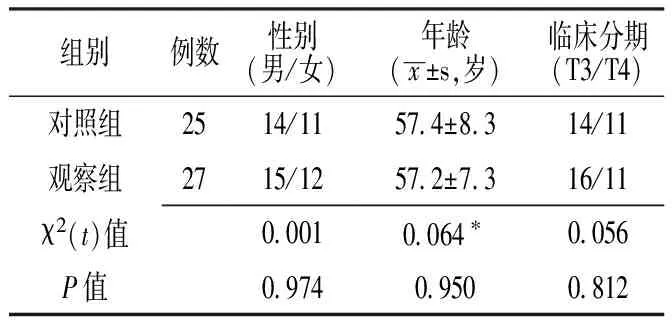
組別例數性別(男/女)年齡(x±s,歲)臨床分期(T3/T4)對照組2514/1157 4±8 314/11觀察組2715/1257 2±7 316/11χ2(t)值0 0010 064?0 056P值0 9740 9500 812
注:*為t值
1.2 治療方法 兩組患者均進行術前放療,每周治療5 d,2 Gy/d,劑量為46~50 Gy/ 4~5 w;觀察組患者在此基礎上口服卡培他濱1 250 mg/m2,2次/d,餐后0.5 h服用,第1~14天,21 d重復,共化療2個周期。兩組患者均在放化療結束后復查CT,無手術禁忌證者于6~8周內進行手術治療,術后進行系統化療。
1.3 觀察指標 (1)臨床療效:治療后1個月復查盆腔增強CT,按照RECIST標準評價臨床療效,無腫瘤殘留為完全緩解(CR);腫瘤浸潤深度變淺為部分緩解(PR);腫瘤浸潤深度無明顯變化為穩定(SD);腫瘤浸潤深度加深為進展(PD);計算總體有效率(ORR),ORR=CR率+PR率。(2)毒副作用:根據世界衛生組織(WHO)制定的關于抗癌藥物毒副作用評定標準評價觀察組患者的毒副作用。(3)治療前后癌胚抗原(CEA)水平(參考值0~5 μg/L)。(4)隨訪:對兩組患者進行隨訪,至少隨訪2年,計算無進展生存期(PFS)、1年及2年生存率。
2 結果
2.1 臨床療效 對照組CR 2例,PR 14例,SD 8例,PD 1例,ORR為16/25;觀察組CR 4例,PR 20例,SD 2例,PD 1例,ORR為24/27。兩組ORR比較,差異有統計學意義(χ2=4.530,P=0.049)。
2.2 毒副作用 觀察組出現骨髓抑制5例、腹瀉4例、惡心/嘔吐3例、皮膚黏膜損害2例、手足綜合征2例,患者可耐受,未進行特殊處理,未見4級毒副作用。
2.3 CEA水平 兩組治療前、治療后CEA水平比較,差異均無統計學意義(P>0.05);對照組治療前后、觀察組治療前后CEA水平比較,差異均有統計學意義(P<0.05,見表2)。
根據臨床療效將患者進一步分為CR+PR組與SD+PD組,兩組治療前CEA水平比較,差異有統計學意義(P<0.05);治療后比較,差異無統計學意義(P>0.05)。CR+PR組治療前后、SD+PD組治療前后比較,差異均有統計學意義(P<0.05,見表3)。
2.4 隨訪 對照組PFS為(20.4±1.1)個月,觀察組為(27.0±1.4)個月,差異有統計學意義(t=3.795,P<0.05);對照組1年生存率為25/25,觀察組為27/27,差異無統計學意義(χ2=0.000,P>0.05);對照組2年生存率為21/25,觀察組為25/27,差異有統計學意義(χ2=0.939,P>0.05)。
2.5 相關性分析 Pearson相關分析顯示,CEA水平與PFS呈負相關(r=-0.329,P=0.017)、與OS無線性相關性(r=-0.185,P=0.189)。
3 討論
直腸癌起病隱匿,缺乏特異癥狀,臨床發現時多數已屬中晚期;盡管全直腸系膜切除術使其局部復發率明顯下降,但仍有10%~15%的患者會出現局部復發[2-3]。一項比較術前單純放療與氟尿嘧啶聯合亞葉酸鈣方案(5-FU/LV方案)同期放化療輔助手術治療無遠處轉移的T3/4直腸癌的研究發現,兩組間總體生存率和保肛率無明顯差異,但術前同期放化療組獲得了較高的CR率(11.4%與3.6%,P<0.05)和較低的局部復發率(8.1%與16.5%,P<0.05)[4];且此結果在后續多項大型臨床研究中得到進一步證實,提示術前同期放化療與術前單純放療相比,可提高腫瘤局部控制率、降低局部復發率。術前新輔助同步放化療已成為歐美局部進展期直腸癌的標準治療方案。
卡培他濱是一種全新的靶向性口服化療藥物,能準確識別腫瘤細胞,經腫瘤組織中特有的高濃度的胸苷磷酸化酶轉化為活性氟尿嘧啶發揮抗癌作用。最近,兩項大型Ⅲ期臨床研究(NSABP R-04和德國合作組研究)證實,直腸癌新輔助放化療中聯合卡培他濱的療效不劣于靜脈注射氟尿嘧啶[5]。考慮到患者對持續靜脈注射氟尿嘧啶的依從性,不易接受,且增加了感染和血栓形成等風險,因此,本研究采用口服卡培他濱聯合放療治療局部進展期直腸癌,更為方便安全。
本研究結果顯示,觀察組ORR高于對照組,PFS長于對照組,主要毒副作用為腹瀉和骨髓抑制,患者可耐受,未見4級毒副作用,表明卡培他濱聯合放療治療局部進展期直腸癌療效優于單純放療,與文獻報道結果一致[6]。對所有患者進行為期2年的隨訪發現,觀察組與對照組1年生存率間無明顯差異,2年生存率間有明顯差異,提示卡培他濱聯合放療治療局部進展期直腸癌遠期療效較好。Sun等[7]進行的Ⅱ期臨床研究中應用西妥昔單抗聯合新輔助放化療治療直腸癌,結果表明其療效并不優于聯合兩種或更多的細胞毒藥物。本研究中有2例患者在放化療后出現遠處轉移,因而未行手術治療,繼續完成后續全身聯合化療;其余50例于同步放化療后6~8周行根治性腫瘤切除,術中見直腸周圍纖維化明顯,術后均未出現吻合口漏,提示卡培他濱聯合放療治療局部進展期直腸癌并不增加手術難度及手術并發癥發生率[8-9]。
CEA水平對消化道腫瘤的診斷及預后判斷有良好的臨床應用價值[10],術前高水平CEA患者較術前低水平CEA者預后差,PFS及OS短[11]。本研究結果顯示,觀察組與對照組治療后CEA水平均明顯下降,SD+PD組治療后CEA水平也較前下降,且CEA水平與PFS呈負相關,而與OS無相關性,提示CEA水平可能為預測卡培他濱聯合放療治療局部進展期直腸癌療效的一項指標,與文獻報道基本一致[11-12]。但本研究樣本量較小,且評價臨床療效的影像學改變有可能晚于血清學改變,有待進一步研究觀察;建議術前CEA水平異常增高或術后無明顯下降的局部進展期直腸癌患者進行系統性輔助化療,以減少腫瘤的復發率、轉移率。
1 吾甫爾·艾克木,王若崢,王多明.卡培他濱化療同步放射治療局部晚期直腸癌的療效觀察[J].中國全科醫學,2009,12(15):1426-1427.
2 梁天偉,孫軼,盧永剛,等.兩種拖出式超低位直腸癌保肛術療效分析[J].中國全科醫學,2011,14(5):1712.
3 謝雪梅.直腸癌切除術的臨床護理[J].實用心腦肺血管病雜志,2011,19(4):672.
4 Sebag-Montefiore D,Stephens RJ,Steele R,et al.Preoperative radiotherapy versus selective postoperative chemoradiotherapy in patients with rectal cancer(MRC CR07 and NCIC-CTG C016):a multicentre,randomised trial[J].Lancet,2009,373(9666):811-820.
5 Chen CF,Huang MY,Huang CJ,et al.A observational study of the efficacy and safety of capecitabine versus bolus infusional 5-fluorouracil in pre-operative chemoradiotherapy for locally advanced rectal cancer [J].Int J Colorectal Dis,2012,27(6):727-736.
6 Hofheinz RD,Wenz F,Post S,et al.Chemoradiotherapy with capecitabine versus fluorouracil for locally advanced rectal cancer:a randomised,multicentre,non-inferiority,phase 3 trial[J].Lancet Oncol,2012,13(6):579-588.
7 Sun PL,Li B,Ye QF.Effect of neoadjuvant cetuximab,capecitabine,and radiotherapy for locally advanced rectal cancer:results of a phase Ⅱ study[J].Int J Colorectal Dis,2012,27(10):1325-1332.
8 蔡鋼,章真.直腸癌的輔助放化療的臨床研究[J].中國癌癥雜志,2006,16(5):399-402.
9 Rullier E,Goffre B,Bonnel C,et al.Preoperative radiochemotherapy and sphincter-saving resection for T3 carcinomas of the lower third of the rectum[J].Ann Surg,2001,234(5):633-640.
10 李雨升,楊立廷,余云云,等.120例結直腸癌手術前后血清CEA RIA 測定的臨床觀察[J].標記免疫分析與臨床,2003,10(1):9-11.
11 Tarantino I,Warschkow R,Worni M.Elevated preoperative CEA is associated with worse survival in stageⅠ-Ⅲ rectal cancer patients[J].Br J Cancer,2012,107(2):266-274.
12 Kim CW,Yu CS,Yang SS,et al.Clinical significance of pre- to post-chemoradiotherapy s-CEA reduction ratio in rectal cancer patients treated with preoperative chemoradiotherapy and curative resection[J].Ann Surg Oncol,2011,18(12):3271-3277.

