阿侖膦酸鈉與阿法骨化醇對骨質疏松老年女性患者動脈硬化參數的影響*
李霞緋,吳 娟
(重慶市第三人民醫院老年病科 400014)
雙磷酸鹽和活性維生素D3是臨床常用的治療骨質疏松藥物。研究表明利塞膦酸鈉治療骨質疏松后降低了心血管疾病,特別是中風的病死率[1],而活性維生素D3能減少腎臟疾病終末期患者心血管死亡風險[2]。因此認為雙磷酸鹽及活性維生素D3具有抗動脈粥樣硬化的作用。在老年人中常同時發生動脈粥樣硬化、血管鈣化與骨質疏松,并且骨質疏松及動脈粥樣硬化也是2型糖尿病患者的常見并發癥,其共同的病理生理機制及相關性成為目前研究的熱點。而女性患者由于其自身生理特點,骨質疏松的發生率遠高于男性,一般女性絕經后年數越久,發生骨質疏松的風險性越大[3]。因此,本研究擬采用踝臂指數(arkle brachial index,ABI)、心踝血管指數(cardio ankle vascular index,CAVI)、頸動脈內膜中層厚度(intima media thickness,IMT)作為動脈硬化參數,觀察骨質疏松治療中阿倫膦酸鈉及阿法骨化醇對2型糖尿病合并骨質疏松的老年女性患者動脈粥樣硬化的影響。
1 資料與方法
1.1 一般資料 研究對象為本院老年科2011年4月至2011年10月門診及住院患者。所有患者均符合1999年世界衛生組織的2型糖尿病診斷標準[4]。骨質疏松的診斷標準為[5]:脊柱或股骨頸骨密度T值小于-2.5,或者T值小于-1.5并有脆性骨折史。所有受試者均排除影響骨代謝的其他疾病,之前未服用過已知的影響骨鈣代謝的藥物(長期服用糖皮質激素、甲狀腺激素、雌激素等)及偏癱、長期臥床、局部制動。所有受試者均無肝、腎功能異常。骨質疏松組為28例2型糖尿病并骨質疏松老年女性患者,年齡66~85歲,平均(75.46±5.37)歲,平均體質量(55.29±7.32)kg;對照組為25例年齡及體質量相匹配的糖尿病非骨質疏松老年女性,年齡66~81歲,平均(73.52±4.50)歲,平均體質量(58.54±7.4)kg。骨質疏松組給予阿倫膦酸鈉每周70mg及阿法骨化醇每天0.5μg治療,持續12個月。兩組均給予膳食補鈣,未服用鈣劑。所有試驗對象在納入12個月后進行骨密度、動脈硬化指數、身高、體質量、血壓以及生化指標測定。
1.2 方法
1.2.1 骨密度(BMD)測定 采用美國Norland公司生產的Prodigy型雙能X線骨密度儀,由同一專業技術人員測定檢試者股骨頸及ward三角區BMD及計算T值。
1.2.2 動脈硬化檢測 CAVI、ABI采用北京福田電子醫療儀器有限公司的VS-1000動脈硬化檢測儀測定。IMT經Philips il/22彩色多普勒檢測儀測定。同時測定左、右兩側的側的CAVI、ABI和IMT。
1.2.3 一般指標及生化指標的檢測 受試者均由同一人測量血壓、身高、體質量。空腹10h,測定血漿生化指標:三酰甘油(TG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、糖化血紅蛋白(HbA1c)。
1.3 統計學處理 采用SPSS17.0統計軟件進行分析,計量資料采用±s表示,兩組間均數比較采用獨立樣本t檢驗,組間治療前后指標均數采用配對樣本t檢驗,兩組間非計量資料比較采用χ2檢驗,以P<0.05為差異有統計學意義。
2 結 果
2.1 兩組間基線特征比較 骨質疏松組和對照組比較,其股骨頸和ward三角區的BMD、T值明顯下降,骨質疏松組ABI較對照組低,而CAVI、IMT明顯升高,差異均有統計學意義(P<0.05),其他參數差異無統計學意義(P>0.05),見表1。
2.2 治療前后骨密度及動脈硬化指標的變化 骨質疏松組治療12個月后其股骨頸及ward三角區BMD、T值明顯升高,動脈硬化參數ABI、CAVI及IMT無明顯變化。同時,骨質疏松組治療12個月后其LDL降低,HDL升高。而對照組的動脈硬化程度在12個月后均較之前加重,見表2。
表1 實驗組和對照組基線特征比較(±s)
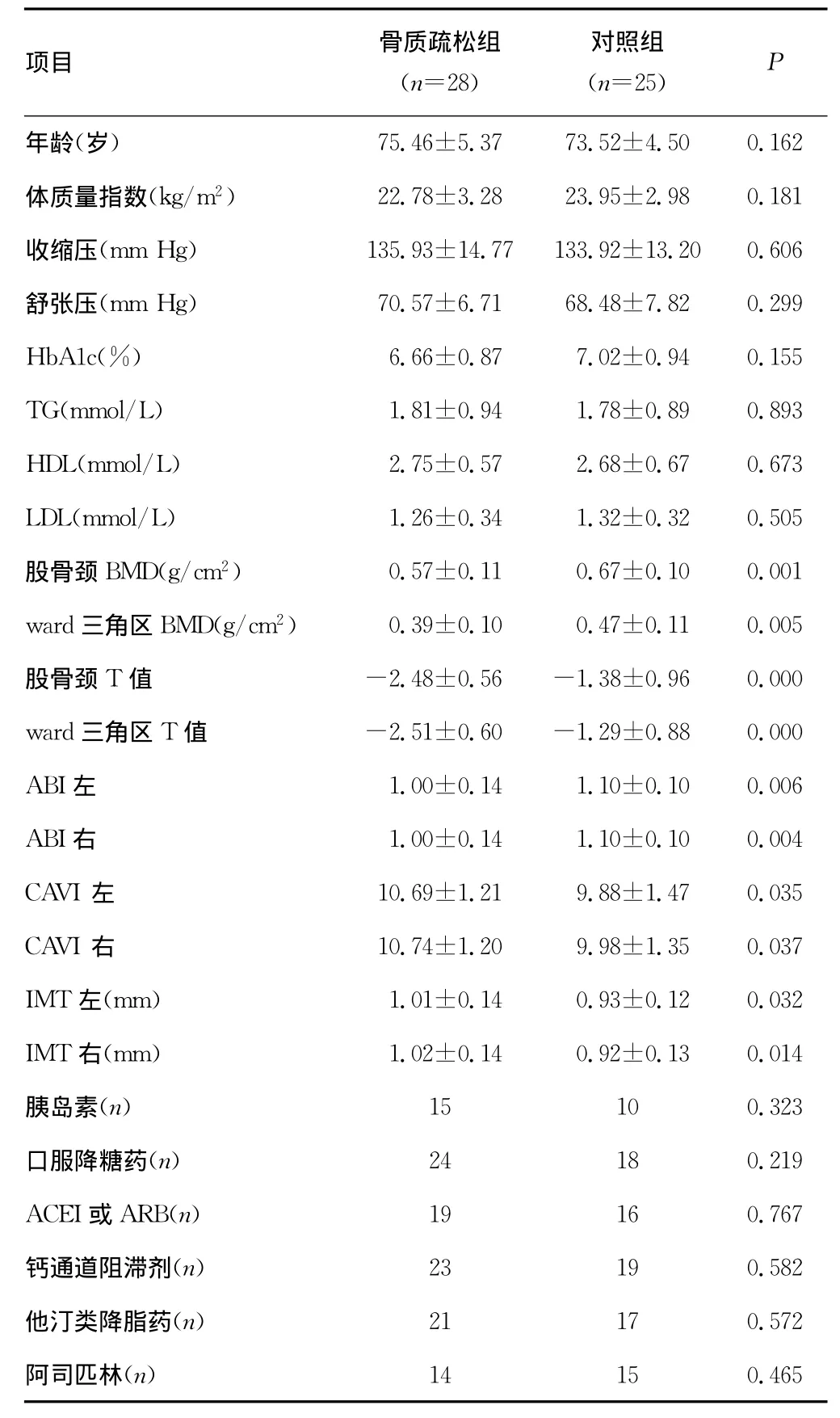
表1 實驗組和對照組基線特征比較(±s)
項目 骨質疏松組(n=28)對照組(n=25)P 75.46±5.37 73.52±4.50 0.162體質量指數(kg/m2) 22.78±3.28 23.95±2.98 0.181收縮壓(mm Hg) 135.93±14.77 133.92±13.20 0.606舒張壓(mm Hg) 70.57±6.71 68.48±7.82 0.299 HbA1c(%) 6.66±0.87 7.02±0.94 0.155 TG(mmol/L) 1.81±0.94 1.78±0.89 0.893 HDL(mmol/L) 2.75±0.57 2.68±0.67 0.673 LDL(mmol/L) 1.26±0.34 1.32±0.32 0.505股骨頸BMD(g/cm2) 0.57±0.11 0.67±0.10 0.001 ward三角區BMD(g/cm2) 0.39±0.10 0.47±0.11 0.005股骨頸T值 -2.48±0.56 -1.38±0.96 0.000 ward三角區T值 -2.51±0.60 -1.29±0.88 0.000 ABI左 1.00±0.14 1.10±0.10 0.006 ABI右 1.00±0.14 1.10±0.10 0.004 CAVI左 10.69±1.21 9.88±1.47 0.035 CAVI右 10.74±1.20 9.98±1.35 0.037 IMT左(mm) 1.01±0.14 0.93±0.12 0.032 IMT右(mm) 1.02±0.14 0.92±0.13 0.014胰島素(n) 15 10 0.323口服降糖藥(n) 24 18 0.219 ACEI或ARB(n) 19 16 0.767鈣通道阻滯劑(n) 23 19 0.582他汀類降脂藥(n) 21 17 0.572阿司匹林(n)年齡(歲)14 15 0.465
表2 骨質疏松組治療前后骨密度及動脈硬化指標的變化(±s)
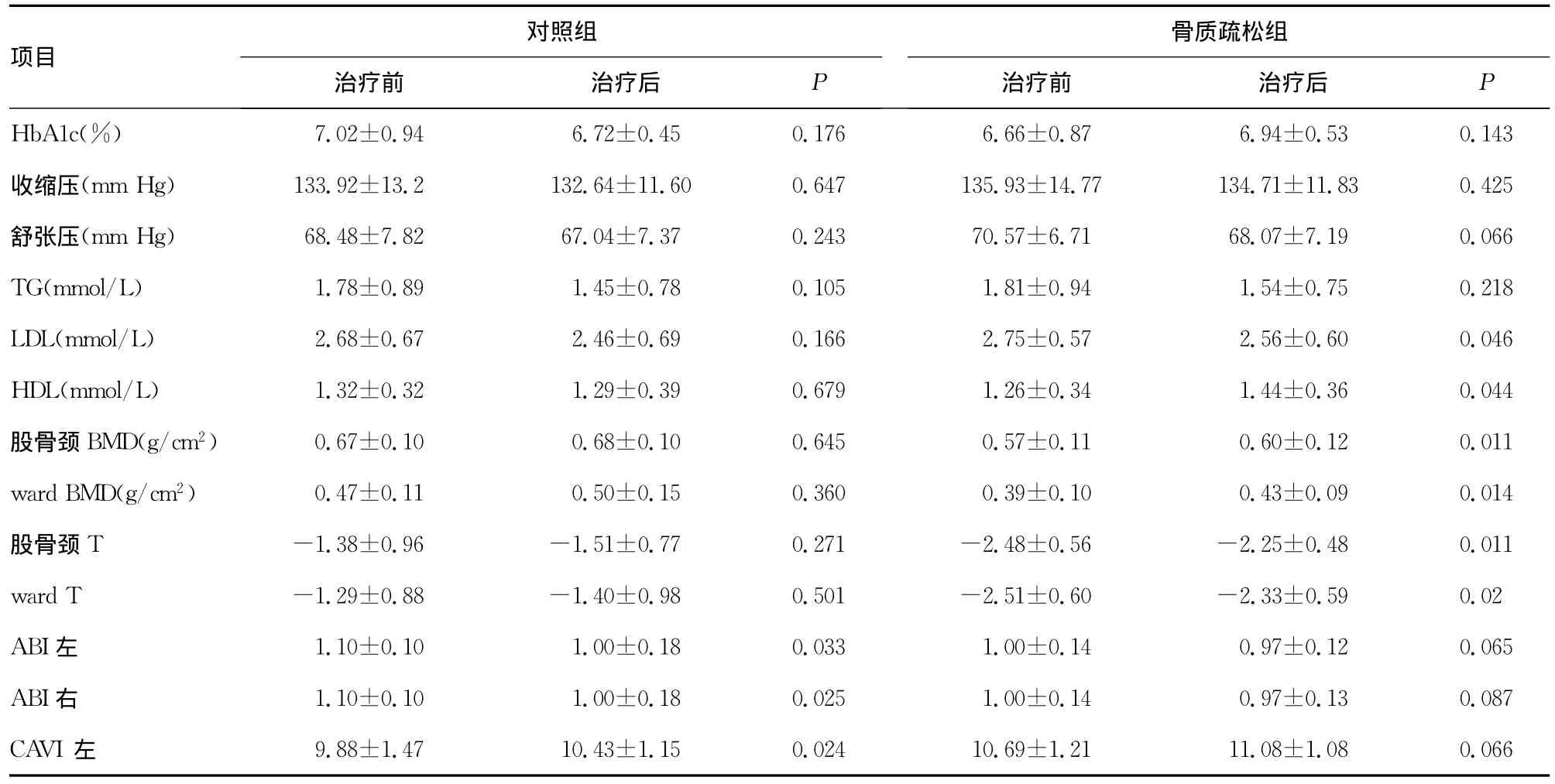
表2 骨質疏松組治療前后骨密度及動脈硬化指標的變化(±s)
項目對照組治療前 治療后P骨質疏松組治療前 治療后P 53 0.143收縮壓(mm Hg) 133.92±13.2 132.64±11.60 0.647 135.93±14.77 134.71±11.83 0.425舒張壓(mm Hg) 68.48±7.82 67.04±7.37 0.243 70.57±6.71 68.07±7.19 0.066 TG(mmol/L) 1.78±0.89 1.45±0.78 0.105 1.81±0.94 1.54±0.75 0.218 LDL(mmol/L) 2.68±0.67 2.46±0.69 0.166 2.75±0.57 2.56±0.60 0.046 HDL(mmol/L) 1.32±0.32 1.29±0.39 0.679 1.26±0.34 1.44±0.36 0.044股骨頸BMD(g/cm2) 0.67±0.10 0.68±0.10 0.645 0.57±0.11 0.60±0.12 0.011 ward BMD(g/cm2) 0.47±0.11 0.50±0.15 0.360 0.39±0.10 0.43±0.09 0.014股骨頸 T -1.38±0.96 -1.51±0.77 0.271 -2.48±0.56 -2.25±0.48 0.011 ward T -1.29±0.88 -1.40±0.98 0.501 -2.51±0.60 -2.33±0.59 0.02 ABI左 1.10±0.10 1.00±0.18 0.033 1.00±0.14 0.97±0.12 0.065 ABI右 1.10±0.10 1.00±0.18 0.025 1.00±0.14 0.97±0.13 0.087 CAVI左 9.88±1.47 10.43±1.15 0.024 10.69±1.21 11.08 HbA1c(%) 7.02±0.94 6.72±0.45 0.176 6.66±0.87 6.94±0.±1.08 0.066
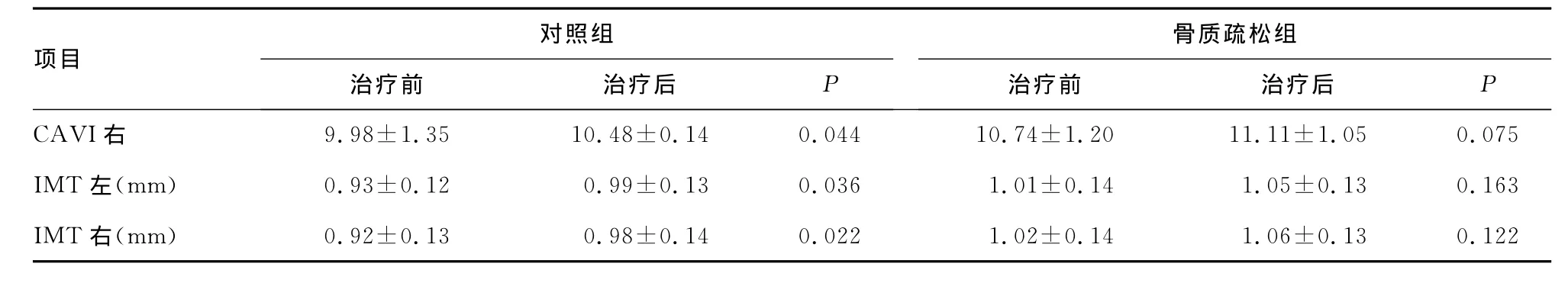
續表2 骨質疏松組治療前后骨密度及動脈硬化指標的變化
3 討 論
2型糖尿病患者心血管疾病發生率大約是年齡匹配的非糖尿病患者的2~4倍[6],而且老年2型糖尿病患者更易患骨質疏松[7]。許多研究已證實了動脈粥樣硬化與骨質疏松的關系,認為絕經后女性動脈鈣化與降低的BMD相關[8]。而動脈僵硬度是心血管疾病發病率及病死率的重要危險因子[9]。IMT是反映全身動脈硬化的早期指標,Bartman等[10]證實超聲測定的IMT可用來評估糖尿病患者心血管疾病風險。ABI是公認的反映外周血管閉塞程度的指標,Pasqualini等[11]的研究認為升高的ABI是內科住院患者心血管死亡及全因死亡的獨立預測因子。CAVI是近年來推出的一項新的能夠反映動脈血管僵硬度改變的檢測技術,具有重復性好以及血壓非依賴性的特點,有文獻報道CAVI、IMT和ABI這3個血管指數在糖尿病患者中具有很好的相關性[12]。因此這3個指標可作為臨床上預測心血管疾病的有效指標。本研究發現,骨質疏松組動脈硬化參數CAVI及IMT明顯高于對照組,而ABI明顯低于對照組,提示骨質疏松患者動脈硬化程度較非骨質疏松患者嚴重,從而也反映了骨質疏松與動脈硬化的相關性。經過阿法骨化醇聯合阿侖膦酸鈉治療后,骨質疏松組的動脈硬化程度無明顯進展,而對照組的動脈硬化程度進一步惡化。同樣說明2型糖尿病患者骨質疏松與動脈硬化或心血管疾病相關。體外實驗及基因表達研究結果表明,人類的血管鈣化過程與骨的構建、重建過程相似,是一個可調節的過程,動脈鈣化的機制類似于成骨過程,涉及許多能引起組織礦化的細胞、蛋白質及細胞因子,而通過抑制破骨細胞骨的重吸收來減少骨量丟失的制劑(如雙磷酸鹽、骨保護素)能夠抑制動脈鈣化[13]。
大量研究證實了雙磷酸鹽與動脈粥樣硬化的關系,阿侖膦酸鈉能顯著降低絕經后骨質疏松女性患者頸動脈內膜中層厚度[14]。而也有一些研究得出了相反的結果,認為阿侖膦酸鹽及伊班膦酸鹽不能改善絕經后骨質疏松女性頸動脈IMT和主動脈鈣化[15]。本研究則發現,經過阿法骨化醇聯合阿侖膦酸鈉治療1年后,骨質疏松組的動脈硬化程度無明顯進展,而對照組的動脈硬化程度進一步惡化,說明阿侖膦酸鈉聯合阿法骨化醇治療能抑制2型糖尿病并骨質疏松老年女性患者動脈硬化的進展。已有許多研究揭示了二磷酸鹽抗動脈粥樣硬化的機制。D′Amelio等[16]發現,利塞膦酸鹽能降低絕經后女性循環破骨細胞前體及炎癥細胞因子——腫瘤壞死因子-α(tumor necrosis factor,TNF-α)的水平,從而阻止絕經后骨質疏松的發生、發展。Albadawi等[17]研究發現,唑來膦酸鹽能有效抑制人血管平滑肌細胞的增殖、黏附和遷移,從而抑制血管內膜的過度增生。同時本實驗結果發現,實驗組阿侖膦酸鈉聯合阿法骨化醇治療12個月后其HDL有所上升,而LDL較之前有所下降,也提示其可能通過調節紊亂的血脂來發揮其抗動脈粥樣硬化的作用。
活性維生素D3與動脈硬化的關系也受到越來越多的關注,Ogawa等[18]研究證實血漿1α,25二羥基維生素D3水平與動脈鈣化程度呈負相關。大量研究發現1α,25二羥基維生素D3能夠下調核轉錄因子-κB基因的表達,從而激活抗炎細胞因子白細胞介素(IL)-10,同時抑制前炎細胞因子IL-6、IL-12、TNF-α的產生,而炎癥反應正是動脈粥樣硬化發生、發展的重要原因[19]。Artaza等[20]的研究證實維生素D3能抑制血管平滑肌細胞的增殖。以上研究均提示維生素D3的代謝參與了動脈粥樣硬化的發生、發展。本研究中實驗組治療前后動脈硬化參數的改變也提示維生素D3可能參與了抗動脈粥樣硬化的過程。
綜上所述,阿侖膦酸鈉聯合阿法骨化醇治療2型糖尿病合并骨質疏松老年女性患者能改善其動脈硬化參數,對其心腦血管疾病的防治有一定作用。當然,還需要更大樣本量及更深入的研究來證實阿侖膦酸鹽及阿法骨化醇等抗骨質疏松藥物對動脈硬化的影響及其機制。
[1]Ippei K,Toru Y,Kumi H,et al.Effects of treatment with risedronate and alfacalcidol on progression of atherosclerosis in postmenopausal wamen with type 2diabetes mellitus accompanied with osteoporosis[J].Am J Med Sci,2010,339(6):519-524.
[2]Ogawa M,Ogawa T,Inoue T,et al.Effect of alfacalcidol therapy on the survival of chronic hemodialysis patients[J].Ther Apher Dial,2012,16(3):248-253.
[3]李慧林,朱漢民,程搖群,等.絕經婦女絕經后年限及年齡與骨量丟失率關系[J].中國骨質疏松雜志,2007,13(7):502-504.
[4]廖二元,莫朝暉.內分泌學[M].2版.北京:人民衛生出版社 ,2002:1375.
[5]中華醫學會骨質疏松和骨礦鹽疾病分會.原發性骨質疏松癥診治指南[J].中華骨質疏松和骨礦鹽疾病雜志,2011,4(1):2-17.
[6]郝雅斌,洪旭,尹潔,等.絕經后2型糖尿病患者下肢動脈硬化與骨密度的相關性探討[J].中國骨質疏松雜志,2012,18(1):40-43.
[7]Xia J,Zhong Y,Huang G,Chen Y,et al.The relationship between insulin resistance and osteoporosis in elderly male type 2diabetes mellitus and diabetic nephropathy[J].Ann Endocrinol,2012,73(6):546-551.
[8]Frost ML,Grella R,Millasseau SC,et al.Relationship of calcification of atherosclerotic plaque and arterial stiffness to bone mineral density and osteoprotegerin in postmenopausal women referred for osteoporosis screening[J].Calcif Tissue Int,2008,83(2):112-120.
[9]Kenichiro K,Astuhiro I,Kanako B,et al.Differential effects in cardiovascular markers between high-dose an-giotensinⅡreceptor blocker monotherapy and combination therapy of ARB with calcium channel blocker in hypertension[J].Int J Hypertens,2011,201(3):284-290.
[10]Bartman W,Pierzchaa K.Clinical determinants of carotid intima-media thickness in patients with diabetes mellitus type 2[J].Neurol Neurochir Pol,2012,46(6):519-528.
[11]Pasqualini L,Schillaci G,Pirro M,et al.Prognostic value of low and high ankle-brachial index in hospitalized medical patients[J].Eur J Intern Med,2012,23(2):240-244.
[12]王紅漫,陳登容.心踝血管指數在老年人大動脈硬化診斷中的意義[J].中國循證心血管醫學雜志,2009,4(1):228-230.
[13]Wojciech K,Beata N,Marek S,et al.The mechanism of vascular calcification:a systematic review[J].Med Sci Monit,2012,18(1):1-11.
[14]Celiloglu M,Aydin Y,Balci P,et al.The effect of alendronate sodium on carotid artery intima-media thickness and lipid profile in women with postmenopausal losteoporosis[J].Menopause,2009,16(4):689-693.
[15]Delibasi T,Emral R,Erdogan MF,et al.Effects of alendronate sodium therapy on carotid intima media thickness in postmenopausal women with osteoporosis[J].Adv Ther 2007,24(3):319-325.
[16]D′Amelio P,Grimaldi A,Di Bella S,et al.Risedronate reduces osteoclast precursors and cytokine production in postmenopausal osteoporotic women[J].J Bone Miner Res,2008,23(3):373-379.
[17]Albadawi H,Haurani MJ,Oklu R,et al.Differential effect of zoledronic acid on human vascular smooth muscle cells[J].J Surq Res,2012,144(5):667-676.
[18]Ogawa T,Ishida H,Akamatsu M,et al.Relation of oral lalpha-hydroxy vtamin D3to the progression of aortic arch calcification in hemodialysis patients[J].Heart Vessels,2010,25(1):1-6.
[19]Artaza JN,Contreras S,Garcia LA,et al.Vitamin D and cardiovascular disease:potential role in health disparities[J].J Health Care Poor Underserved,2011,22(4):23-38.
[20]Artaza JN,Sirad F,Ferrini MG,et al.1,25-(OH)2Vitamin D3inhibits cell proliferation by promoting cell cycle arrest without inducing apoptosis and modifies cell morphology of mesenchymal multipotent cells[J].J Steroid Biochem Mol Biol,2010,119(1/2):73-83.

