復合氨基酸螯合鈣的合成工藝優化
馬海霞 楊賢慶 胡振珠
張 楨1 陳勝軍1 楊 燕1
(1.中國水產科學研究院南海水產研究所,廣東 廣州 510300;2.國家水產品加工技術研發中心,廣東 廣州 510300)
復合氨基酸螯合鈣的合成工藝優化
馬海霞1,2楊賢慶1,2胡振珠1
張 楨1陳勝軍1楊 燕1
(1.中國水產科學研究院南海水產研究所,廣東 廣州 510300;2.國家水產品加工技術研發中心,廣東 廣州 510300)
以魚類加工下腳料魚頭、魚排為原料制備復合氨基酸螯合鈣,采用Plackett-Burman設計、最陡爬坡試驗和中心組合設計法對螯合工藝條件進行優化。結果表明,pH值和氨基態氮對螯合率有顯著影響(P<0.05),復合氨基酸液中氨基酸的種類及其含量對螯合效果影響較大,當氨基酸濃度大于2.1mg/mL時,螯合鈣中相應的氨基酸相對含量也較高;在復合氨基酸液與鈣液螯合時,甲硫氨酸和甘氨酸對鈣的螯合能力均大于丙氨酸。優化后的螯合工藝參數:pH值7.90,溫度50℃,時間60min,氨基態氮濃度為3.66g/L,復合氨基酸液∶鈣液(V∶V)20∶1,該條件下螯合率為58.19%。
Plackett-Burman設計;復合氨基酸螯合鈣;甲硫氨酸;甘氨酸;螯合
氨基酸螯合鈣是一類金屬螯合物,與磷酸鈣、碳酸鈣、葡萄糖酸鈣、醋酸鈣、乳酸鈣等相比,易于被人體吸收、副作用小、生物利用率高,而且在補鈣的同時又可補充人體必需的氨基酸,是一種較理想的補鈣產品[1-3]。羅非魚、斑點叉尾鮰等魚類加工下腳料占到魚體重量的50%以上,如中國凍羅非魚片2009年產量超過22萬t,僅產生的魚頭、魚排下腳料就超過14萬t,約占魚體重量的36%~40%[4];這些下腳料多作為飼料原料被廉價銷售,附加值很低。魚骨中除含有蛋白質、脂肪等營養元素以外,還含有大量的鈣、鐵、鋅、鎂、磷及膠原成分,是開發骨源補鈣產品的良好資源。
國內關于氨基酸螯合鈣合成工藝的文獻報道很多,主要表現在兩方面:① 由單一氨基酸與某一鈣鹽反應的制備工藝[5-7];② 復合氨基酸螯合鈣的制備工藝[1,8-12],其復合氨基酸和鈣源分別是雞羽毛水解物和文蛤殼、米渣蛋白水解物和Ca(OH)2、豆粕水解物和動物骨骼或骨渣(生產骨膠的廢棄物)、低值魚蛋白酶解物和CaCl2等。而以魚類加工廢棄物魚頭、魚排酶解物為復合氨基酸來源、魚骨為鈣源開發復合氨基酸螯合鈣產品迄今較少見報道。本試驗以羅非魚加工下腳料魚頭、魚排為原料,采用Plackett-Burman設計、最陡爬坡試驗和中心組合設計優化出最適螯合工藝條件,并對比、分析酶解液和螯合鈣產品中的氨基酸組成及其含量,以期為魚類加工下腳料的高值化利用提供參考。
1 材料與方法
1.1 材料與試劑
魚頭、魚排:廣州市恒發水產有限公司;
鈣標準溶液:濃度為(999±2)mg/L,德國 Merck公司;
胰蛋白酶:酶比活力1×105U/g,廣州齊云生物科技有限公司;
風味蛋白酶:酶比活力8×104U/g,廣州華琪生物有限公司;
氨基酸標準品:美國sigma公司;
其它試劑:均為分析純;
試驗所有用水:均為超純水。
1.2 儀器與設備
離心機:TD5A-WS,湖南賽特湘儀離心機儀器有限公司;
pH 計:PB-10,德國Sartorius集團;
恒溫水浴鍋:DK-S 24型,上海森信實驗儀器有限公司;
電熱恒溫鼓風干燥箱:DHG-9145型,上海恒科技術有限公司;
旋轉蒸發儀:EYELA N-1000,托普儀器有限公司;
紫外/可見分光光度計:Spectronic GENESYS 5,美國Thermo公司;
智能電位滴定儀:809Titrando,瑞士萬通中國有限公司;
原子吸收分光光度計:AA240FS,美國Varian公司;
微波消解器:MARS5,美國CEM公司;
氨基酸自動分析儀:日立835-50型,日本日立公司。
1.3 方法
1.3.1 復合氨基酸螯合鈣制備工藝流程

1.3.2 復合氨基酸液制備 取一定質量魚頭、魚排,剁碎,按以下條件酶解:固液比3∶1(m∶V),pH 6.5,酶濃度1.5%,復合酶比例(風味蛋白酶∶胰蛋白酶)1∶3,酶解溫度50℃,酶解時間4h。酶解結束后,將酶解液溫度升至90℃并保持20min滅酶,冷卻,過濾,濾液貯藏于4℃備用。
1.3.3 Plackett-Burman設計 影響螯合率的可能因素有pH值、反應溫度、氨基態氮濃度、時間、復合氨基酸液∶鈣液(體積比)等[13,14],對這5個因素進行考察,選用N=6的Plackett-Burman設計,并設1個空白作為誤差分析項。每個因素取高(+1)低(-1)兩個水平,以螯合率作為響應值,運用Minitab 15軟件分析計算各因素的效應值,并對各因素效應進行t檢驗,選擇顯著因素進一步試驗。各因素所代表的參數、水平見表1。
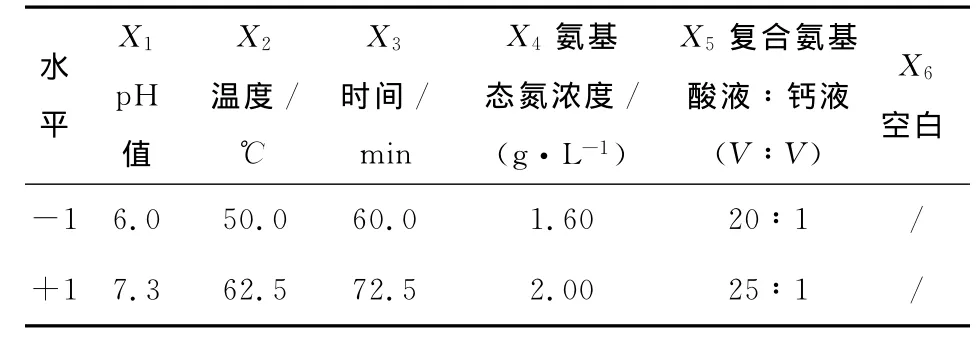
表1 Plackett-Burman設計的因子水平表Table 1 Factors and levels of Plackett-Burman design
1.3.4 最陡爬坡試驗設計和中心組合試驗設計 由Plackett-Burman法篩選出的顯著因子是pH值(X1)和氨基態氮濃度 (X4),pH值的最小值和最大值分別取6.25、8.50,氨基態氮濃度的最小值和最大值分別取2.0、3.8,pH值、氨基態氮濃度的步長分別取0.25、0.2,進行最陡爬坡試驗。
根據最陡爬坡試驗結果,選擇pH值、氨基態氮濃度分別為8.25、3.60作為響應面試驗因素水平的中心點進行響應面試驗設計。響應面中心組合設計的因素及水平見表2。
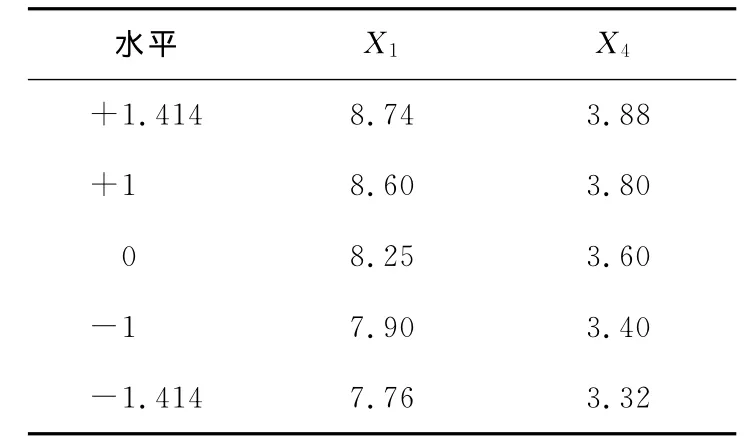
表2 響應面中心組合設計的因子水平表Table 2 Factors and levels of response surface central composite design
1.3.5 鈣的測定 采用微波消解-火焰原子吸收分光光度法測定。
(1)樣品前處理:稱取樣品約0.500g,置于聚四氟乙烯消解罐中,加入硝酸10mL,在微波消解儀中消解(功率800W,比例100%,升溫時間15min,消解溫度180℃,保持時間20min)。消解結束后,取出消解罐,冷卻,將消解液轉移至聚四氟乙烯溶樣杯中,在電熱板上于180℃趕酸直至消解液為無色透明,冷卻,然后將其轉入100mL容量瓶中用20g/L氧化鑭定容至刻度,待測定。
(2)儀器操作參數:波長422.7nm,夾縫0.5nm,空氣流量13.5L/min,乙炔流量2.00L/min,燈電流10.0mA。
1.3.6 游離氨基酸含量的測定 游離氨基酸樣品制備:稱取約0.100 0g樣品,加入5%磺基水楊酸10mL浸提24h,離心(15 000r/min,4℃,15min),收集上清液;重復以上步驟兩次,合并上清液,移入50mL容量瓶中,用水定容,待上機分析。儀器測定條件:離子交換柱,2.6mm×150mm;交換樹 脂 型 號,NO.2619(52051);柱 溫,53 ℃;泵 流 速:0.225mL/min;泵壓力:90kg/cm2;洗脫液:IPH-1,2,3,4;分析時間:72min;進樣體積:50μL。
1.3.7 螯合率計算 螯合率按式(1)計算:

式中:
c—— 螯合率,%;
m1——鰲合態鈣元素含量,g;
m2——反應體系中鈣元素含量,g。
1.4 統計分析
采用Minitab 15軟件對試驗數據進行分析。
2 結果與分析
2.1 Plackett-Burman試驗設計及結果
Plackett-Burman試驗設計及結果見表3、4。由表4可知,對螯合率有顯著影響(P<0.05)的因子是pH值和氨基態氮濃度,二者對螯合率均有正效應,要提高螯合率可以適當提高pH值和氨基態氮濃度。其它因素影響不顯著,可以維持在較低水平。
2.2 最陡爬坡試驗設計及結果
響應面擬合方程只有在考察的鄰近區域里才能較好地反映真實情形,所以,要先逼近最大螯合區域后才能建立有效的擬合方程。根據Plackett-Burman法篩選出的顯著因子效應大小設定它們的步長,進行最陡爬坡試驗設計,尋找最大螯合區。
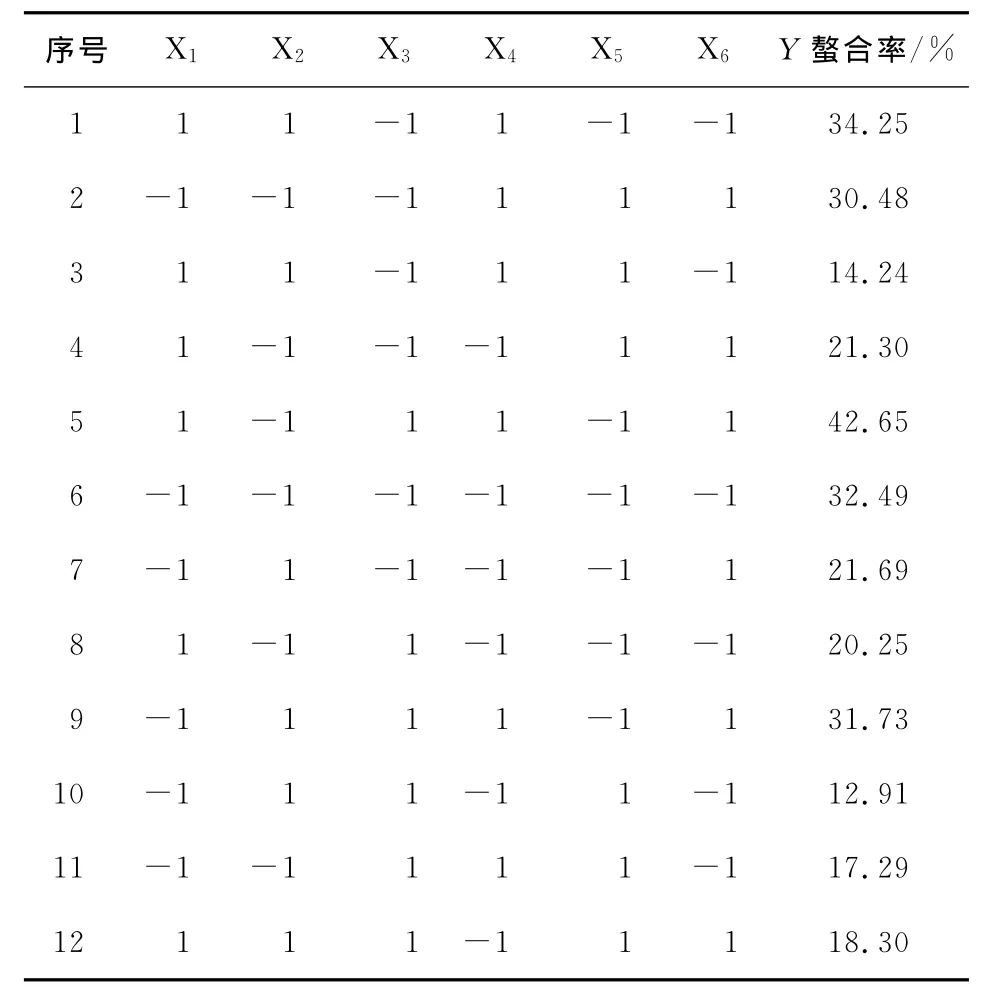
表3 Plackett-Burman試驗設計及結果Table 3 Experimental design of Plackett-Burman and corresponding rusults
由表4可知,pH值和氨基態氮濃度為顯著影響因子,因此選擇這兩個因子進行最陡爬坡試驗。由于pH值對螯合效果的影響較大,選pH值作為標準,按照pH遞增,氨基態氮濃度相應遞增設計試驗,pH值、氨基態氮濃度的步長依次取0.25、0.2。最陡爬坡試驗設計及結果見表5。由表5可知,最大螯合率出現在第9次試驗附近,故以試驗9的條件作為中心組合試驗設計的中心點。
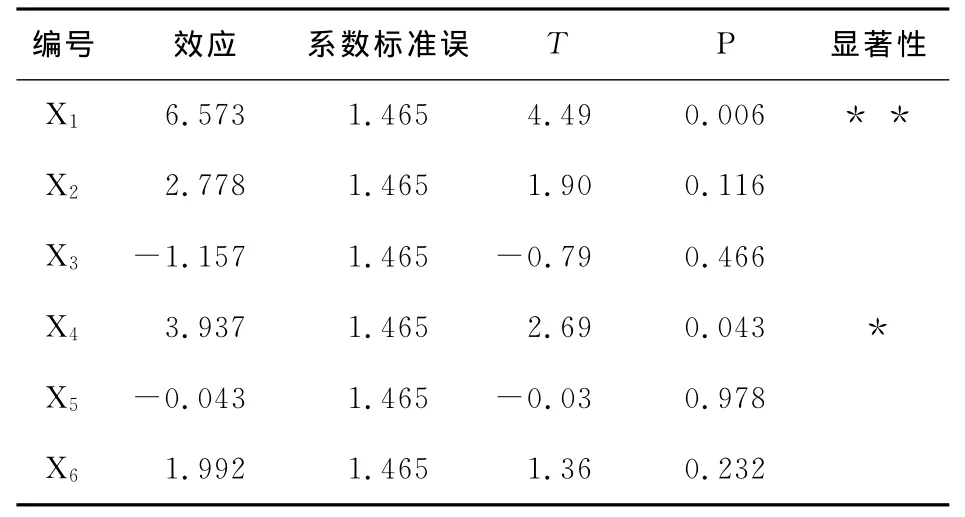
表4 Plackett-Burman試驗參數估計表 Table 4 Parameter estimation of Plackett-Burman design
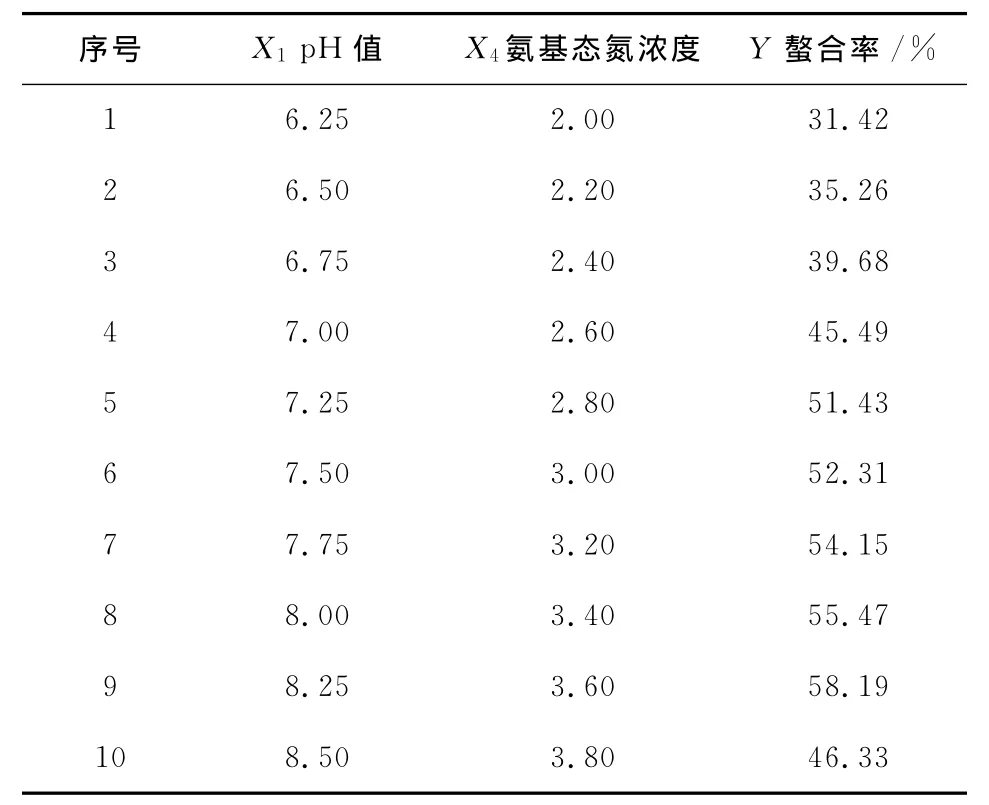
表5 最陡爬坡試驗設計及結果Table 5 Experimental design of steepest ascent and corresponding results
2.3 響應面分析法優化工藝條件
以螯合效果最好的區域進行響應面中心組合試驗設計,2因素5水平的響應面中心組合試驗設計及結果見表6。
2.3.1 回歸模型的建立及置信度分析 由Minitab 15軟件擬合的方程:
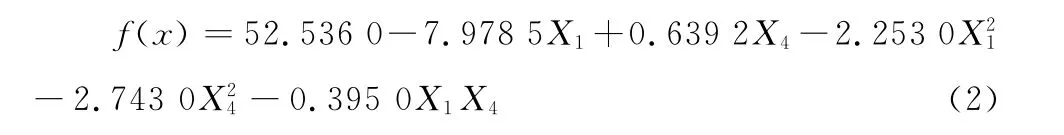
回歸模型系數的估計見表7,方差分析見表8。由表7、8可知,交互項的系數和均方差較小,說明響應面分析所選的2個因素之間交互效應較小。在α=0.01水平上,該模型失擬不顯著,回歸高度顯著。決定系數R2=97.89%,表明97.89%的變化可由此模型解釋,因此可以用上述模型代替真實試驗點對復合氨基酸螯合鈣的螯合率進行分析和預測。
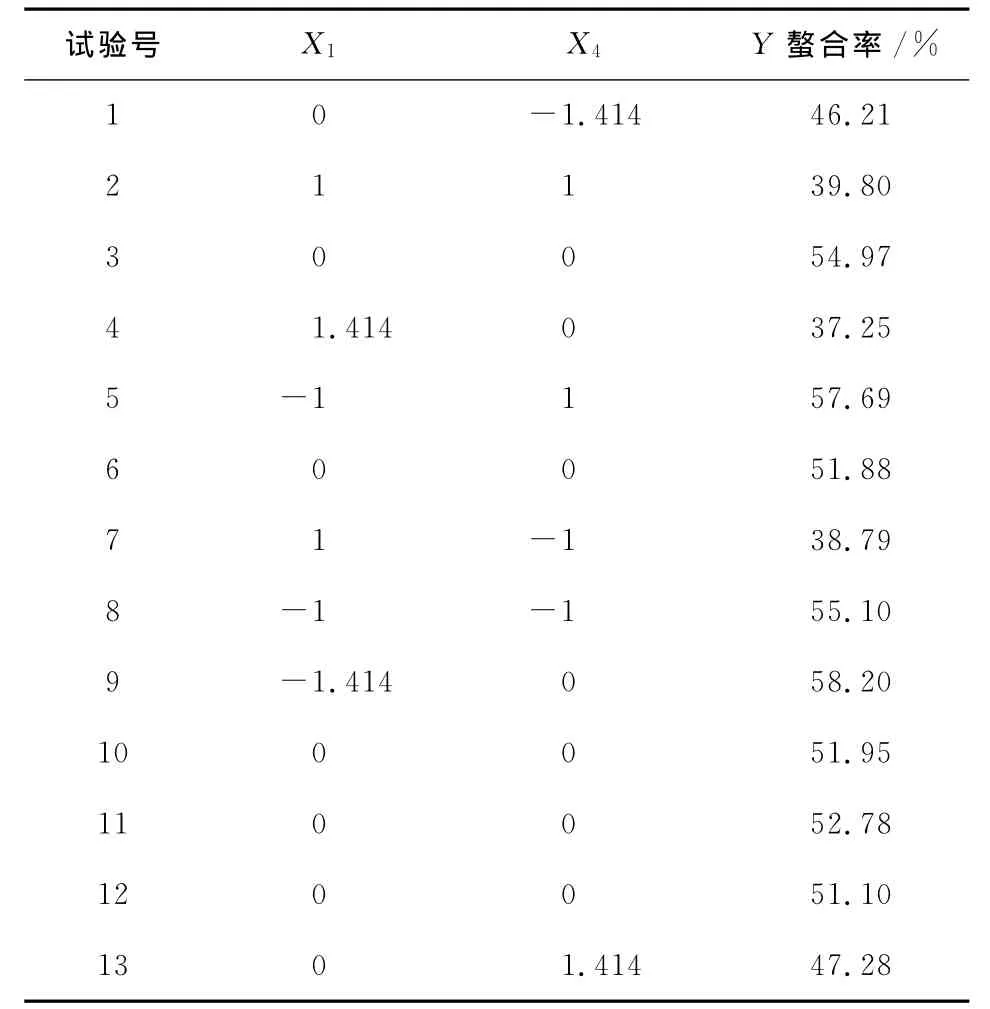
表6 中心組合試驗設計及結果Table 6 Central composite design and corresponding results
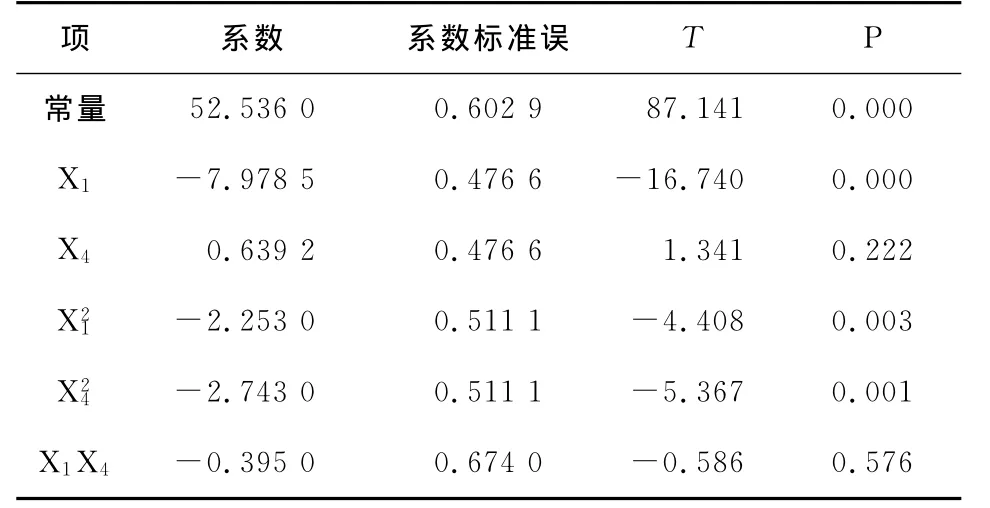
表7 中心組合試驗設計參數估計表Table 7 Parameter estimation of central composite design
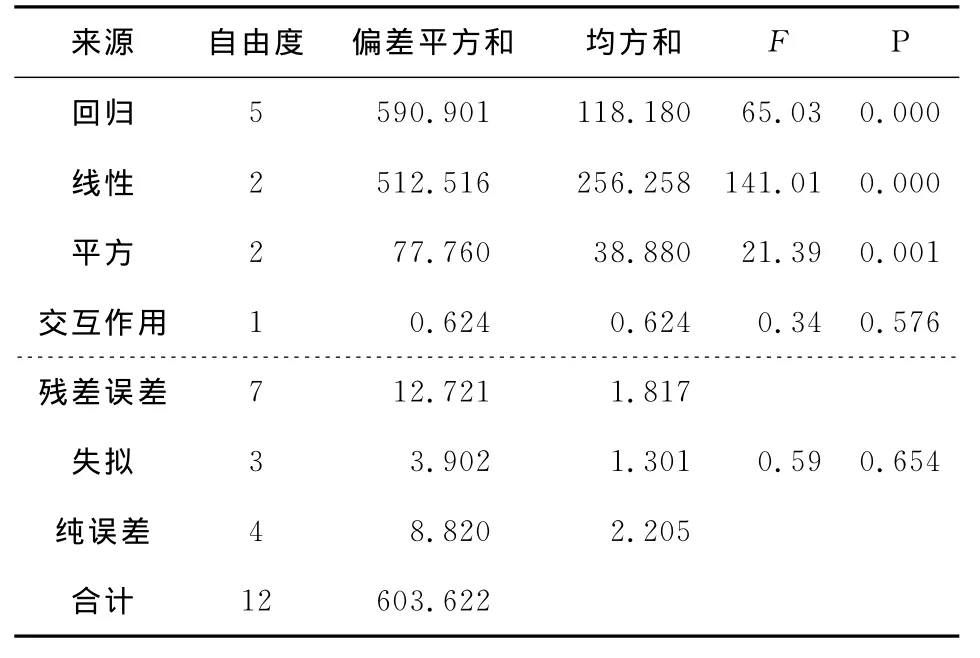
表8 中心組合試驗設計方差分析表 Table 8 Analysis of variance for central composite design
2.3.2 顯著因素水平的優化 運用Minitab 15軟件對回歸方程進行分析,結合圖1、2三維響應面圖和等高線圖可求出的該方程的最大值及對應的因素水平X1= -1.414,X4=0.271 4,即pH 值為7.896 5,氨基態氮濃度為3.654 3g/L。考慮到實際的操作,pH取7.90,氨基態氮濃度為3.66g/L。優化后的螯合工藝參數:pH 值7.90,溫度50℃,時間60min,氨基態氮濃度為3.66g/L,復合氨基酸液∶鈣液為20∶1(V∶V),此時的理論最大螯合率為62.04%。而實際螯合率為58.19%,說明實際產量與預測值比較接近,模型能很好的預測螯合情況。
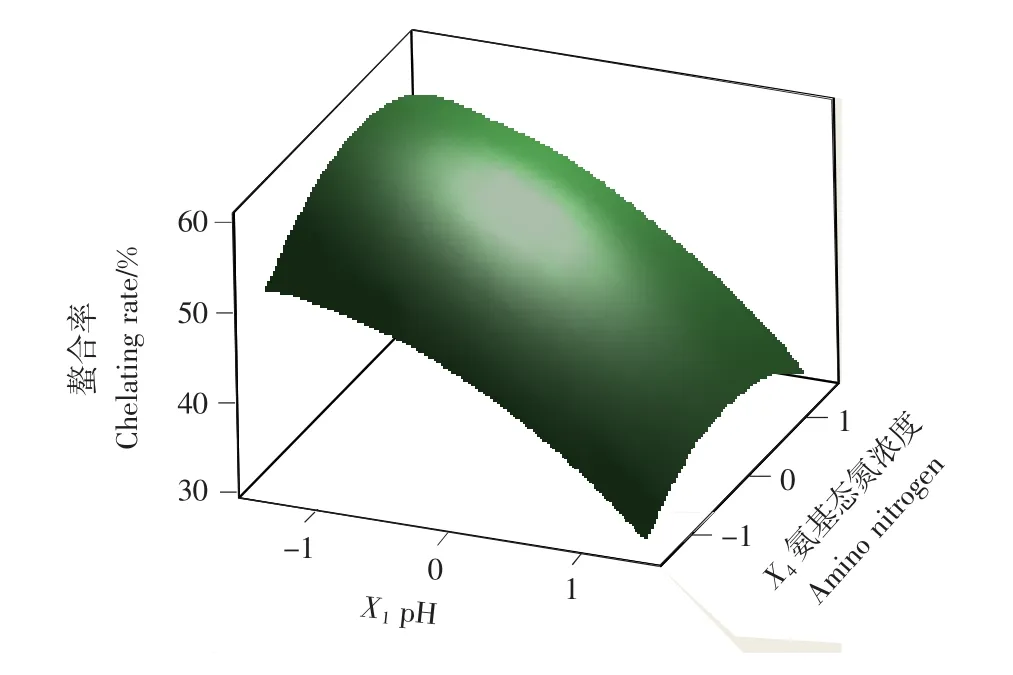
圖1 pH值和氨基態氮濃度對螯合率的響應圖Figure 1 Surface plot for the effects of pH vs.amino nitrogen concentration on chelating rate
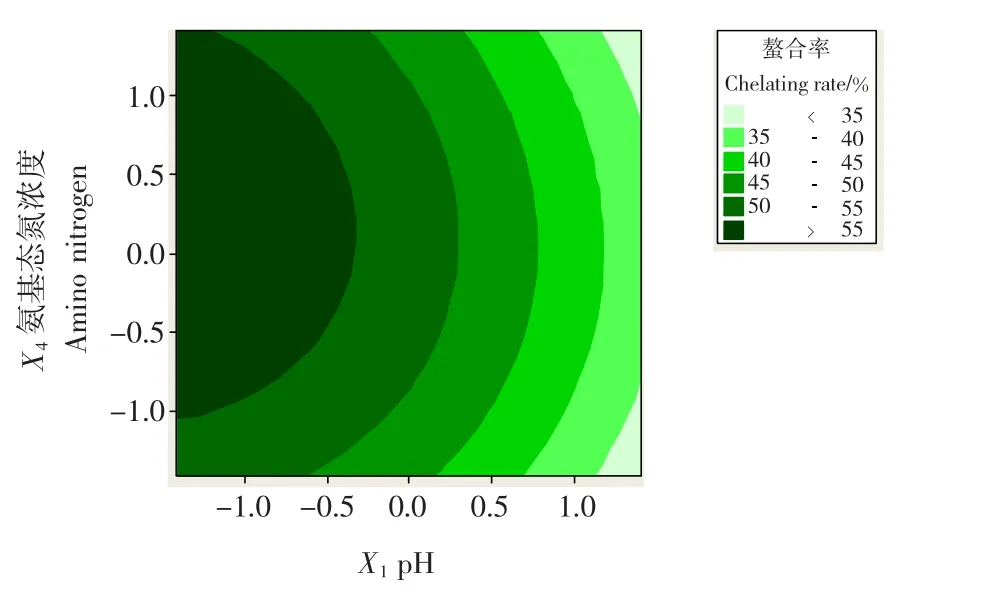
圖2 pH值和氨基態氮濃度對螯合率的等高線圖Figure 2 Contour plots for the effects of pH vs.amino nitrogen concentration on chelating rate
2.4 復合氨基酸液與螯合鈣產品中的氨基酸組成對比分析
由表9可知,復合氨基酸液中含量最多的6種氨基酸依次是亮氨酸、賴氨酸、精氨酸、苯丙氨酸、蘇氨酸、纈氨酸(含量均大于2.4mg/mL),它們之和占到氨基酸總量的61.45%;對應螯合鈣中含量最多的氨基酸也依次是這6種,它們占到螯合鈣氨基酸總量的62.43%。此外,在復合氨基酸液中含量小于2.0mg/mL的丙氨酸、甲硫氨酸、甘氨酸分別占氨基酸總量的百分比為5.07%、4.62%、2.66%,但在螯合鈣中三者占氨基酸總量的百分含量則分別為4.02%、5.15%、4.21%,這說明復合氨基酸液與鈣液螯合時,甲硫氨酸和甘氨酸對鈣的螯合能力均大于丙氨酸。
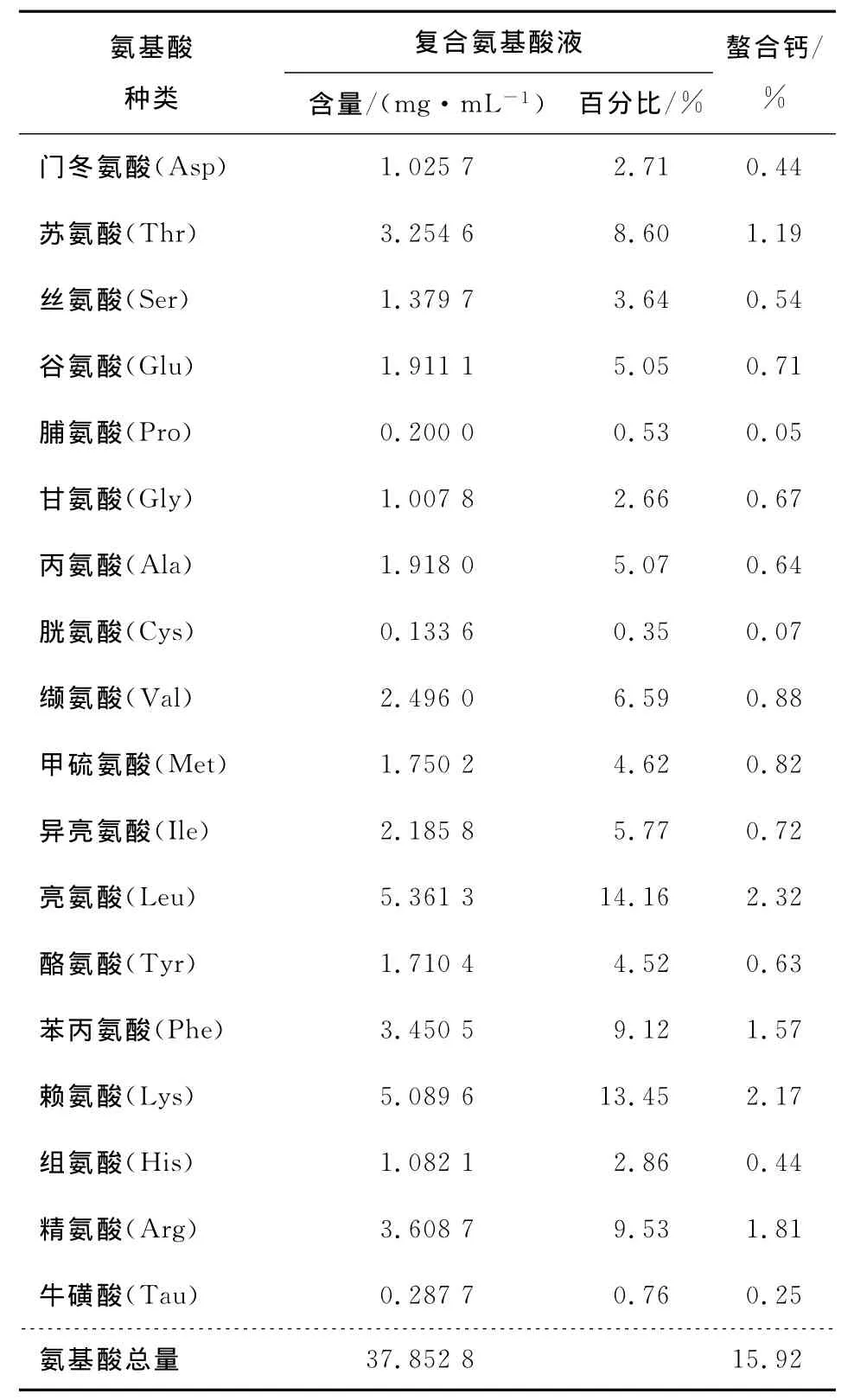
表9 復合氨基酸液與螯合鈣中的氨基酸種類和含量Table 9 Variety and content of amino acid in compound amino acid solution and chelated compound amino acid calcium
3 結論
(1)優化后的螯合工藝參數:pH值7.90,溫度50℃,時間60min,氨基態氮濃度為3.66g/L,復合氨基酸液∶鈣液為20∶1(V∶V)。在此條件下理論螯合率為62.04%,而實際螯合率為58.19%,說明實際產量與預測值比較接近,模型能很好的預測螯合情況。
(2)復合氨基酸液中的氨基酸種類及其含量對螯合效果影響較大,當氨基酸含量大于2.1mg/mL時,螯合鈣中對應的氨基酸相對含量也較高;復合氨基酸液中含量小于2.0mg/mL的丙氨酸、甲硫氨酸、甘氨酸,在復合氨基酸液與鈣液螯合時,前兩者對鈣的螯合能力均大于丙氨酸。
(3)所制得的復合氨基酸螯合鈣產品為粉末狀,色澤淡黃,具特有的鮮味,暴露于空氣中易吸潮變粘,鈣含量為26.14mg/g,溶解度為78.42g/100g,水溶液 pH 值 為6.23±0.05。
1 鄭清,王玉琴.利用文蛤殼制備復合氨基酸螯合鈣[J].安徽化工,2009,35(1):25~28.
2 張茜,曾凡駿,曾里.氨基酸螯合鈣奶味咀嚼片的研制[J].食品工業科技,2006,27(8):132~134.
3 王俊,程薇,文莉,等.復合氨基酸螯合鈣對大鼠生物利用率的研究[J].湖北農業科學,2008,47(12):1 492~1 494.
4 楊洋.羅非魚4月市場報告[J].當代水產,2010(5):84~85.
5 魏凌云,錢建強,魏鵬,等.谷氨酸螯合鈣的合成條件研究[J].氨基酸和生物資源,2009,31(3):43~46.
6 甘林火,翁連進,劉青,等.制備L-亮氨酸螯合鈣的新工藝及其生物利用度的研究[J].食品與發酵工業,2008,34(3):53~57.
7 常達正,張經坤.氨基酸鈣的制備方法及其應用:中國,96100091[P].1997-07-16.
8 郭艷.水解米渣蛋白及制備氨基酸螯合鈣的工藝研究[D].成都:四川大學,2006.
9 朱迎春,黃素珍.復合氨基酸螯合鈣的開發研制[J].山西農業大學學報(自然科學版),2009,29(2):173~177.
10 夏松養,謝超,霍建聰,等.魚蛋白酶水解物的鈣螯合修飾及其功能活性[J].水產學報.2008,32(3):471~477.
11 高明俠,秦衛東,苗敬之,等.雙酶解工藝制備復合L-氨基酸鈣及生物利用的研究[C]//第十一屆中國國際食品添加劑和配料展覽會學術論文集.北京:中國食品添加劑生產應用工業協會,2007:274~280.
12 黃素珍,楊國勝,朱迎春,等.動物骨骼復合氨基酸螯合鈣的開發與研究[J].肉類研究,2009(3):78~82.
13 吳玥霖,王俊.魚骨粉制備復合氨基酸螯合鈣工藝研究[J].食品與發酵科技,2009,45(1):51~54.
14 胡振珠,楊賢慶,馬海霞,等.羅非魚骨粉制備氨基酸螯合鈣及其抗氧化性研究[J].食品科學,2010,31(20):141~145.
Optimization of synthetization process for chelated compound amino acid calcium
MA Hai-xia1,2YANG Xian-qing1,2HU Zhen-zhu1
ZHANG Zhen1CHEN Sheng-jun1YANG Yan1
(1.South China Sea Fisheries Research Institute,CAFS,Guangzhou,Guangdong510300,China;2.National R&D Center for Aquatic Product Processing,Guangzhou,Guangdong510300,China)
The chelating condition of chelated compound amino acid calcium from fish heads and fish ribs was optimized using Plackett-Burman design,steepest ascent design and central composite design.The experiments results indicated that pH value and the concentration of amino nitrogen significantly affected the chelating rate(P<0.05).The variety and content of amino acid in compound amino acid solution also had influence to the chelating rate,the amino acid content in the chelated calcium was higher when the amino acid concentration was more than 2.1mg/mL,and calcium was easier to be chelated by methionine and glycine than alanine.The optimal chela-ting condition for maximum chelating rate was:pH value 7.9,temperature 50℃,chelating time 60min,concentration of amino nitrogen 3.66g/L,volume ratio(volume of compound amino acid solution:volume of calcium solution)20∶1,and the highest chelating rate was 58.19%.
Plackett-Burman design;chelated compound amino acid calcium;methionine;glycine;chelate
10.3969/j.issn.1003-5788.2012.01.057
國家現代農業產業技術體系(編號:CARS-49);國家農業科技成果轉化資金項目(編號:2010GB23260577;2010GB2E000335);廣東省科技計劃項目(編號:2009A020700004);廣東省水產蛋白改性技術研究團隊專項經費(編號:2011A020102005)
馬海霞(1977-),女,中國水產科學研究院助理研究員,碩士。E-mail:haixiam@gmail.com
楊賢慶
2011-11-10

