CS-PVA-NH4Cl共混固態聚合物電解質膜的制備與性能
楊 丞,閆康平
(四川大學化學工程學院,四川 成都 610065)
0 引 言
固態聚合物電解質(SPE)作為近年來廣受關注的新型電解質,可廣泛應用在燃料電池、電化學傳感器、超級電容器等領域,而作為薄膜電池等一類新型微型能源裝置的關鍵組成部分,其諸如電導率,電化學穩定窗口等性能的優劣直接決定了電池性能的好壞。SPE膜過去主要采用PEO[1]作為基體進行摻雜改性。
聚乙烯醇(polyvinyl alcohol,PVA)具有良好的成膜性質,生物相容性,可降解性,已被廣泛運用于生物醫學領域;在電化學方面,聚乙烯醇作為成膜材料為摻雜的導電劑提供場所,也得到了很好的效果[2]。陳忠元等使用Nb2O5摻雜PVA得到的SPE室溫電導率在10-3S·cm-1數量級[3]。殼聚糖(chitosan,CS,1,4-二氨基-2-脫氧-β-D-葡萄糖)由于其具有的成膜性能,無毒無害,豐富的來源等特性,已經在紡織、化妝品等領域得到了廣泛應用,而作為SPE膜基體,單純的殼聚糖膜電導率在10-5S·cm-1,且較脆、力學性能欠佳,還無法作為電解質實際運用[4]。文獻[5]中對其進行了廣泛的電導率改性工作,A K Arof等向殼聚糖主體中添加油酸作為增塑劑,并添加LiOAc作為添加鹽類,在含有質量分數40%LiOAc與10%OA最高電導率達到了10-5S·cm-1數量級[5],Ying Wan等將殼聚糖作為基礎結構矩陣并在其中溶解KOH提供導電離子,得到室溫下含5.5~8.5wt.%KOH 電導率為10-6S·cm-1的干燥薄膜[6]。制備方法上,聚乙烯醇(PVA)具有良好的成膜性能,成膜后具有良好的機械性能,并能與殼聚糖很好的互溶,與殼聚糖進行共混,避免了使用有毒的戊二醛對PVA進行交聯,且可以用工藝簡單的溶液澆鑄法進行SPE膜制備,CS-PVA體系SPE膜由于其兩種基體材料的良好性能得到了越來越多的關注,對其添加無機鹽類進行改性后能大大提高膜電導率和穩定性[7]。
對導電機理的解釋方面,SPE膜的導電性能高度依賴于其內部含水量[8]。R H Y Subbaw等使用弱電解質理論解釋添加NaClO4于1 g/100 ml殼聚糖-乙酸溶液中,室溫下緩慢干燥得到含有NaClO4的乙酰基殼聚糖薄膜,認為在酸性水溶液中,殼聚糖的氨基被質子化,使得殼聚糖表現出一種陽離子聚合物的性質,摻雜的鹽類陽離子被吸附在殼聚糖的氮、氧原子之上[9]。由于胺官能團上氮氧原子與其中鹽類的共同存在,導致殼聚糖SPE膜的導電機理十分復雜,目前公認的主要解釋來自Rice與Roth對其SPE膜提出的離子傳導模型[10]。
筆者將作為傳統工業電解液的NH4Cl使用到SPE膜中進行摻雜改性,使用溶液澆鑄法制備得到CS-PVA-NH4Cl體系SPE膜,并利用Zview軟件對得到的交流阻抗進行擬合,使用Hebb-Wagner直流極化法測量離子遷移率[11],循環伏安測得該膜電化學穩定窗口,以期能夠得到性能優良,能夠在電池等電化學器件中實際使用的固態聚合物電解質膜。
1 實 驗
1.1 聚合物電解質膜的制備
分別將3.6 g殼聚糖(AR,分子量1.0×105~3.0×105,成都科龍)常溫下溶于100 ml 1%冰乙酸溶液,2.4 g聚乙烯醇(AR,聚合度DP=1799±50,成都科龍)95℃下溶于100 ml去離子水中,二者充分攪拌混勻后分別按比例加入NH4Cl,得到的均勻粘稠液體倒入有機玻璃模具中,室溫下靜置脫泡,恒溫干燥箱內50℃下干燥得到CS-PVA-NH4Cl電解質膜,按其中NH4Cl質量分數0、10%、20%、30%、40%、50%、60%分別編號為0#、1#、2#、3#、4#、5#、6#,同一編號下澆鑄4個樣本進行測試后計算平均值。
1.2 性能測試
1.2.1 溶脹度計算
將完全干燥后薄膜稱重再用去離子水充分浸泡,用濾紙吸干表面水分,溶脹度R由式(1)計算:
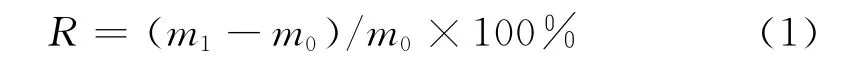
式中,m1為充分吸水后膜重;m0為干燥狀態下膜重。
1.2.2 電導率δ的測定
將充分吸水后的固態電解質膜剪為圓片,用濾紙吸去薄膜表面水分,夾在兩片直徑2.4 cm的高壓石墨電極之間構成 C/CS-PVA-NH4Cl/C電極體系,連接到普林斯頓273 A電化學工作站上進行測試,測試頻率范圍105Hz~10 Hz,正弦波擾動振幅5 mV。電導率δ采用式(2)進行計算:

式中,Rb為電極體系電阻,在本文采用的電極體系中即可認為是固態電解質膜本體電阻,由Zview軟件進行擬合得到;A為電解質膜有效工作面積;l為固態電解質膜厚度。
1.2.3 離子遷移數(tion)的測定
在上述電極體系兩邊施加穩定直流電壓,測試通過體系的電流逐漸降低并趨于穩定,得出電流-時間曲線,并按式(3)計算[12]:
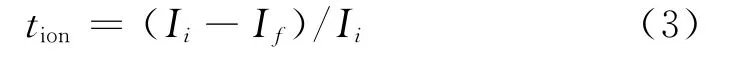
式中,Ii為初始總電流,是離子電流與電子電流之和;If為最終穩定電流,僅為電子電流。
1.2.4 電化學穩定窗口測試
將上述電極體系連接到普林斯頓273 A電化學工作站,掃描速度1 mV/s,掃描范圍-2.0V~2.0V,進行循環伏安測試,得到穩定電化學窗口電壓。
2 結果與討論
2.1 外觀與溶脹度
干燥后的薄膜外觀呈均勻半透明的淡黃色,伴隨NH4Cl添加量增加,顏色逐漸變為白色,具有一定的韌性,使用游標卡尺測量厚度平均值為0.15 mm。溶脹度R根據式(1)計算,各個試樣溶脹度結果如表1。
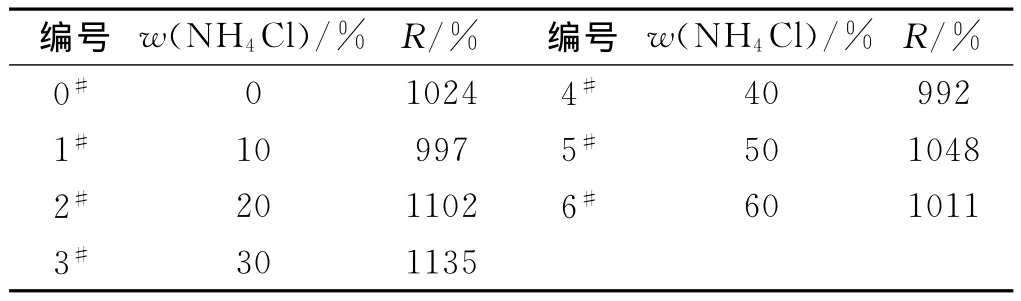
表1 不同NH4Cl摻雜量聚合物電解質膜溶脹度
在文獻中確定的殼聚糖與聚乙烯醇最佳配比為3:2基礎上添加NH4Cl后,各個試樣溶脹度均為10倍左右,主要是由于殼聚糖及聚乙烯醇都具有良好的吸濕率,膜內部大量的自由水給離子遷移提供了場所和通道。
2.2 交流阻抗譜擬合
本實驗中采用 C/CS-PVA-NH4Cl/C電極體系,利用離子阻塞型石墨電極進行交流阻抗測試,圖1為樣品交流阻抗譜,對于理想的電解質膜譜圖應為垂直于實軸的一條直線,即只有體系電阻R1存在,但由于電極表面粗糙、電解質共混無法形成完全均一體系等因素影響,在高頻區會出現半弧,半弧在模擬電路中使用CPE元件(Constant Phase Element、常相元素)代表,是容抗與感抗的共同作用,Z 滿足式(4)[13]:

此時的Z在n值降低時,阻抗譜高頻半弧會被壓扁。n=1時為理想電容,n=0時為理想電阻,可見所制備的聚合物電解質膜伴隨電導率的升高,圓弧半徑逐漸減小,n值逐漸增大,電解質表現出更多的電容性質。當電阻小到圓弧最高點頻率超過儀器測定頻率范圍時,在阻抗復平面圖上,除了低頻區的直線,高頻區的圓弧很短或直接消失,在40%NH4Cl摻雜時電導率達到最高,在復平面圖上只能觀測到一條直線。在低頻區通過電解質膜的電流可以近似認為是直流電,由于直流電的作用,膜內部開始有擴散發生,伴隨擴散過程導致電極表面出現厚而致密的鈍化膜時,膜內擴散阻抗用Warburg阻抗W1表示,由于W1的存在,曲線發生上翹,在低頻部分表現為一條45°傾斜向上的斜線,離子的遷移過程受到極大的抑制,并使得半圓弧右端無法與實軸相交。但這不影響電導率的測定和后續的擬合。
文獻中往往采用直線外推的方法求得與實軸的交點即體系電阻Rb,本文使用Zview交流阻抗擬合軟件進行擬合計算,圖2為交流阻抗譜等效電路。
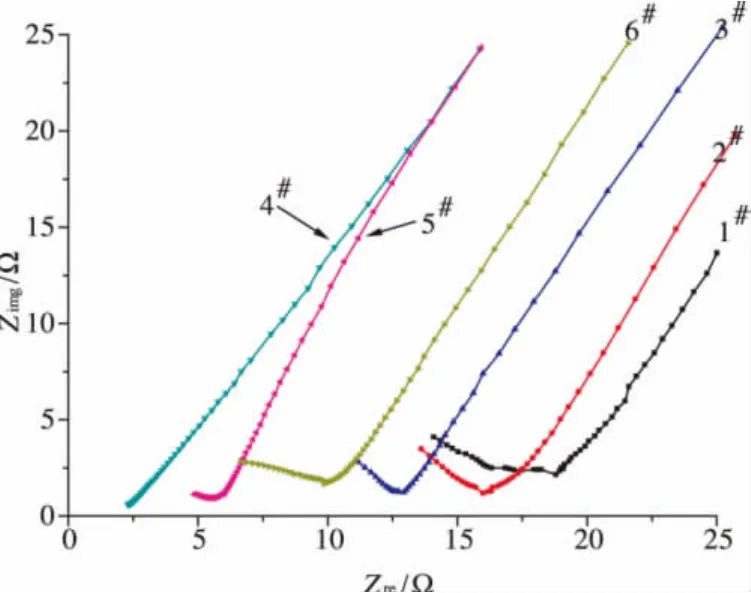
圖1 不同NH4CI摻雜固體聚合物電解質膜交流阻抗譜
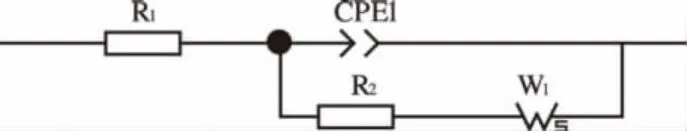
圖2 交流阻抗譜等效電路
由于固態聚合物電解質膜同時受電化學和濃差極化混合控制,交流信號通過電極時,除了濃差極化外還將出現電化學極化,這時電極反應過程在高頻部分為雙電層的容抗弧,而在低頻部分,擴散控制將超過電化學控制,出現Warburg阻抗,其擬合后阻抗圖譜如圖3所示。該等效電路理想狀態下在阻抗復平面圖上的曲線為高頻區的一段圓弧和低頻區的一條直線。在通常測定電池電阻時,由于電導較小,在阻抗復平面圖上可以看到完整的高頻區圓弧,而半圓弧左端點與實軸交點即代表電池電極體系的體系電阻R1,右端點與實軸交點代表電極體系的體系電阻R1與極化電阻R2之和。
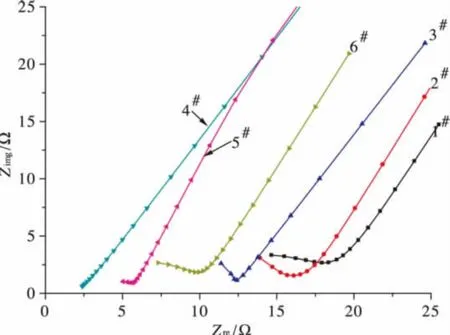
圖3 交流阻抗譜擬合圖譜
從擬合結果表2可以看出,NH4Cl的添加帶來了在膜內部可以自由遷移的導電離子,伴隨體系阻抗R1及極化電阻R2的降低,薄膜阻抗在不斷降低。CPE元件的兩個參數CPE-T及CPE-P中CPE-P的相位角參數變化在各個樣中均超過了0.5,即在式(4)中n>0.5,可以認為樣品在低頻區表現出更多的電容性質。Warburg阻抗W1受含水膜內部微觀結構導致離子擴散過程的不穩定,且導電過程由離子導電主導,無法忽略W1或設置為Fixed進行擬合的影響,三個參數變化缺乏規律,只能看出W1-R數值上0#比其他樣品至少大104倍,可認為主要是受摻雜的影響。
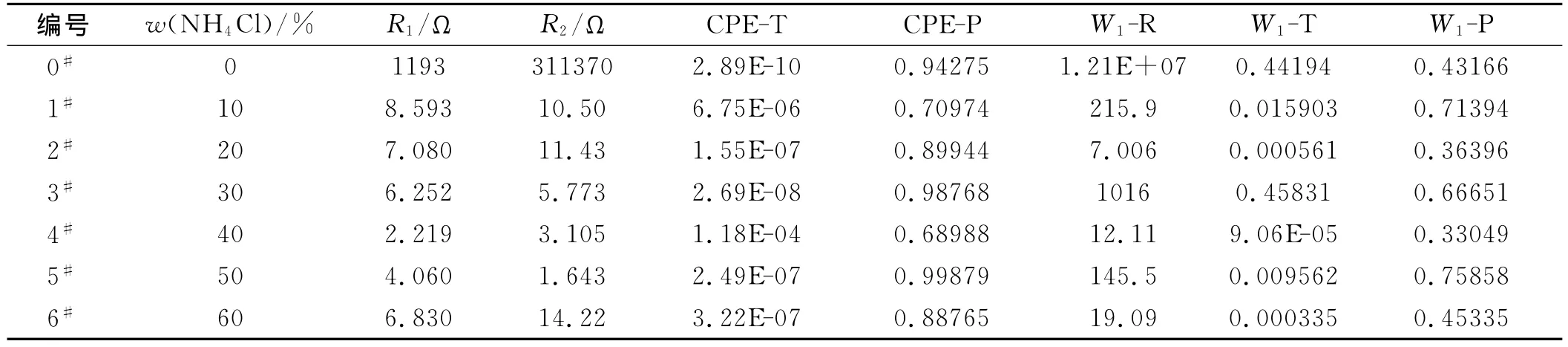
表2 不同NH4Cl摻雜量聚合物電解質膜擬合結果
2.3 NH4Cl含量對電導率的影響
由擴散主導的固體電解質薄膜電導率還可表示為式(5)

式中,n,e,μ分別為電荷載體的數量、電荷數與遷移能力[14],在摻雜同一種無機鹽類的情況下e為常數,σ取決于載體數量n、遷移能力μ。而遷移能力μ也受摻雜物自由離子濃度影響。如圖4可見,隨著NH4Cl摻雜濃度的增加,即n的增加,薄膜電導率逐漸提高,在40%摻雜量時得到了1.4×10-3S·cm-1的電導率。伴隨NH4Cl摻雜濃度的進一步增加,離子無法完全自由電離,且自由離子數量n受限于殼聚糖主體的吸收能力,離子在其中呈現一種“擁擠”的狀態,而實際上參與電荷載運與遷移的自由離子數量反而減少,導致遷移能力μ降低,最終導致電導率的降低。

圖4 不同NH4Cl摻雜固體聚合物電解質膜電導率
2.4 NH4Cl含量對離子遷移數的影響
在向本文使用的C/CS-PVA-NH4Cl/C體系施加一恒定直流電壓后,最初離子和電子都共同參與導電,隨后自由離子在高壓石墨離子阻塞電極處迅速耗盡,電流只剩下電子傳遞部分,過程逐漸達到穩態,由圖5可知,40%NH4Cl摻雜下薄膜為初始總電流Ii=1.46×10-5A,最終穩定電流If=0.10×10-5A,由式(3)得40%NH4Cl摻雜離子遷移率tion=0.93。而未摻雜的0#樣基本沒有離子遷移現象發生,且其I-T曲線波動很大。
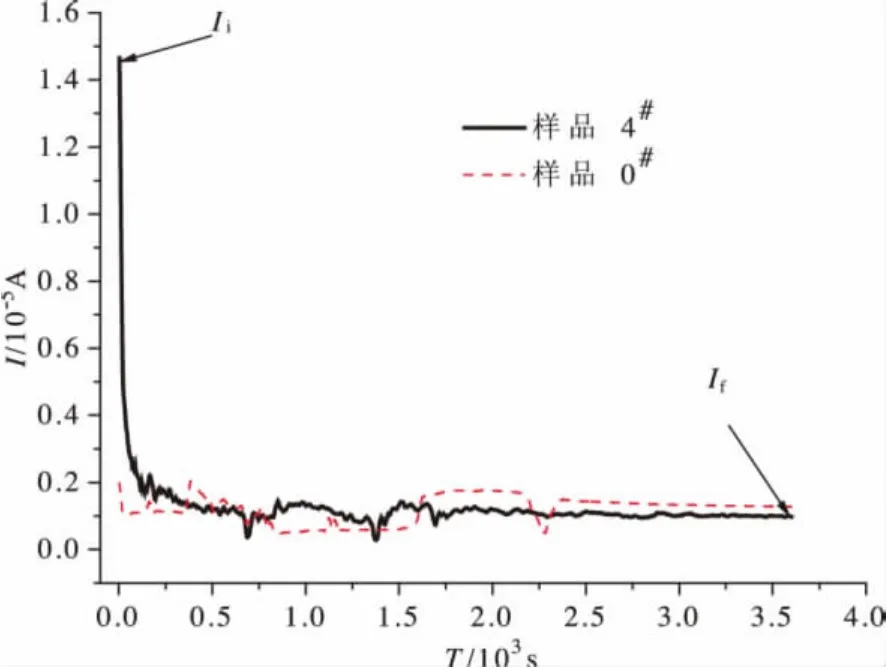
圖5 固體聚合物電解質膜電流-時間曲線
伴隨鹽含量的增加,wt.40%之前,離子遷移數不斷提高,可以認為溶解在電解質膜基體中的鹽類提供了更多的自由離子進行遷移,而超過40%之后,大量的離子在電解質膜中重新結合,自由離子數減少,離子遷移數反而下降,得到的離子遷移數計算如表3,離子遷移數的變化規律與電導率相同,最高值出現在40%摻雜量處,也證明了導電過程由離子導電主導。
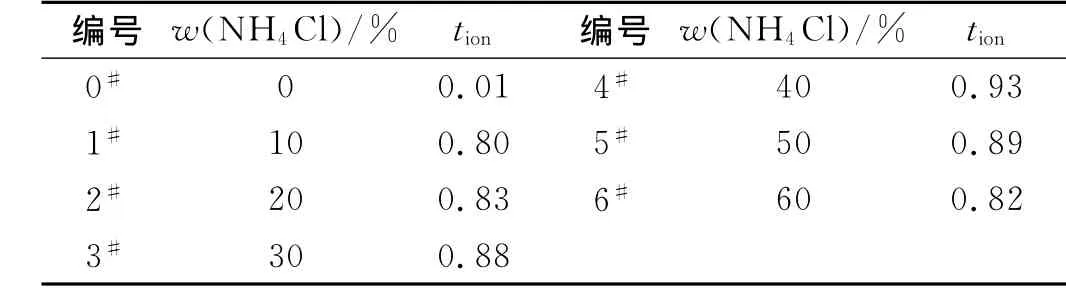
表3 不同NH4Cl摻雜量聚合物電解質離子遷移數
2.5 電化學穩定窗口
由圖6可知,樣品4#的極化電流出現在-1 V~1 V之間,電化學穩定窗口在2.0V左右,主要是由于CSPVA共混體系得到的膜具有良好的韌性和強度,添加NH4Cl在增強導電性的同時,對PVA有一定的增塑作用,可以推遲電解質極化的發生,拓寬電化學穩定窗口。
3 結 論
通過向CS-PVA體系中添加NH4Cl進行摻雜改性,采用溶液澆鑄法制備了SPE膜,具有良好的韌性和極高的溶脹度。在NH4Cl摻雜量40%時,通過對交流阻抗譜的擬合得到了1.4×10-3S·cm-1的室溫電導率。采用直流極化法測定該摻雜SPE膜導電過程由離子導電主導,在40%摻雜量時,離子電導率達到0.93的最高值,此時SPE膜室溫電化學穩定窗口在2.0V左右。
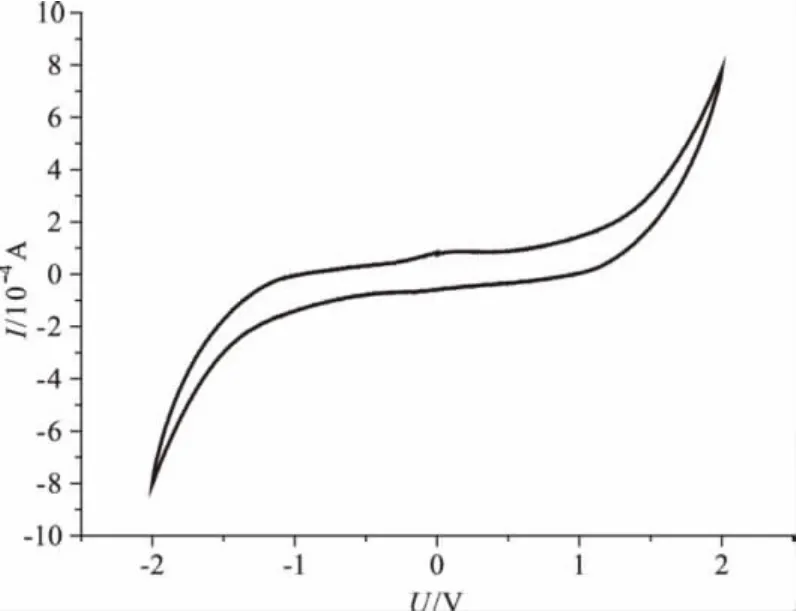
圖6 樣品4#的循環伏安曲線
采用共混溶液澆注法制備的CS-PVA-NH4Cl體系SPE膜,具有材料對環境友好,制備過程簡便,能達到較高的電導率的特點。但是其導電過程,電化學行為復雜,由多個不可忽略的電化學極化與擴散過程交互主導,通過使用等效電路對其進行數值模擬,可以加深對離子導電模型與相關電化學行為的了解。
[1]Fenton D E,Parker J M,Wright P V,et al.Complexe of alkali metal ions with poly(ethytlene oxide)[J].Polymer,1973,14:589-591.
[2]Arunima Saxena,Arvind Kumar,et al.Preparation and characterization of N-methylene phosphonic and quaternized chitosan composite membranes for electrolyte separations[J].Journal of Colloid and Interface Scien,2006,303:484-493.
[3]Chen Zhongyuan(陳忠元),JV Yalan(居亞蘭).PVA/Nb2O5復合堿性固體聚合物電解質的性能[J].Battery Bimonthly(電池),2009,39(4):200-202.
[4]Ying Wan,Katherine A M Creber,et al.Chitosan-based electrolyte composite membranes I.Preparation and Characterization[J].J.Membrane Science,2006,280:666-674.
[5]M Z A Yahya,A K Arof,et al.Effect of oleic acid plasticizer on chitosan-lithium acetate solid polymer electrolytes[J].European Polymer Journal,2003,39:897-902.
[6]Ying Wan,Katherine A M Creber,et al.Chitosan-based electrolyte composite membranes II.Mechanical properties and ionic conductivity[J].J.Membrane Science,2006,284:334-331.
[7]L S Ng,A A Mohamad,et al.Protonic battery based on a plasticized chitosan-NH4NO3 solid polymer electrolyte[J].J.Power Source,2006,163:382-384.
[8]Chun Chen Yang.Chemical composition and XRD analyses for alkaline composite PVA polymer electrolyte[J].Materials Letters,2003,58:33-38.
[9]R H Y Subbaw,A K Arof,et al.Polymer batteries with chitosan electrolyte mixed with sodium perchlorate[J].Material Science&Engineering B,1996,38:156-160.
[10]M J Rice,W L Roth.Ionic transport in super ionic conductors:a theoretical model[J].Journal of Solid State Chemistry,1972,4(2):294-310.
[11]WU Lingli(吳玲麗),WANG Shizhong(王世忠).La0.9Sr0.1Ga0.8Mg0.2AlxO3-σ(x=0~0.05)電解質電導率的研究[J].Battery Bimonthly(電池),2009,39(4):429-431.
[12]TANG Zhiyuan(唐致遠),WANG Zhanliang(王占良).塑料鋰離子電池用聚合物電解質性能表征[J].Polymer Materials Science and Engineering(高分子材料科學與工程),2002,18(2):33-36.
[13]CAO Chu nan(曹楚南),ZHANG Jian qing(張鑒清).電化學阻抗譜導論[M].Beijing(北京):Science Press(科學出版社),2002.
[14]Tan Winie,S Ramesh,et al.Studies on the structure and transport properties of hexanoyl chitosan-based polymer electrolytes[J].Physica B,2009,404:4308-4311.

