慢性低氧所致肺動脈高壓對大鼠肺血管平滑肌細胞及成纖維細胞中蛋白激酶CβI的膜轉位和蛋白表達量的影響
程振玲,于文燕,聶 欣,施熠煒,杜永成
(1.山西醫科大學附屬人民醫院呼吸科,太原 030001;2.山西醫科大學第一臨床醫學院呼吸科,太原 030001)
慢性低氧所致肺動脈高壓對大鼠肺血管平滑肌細胞及成纖維細胞中蛋白激酶CβI的膜轉位和蛋白表達量的影響
程振玲1,于文燕1,聶 欣1,施熠煒2,杜永成1
(1.山西醫科大學附屬人民醫院呼吸科,太原 030001;2.山西醫科大學第一臨床醫學院呼吸科,太原 030001)
目的 通過觀察慢性低氧所致肺動脈高壓對大鼠肺血管平滑肌細胞及成纖維細胞中蛋白激酶C βI(PKC βI)的膜轉位和蛋白表達量的影響,初步探討PKC βI在慢性低氧誘導大鼠肺動脈高壓的發生、發展過程中所起的作用。方法 建立慢性常壓低氧肺動脈高壓大鼠模型,將雄性SD大鼠隨機分為正常對照組、低氧1 d、3 d、7 d、14 d和21 d組,應用蛋白免疫印跡和免疫組化技術檢測肺動脈高壓形成過程中大鼠肺血管平滑肌細胞及成纖維細胞中PKC βI的膜轉位和蛋白表達水平。結果(1)RVSP和 RV/(LV+S)比值較正常對照組明顯增加(P<0.05),低氧后3 d、7 d、14 d和21 d后大鼠肺血管明顯增厚;(2)大鼠肺血管平滑肌細胞和成纖維細胞均有 PKCβI的表達,且低氧14 d后 PKCβI的蛋白表達量較正常對照組相比降低(P<0.05)。結論 PKCβI蛋白表達量的下調可能參與了慢性低氧誘導的大鼠肺動脈高壓肺血管重塑的發生、發展過程。
PKCβI;慢性低氧;肺動脈高壓;膜轉位;蛋白表達水平
肺動脈高壓(pulmonary hypertension,PH)是一組由異源性疾病和不同發病機制引起的以肺血管阻力持續增加為特征的臨床-病理生理綜合征,臨床表現為右心室后負荷增加,活動耐力下降,嚴重者可發生心臟衰竭而死亡,是最嚴重的具有潛在致命性的慢性肺循環疾病[1]。其基本病理生理特征是肺血管收縮和重塑。蛋白激酶C(protein kinase C,PKC)廣泛分布于哺乳動物細胞中,屬于絲/蘇氨酸蛋白激酶家族,參與了細胞生長、分化和轉化等多種生化過程,并且在激素、神經遞質、生長因子和抗原等信號的傳導中起到重要作用[2]。一些報道證實PKCβI表達在肺血管平滑肌和成纖維細胞中[3]。一些體外細胞實驗研究也證實了 PKCβI作為細胞增殖信號轉導通路的成員可能參與了肺動脈高壓肺血管重塑的形成[4],但對參與 PH形成的PKCβI的慢性常壓低氧大鼠的整體動物模型的研究尚無報道。本研究目的為通過觀察大鼠肺血管平滑肌細胞及成纖維細胞中 PKCβI的膜轉位和蛋白表達水平的變化,進而明確在動物整體模型中PKCβI是否參與慢性低氧誘導肺動脈高壓的發生、發展過程。
1 材料和方法
1.1 主要試劑及儀器
鼠源性單克隆抗體(Anti-β-actin)(美國Sigma公司)、BCA蛋白定量試劑盒(BCA protein assay kit)(美國 Pierce 公司)、Gel-Doc 凝膠成像分析系統(美國 Bio-Rad公司)、Leica Qwin圖像分析系統(德國 Leica公司)、蛋白/核酸分析儀(美國Barnstead公司)、高速離心機(美國 Barnstead公司)、超聲波粉碎儀(美國 Cole-Parmer公司)、平推式石蠟切片機(德國 Leica公司)、高壓氮氧混合氣罐、氧濃度分析儀等。
1.2 動物模型的建立和分組
清潔級健康雄性成年SD大鼠60只,體重200~250 g,由山西醫科大學實驗動物部提供【SCXK(晉)2009-9991】,隨機分成正常對照組、低氧1 d、3 d、7 d、14 d和21 d組,每組10只。正常對照組放置在空氣中,其余低氧組放置在低氧艙中低氧相應的天數,向艙內輸送氧氣和氮氣的混合氣體。低氧艙內用氧濃度分析儀來檢測氧氣濃度,控制艙內氧濃度在(10±0.1)%,艙內放置鈉石灰吸收 CO2,以無水CaCl2吸收水蒸氣。每天打開艙門60min,用于清理低氧艙、補充飼料和飲水。
1.3 右心室收縮壓(RVSP)和右心室肥大指數(RVHI)的測定
低氧各時相點結束后,分別從低氧各組和對照組中隨機選擇6只大鼠,10%水合氯醛(4mL/kg)腹腔注射麻醉后,經右頸總靜脈插入微導管,通過壓力傳感器接上壓力換能器和多導生理記錄儀測大鼠右心室收縮壓。測完后,取出心房,沿室間隔邊緣分離出右心室(RV)和左心室+室間隔(LV+S),用濾紙吸干水分后稱量 RV和 LV+S的重量,以RV/(LV+S)比值來反映右心室肥厚指數(RVHI)[5]。
1.4 肺組織蘇木精-伊紅(HE)染色
隨機取6只大鼠右下肺相同部位組織,用10%中性福爾馬林固定液(pH=7.4)固定,以梯度酒精順序脫水,二甲苯透明,石蠟包埋,沿肺門水平橫切,厚度約5 μm,進行HE染色。
1.5 PKC βI的膜轉位和蛋白表達檢測
1.5.1 肺血管的制備
低氧各時相點結束后,從低氧各組和對照組中隨機選擇6只大鼠,用10%水合氯醛腹腔注射麻醉后,剖胸取出肺臟,在手術顯微鏡下分離出肺動脈,放入Hanks液中漂洗,剪去鑷夾過的中膜,將動脈縱行剪開,使內膜朝上,以圓鈍的鑷子或剪刀背輕輕刮去內皮細胞。制備后的血管先用濾紙將組織液盡量吸收干凈,然后放入1.5mL的進口EP管中,立即放入液氮中凍存,備用[6]。
1.5.2 不同細胞組分的分離和提取
將凍存的肺動脈標本取出,加入組織裂解液Buffer A,手持式勻漿器勻漿、超聲破碎,離心(4℃、30000×g)30 min,吸取上清,即得到胞漿蛋白成分。在移去上清的沉淀中,加等體積的 Buffer B后,勻漿、超聲破碎,離心(4℃、30000×g)30 min,吸取上清,即得到膜相關蛋白成分。胞漿蛋白和膜相關蛋白用于PKCβI膜轉位的分析。將標本取出后,待標本未完全融開時,將標本剪碎,按每1 mg組織10 μL的比例加入Buffer C,勻漿、超聲破碎,使組織細胞溶解,即得到全細胞蛋白。全細胞蛋白用于PKCβI蛋白表達量的分析[7]。
1.6 蛋白免疫印跡(Western blot)
用BCA蛋白定量法對上述獲得的蛋白組分進行蛋白定量,用凝膠加樣緩沖液制備成電泳樣品。取50 μg樣品,用濃度為10%的凝膠進行電泳。電泳條件:4℃、恒流30 mA。電泳結束后將蛋白轉移到聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)膜上。轉膜條件:4℃、恒流 400 mA、3 h[8]。PVDF 膜用 TTBS緩沖液漂洗5 min,然后用10%脫脂牛奶將膜封閉1 h,用蒸餾水洗膜,再用 TTBS緩沖液洗膜3次,每次10 min。將膜放入濃度為1:500的兔源性單克隆抗體(Anti-cPKCβI)中,室溫下孵育 3 h。蒸餾水洗膜,再用TTBS緩沖液洗膜3次。將膜放入1:5000的辣根過氧化物酶(HRP)標記的山羊抗兔或山羊抗小鼠IgG中,孵育1 h。棄二抗,蒸餾水洗膜,再用TTBS緩沖液洗膜3次。根據美國Pierce公司ECL試劑盒的步驟,得到特異蛋白條帶的X光片[9]。
1.7 免疫組織化學染色(DAB)染色
將取出的肺組織固定4%的多聚甲醛中12~24 h,常規石蠟包埋、切片。二甲苯脫蠟,梯度酒精水化。室溫下,3%H2O2-PBS溶液封閉內源性過氧化物酶10 min,PBS漂洗。96℃抗原熱修復10 min。冷卻后PBS洗滌。37℃ 5%羊血清孵育10 min,封閉非特異性抗原的結合位點。吸取多余血清,加入一抗(1∶200),室溫下孵育3 h,4℃冰箱過夜。次日取出濕盒,37℃孵育40 min,用 PBS漂洗。加入生物素標記的羊抗兔免疫球蛋白(1∶300),37℃孵育30 min。棄二抗,PBS漂洗。加入辣根過氧化物酶標記的鏈霉卵白素(1∶300),37℃孵育 20 min。棄三抗,PBS漂洗。加 DAB避光顯色,至顯色滿意后終止反應。蘇木素復染數秒,梯度酒精、無水乙醇脫水。二甲苯透明、中性樹膠封片。用Leica Qwin圖像分析系統對切片進行觀察和拍照。
1.8 數據處理和統計學分析
1.8.1 Western-blot數據處理和統計學分析
實驗結果應用Gel Doc凝膠成像系統中的Quantity One圖像分析軟件進行定量分析。PKCβI膜轉位水平的表示方法由Quantity One圖像分析軟件分析得出胞漿,膜相關和膜蛋白成分中,PKCβI在X-膠片上的密度值。然后,計算出 PKCβI在膜相關組份的密度值與PKCβI在胞漿,膜相關和膜蛋白成分總的密度值的比值。以正常對照組的比值作為100%,其余各組用百分數表示 PKCβI膜轉位水平。實驗數據用SPSS for Windows11.5統計軟件進行單因素方差分析(One Way ANOVA),結果以均數±標準誤(X±S.E.)表示,差異顯著性水平 P<0.05,并用 Sigma-plot繪圖軟件作圖。
PKCβI蛋白表達量的表示方法由 Quantity One圖像分析軟件分析得出胞漿,膜相關和膜蛋白成分中,PKCβI在X-膠片上的密度值。然后,計算出各組份PKCβI在 X-膠片上的密度值的總和。以正常對照組的比值作為100%,其余各組用各組份密度值的總和表示 PKCβI蛋白表達量。實驗數據用SPSS for Windows11.5統計軟件進行單因素方差分析(One Way ANOVA),結果以均數 ±標準誤(X±S.E.)表示,差異顯著性水平P<0.05。
1.8.2 免疫組化數據分析
PKCβI染色細胞計數方法 在高倍視野下對各組大鼠肺血管組織內染色陽性的細胞進行計數。每組選取5張切片,每張切片選取8個高倍視野,取平均值。計算出每0.01mm2面積中染色陽性的細胞數。實驗數據用SPSS for Windows 11.5統計軟件進行 T-檢驗(T-test),結果以均數 ± 標準誤(X±S.E.)表示,P<0.05作為差異顯著性水平。
2 結果
2.1 右心室收縮壓(RVSP)和右心室肥厚指數(RVHI)的變化
如圖1A隨著低氧暴露時間的延長,與正常對照組比較,RVSP明顯上升(與第0天比,P<0.05,23.76±0.82mmHg,n=6),并在低氧7d后達到頂峰。如圖1B隨著低氧暴露時間的延長,與正常對照組比較,RV/(LV+S)比明顯增加(與第0天比,P<0.05,100%,n=6)。
2.2 肺血管蘇木精-伊紅(HE)染色結果
在低氧暴露3 d、7 d和21 d后大鼠的肺血管有明顯的病理改變。如圖2所示,和對照組相比(彩插2圖2的A和E),肺動脈高壓大鼠肺血管的遠端(彩插2圖2的 B,C和 D)和近端(彩插2圖2的F)肺血管有明顯的血管重塑,包括中膜肥大和外膜增生。這些結果表明長期暴露于低氧環境中可誘導大鼠形成肺動脈高壓。

圖1 右心室收縮壓和右心室肥厚指數的變化Fig.1 Changs of RVSP and RVHI
2.3 在慢性低氧誘導的肺動脈高壓大鼠肺血管平滑肌細胞及成纖維細胞中PKCβI特異性蛋白表達和膜轉位
圖3 的蛋白免疫印跡結果顯示 PKCβI(79×103)存在于大鼠的肺血管平滑肌細胞及成纖維細胞中。如圖4的A和B所示,和常氧對照組相比,在1-21d,PKCβI蛋白表達為(68.58±2.96%,47.39±7.40%,25.02±2.74%,38.52±2.69%和40.61±5.46%,P<0.05)。如圖5所示,在肺動脈高壓大鼠的肺血管平滑肌細胞及成纖維細胞中PKCβI的膜轉位沒有下降。

圖3 PKCβI和 PKCγ在肺血管的表達Fig.3 Identification of PKCβI and PKCγ in pulmonary vasculars.
2.4 在慢性低氧誘導的肺動脈高壓大鼠肺血管平滑肌細胞及成纖維細胞中PKCβI的蛋白表達水平

圖4 肺血管中PKC βI的表達水平Fig.4 The PKCβI protein levels in pulmonary vasculars.
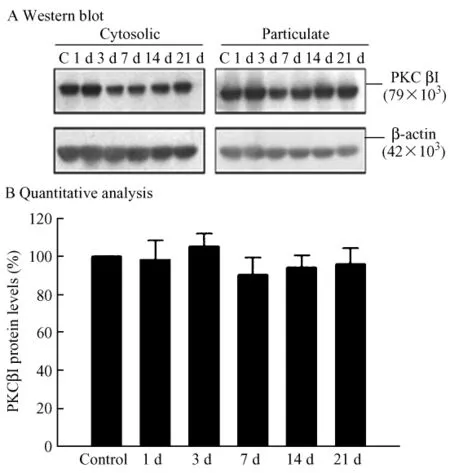
圖5 肺血管中PKCβI的膜轉位結果Fig.5 The results of PKC βI membrane translocation in pulmonary vasculars.
免疫組化的研究發現在慢性低氧14 d后PKCβI蛋白表達是下降的(彩插2圖6B)。
3 討論
肺動脈高壓是最嚴重的具有潛在致命性的慢性肺循環疾病[1]。肺血管收縮和重塑都引起肺動脈高壓形成。本實驗結果表明:隨著低氧暴露時間的延長,與正常對照組比較,低氧各組RVSP和RV/(LV+S)比值均明顯增加,病理結果也顯示肺動脈重塑,這些結果均提示肺動脈高壓形成。肺動脈高壓的發病機理目前還不是很清楚,但是,低氧是導致肺動脈高壓的誘因之一。在低氧條件下,可以導致肺血管收縮和肺血管壓力增加[10]。當低氧性肺動脈血管收縮持續存在時,血管細胞中的促增殖信號傳導通路被激活,從而激活一系列增殖信號通路,導致了肺血管重塑,最終引起慢性低氧性肺動脈高壓[11]。PKC屬于絲/蘇氨酸蛋白激酶家族,是一種重要的信號分子,在慢性低氧性肺動脈高壓中起重要作用[12]。迄今為止,在哺乳動物中至少鑒定出10種PKC亞型,并根據它們的分子結構和對激活劑的敏感性分為3個亞組:經典型PKC(cPKCα、βI、βII和 γ),需要鈣離子和 DAG 來激活;新奇型PKC(nPKCδ、ε、η 和 θ);和非典型性 PKC(aPKCλ/ι和 ζ)[13]。PKCs激活后可以發生移位,即從胞漿轉移到胞膜、細胞骨架結構或細胞核內,稱為膜轉位或核轉位,本實驗中PKC亞型的激活通常以它們從胞漿成分轉位到膜或膜相關成分上來衡量[14]。如膜或膜相關成分增多,說明PKC激活。LiaoDF等用免疫印跡方法發現在大鼠的主動脈血管平滑肌細胞中有 PKCβI的表達[15]。此外,在新生牛肺動脈外膜成纖維細胞和新生小牛肺動脈平滑肌細胞中都曾報道過有 PKCβI的表達[16]。與之相似,在我們的整體動物研究中應用免疫印跡和免疫組化的技術發現在大鼠肺動脈平滑肌細胞和成纖維細胞中均有 PKCβI的表達。
在體內研究中,低氧性肺動脈高壓發生后肺動脈平滑肌細胞和成纖維細胞發生增殖反應[17]。PKC是一種重要的蛋白激酶,可以促進生長因子、激素和抗原等的細胞增殖反應。但是在體內模型中PKCβI是否參與了低氧誘導的肺血管重塑還不太清楚。盡管已有研究者報道低氧條件下經典型PKCβI是被激活的,但是,本研究卻發現 PKCβI蛋白表達量的下調以及膜轉位水平無變化。這些結果和以前在腦缺血和谷氨酸損傷的神經細胞原代培養中的結果是相似的[18]。本實驗結果表明:PKCβI特異蛋白表達的下調可能和肺動脈平滑肌細胞增大的生長能力有關。
在本研究中我們還發現慢性低氧誘導的大鼠肺動脈高壓的發生、發展與肺血管重塑結果不相一致,表明血管收縮也是導致肺動脈壓增高的主要原因。PKC的激活參與了肺臟中肺泡低氧肺血管收縮反應的信號傳導通路[19]。以往研究多認為 PKC的激活可以增強低氧條件下肺血管收縮,其機制可能是通過佛波酯導致PKC激活,從而使肺動脈中不依賴鈣的血管平滑肌組織收縮。PKC通過磷酸化和激活 PKC賦予的肌球蛋白磷酸酶抑制劑(CPI-17)引起鈣離子的敏化,進而抑制肌球蛋白輕鏈磷酸酯酶催化結構域。但是與激活相反,本實驗發現在慢性低氧誘導的大鼠肺動脈高壓中 PKCβI蛋白表達明顯下降。Robertson等推測在持續性低氧誘導的肺動脈高壓中觀察到的鈣敏感化是不依賴于大鼠肺動脈中 PKC的激活的[20],有著自己獨立的激活路徑。這些數據表明根據磷酸化不同的底物蛋白,這些PKC亞型可能有多種不同的功能,如細胞增殖和血管收縮。
總之,本研究系統地描述了慢性持續性常壓低氧誘導的大鼠肺動脈高壓整體動物模型樣本中肺血管平滑肌細胞及成纖維細胞中PKCβI特異的膜轉位和蛋白表達水平的變化情況。本實驗的研究表明PKCβI蛋白表達的下調可能參與了慢性低氧誘導的大鼠肺動脈高壓肺血管重塑的發生和發展過程。
[1]Hoette S,Jardim C,Souza RD.Diagnosis and treatment of pulmonary hypertension an update[J].Bras.Pneumol,2010,36(6):795-811.
[2]Nishizuka Y.Protein kinase C and lipid signaling for sustained cellular responses.[J].FASEB J,1995,9(7):484-496.
[3]Barman SA,Zhu S,White RE.Protein kinase C inhibits BKCa channel activity in pulmonary arterial smooth muscle[J].Am J Physiol Lung Cell Mol Physiol,2004,286(1):L149-L155.
[4]Dempsey EC,Das M,Frid MG,et al.Hypoxic growth of bovine pulmonary artery smooth muscle cells[J].Chest,1998,114:29S.
[5]Deten A,Millar H,Zimmer HG..Catheterization of pulmonary artery in rats with an ultraminiature catheter pressure transducer[J].Am J Physiol Heart Circ Physiol,2003,285(5):H2212-H2217.
[6]Christou H,Morita T,Hsieh CM,et al.Prevention of hypoxiainduced pulmonary hypertension by enhancement of endogenous heme oxygenase-1 in the rat[J].Circ Res,2000,86(12):1224-1229.
[7]Li J,Niu C,Han S,et al.Identification of protein kinase C isoforms involved in cerebral hypoxic preconditioning of mice[J].Brain Res,2005,1060(1-2):62-72.
[8]Wei Y,Wang N,Lu Q,et al.J.Enhanced protein expressions of sortilin and p75NTR in retina of rat following elevated intraocular pressure-induced retinal ischemia[J].Neurosci Lett,2007,429(2-3):169-174.
[9]Ding J,Ding N,Wang N,et al.Determination of conventional protein kinase C isoforms involved in high intraocular pressureinduced retinal ischemic preconditioning of rats[J].Vision Res,2009,49(3):315-321.
[10]Stenmark KR,Mecham RP.Cellular and molecular mechanisms of pulmonary vascular remodeling[J].Annu Rev Physiol,1997,59:89-144.
[11]Jeffery TK,Wanstall JC.Pulmonary vascular remodeling:a target for therapeutic intervention in pulmonary hypertension[J].Pharmacol Ther,2001,92(1):1-20.
[12]Littler CM,Wehling CA,Wick MJ,et al.Divergent contractile and structural responses of the murine PKC-epsilon null pulmonary circulation to chronic hypoxia[J].Am J Physiol Lung Cell Mol Physiol,2005,289(6):L1083-L1093.
[13]Barnett ME,Madgwick DK,Takemoto DJ.Protein kinase C as a stress sensor[J].Cell Signal,2007,19(9):1820-1829.
[14]Kurkinen K,Busto R,Goldsteins G,et al.Isoform-specific membrane translocation of protein kinase C afterischemic preconditioning[J].Neurochem Res,2001,26(10):1139-1144.
[15]Liao DF,Monia B,Dean N,et al.Protein kinase C-zeta mediates angiotensin II activation of ERK1/2 in vascular smooth muscle cells[J].J Biol Chem,1997,272(10):6146-6150.
[16]Das M,Stenmark KR,Ruff LJ,et al.Selected isozymes of PKC contribute to augmented growth of fet al and neonatal bovine PA adventitial fibroblasts[J].Am J Physiol,1997,273(6 Pt 1):L1276-L1284.
[17]Hayashida K,Fujita J,Miyake Y,et al.Bone marrow-derived cells contribute to pulmonary vascular remodeling in hypoxiainduced pulmonary hypertension.[J].Chest,2005,127(5):1793-1798.
[18]Chakravarthy BR,Wang J,Tremblay R,et al.Comparison of the changes in protein kinase C induced by glutamate in primary cortical neurons and by in vivo cerebral ischaemia[J].Cell Signal,1998,10(4):291-295.
[19]Weissmann N,Voswinckel R,Hardebusch T,et al.Evidence for a role of protein kinase C in hypoxic pulmonary vasoconstriction[J].Am J Physiol,1999,276(1 Pt 1):L90-L95.
[20]Robertson TP,Aaronson PI,Ward JP.Hypoxic vasoconstriction and intracellular Ca2+in pulmonary arteries:evidence for PKC-independent Ca2+sensitization[J].Am J Physiol,1995,268(1 Pt 2):H301-H307.
Determination of PKCβI Membrane Translocation and Protein Expression in Pulmonary Artery Smooth Muscle Cells and Fibroblasts of Rats with Chronic Hypoxia-induced Pulmonary Hypertension
CHENG Zhen-ling1,YU Wen-yan1,NIE Xin1,SHI Yi-wei2,DU Yong-cheng1
(1.Department of Respiratory Medicine,People's Hospitalof Shan Xi Medical University,Taiyuan 030001,China;2.Department of Respiratory Medicine,the First Hospital of Shan Xi Medical University,Taiyuan 030001,China)
Objective By observing the influence of PKCβI membrane translocation and protein expression level in pulmonary artery Smooth muscle cells and Fibroblasts of chronic hypoxia-induced rat pulmonary hypertension,discuss the function of PKCβI in process of chronic hypoxia-induced rat pulmonary hypertension preliminary.Methods Chronic atmospheric pressure hypoxic PH model rats were established.Male SD rats were randomLy divided into six groups,and exposed to normoxia control or to normoxia hypoxia for 1d,3d,7d,14d and 21d to induce pulmonary hypertension.Western blot and immunohistochemistry were used to detect the expression of PKCβI membrane translocation and protein expression level in pulmonary artery Smooth muscle cells and Fibroblasts of chronic hypoxia-induced rat pulmonary hypertension.Results(1)RVSP and RV/(LV+S)increased significantly than normal control groups(P <0.05),rats pulmonaryvascular obvious thickening after chronic hypoxia 3d,7d,14d and 21d.(2).PKCβI was expressed in rat pulmonary artery Smooth muscle cells and Fibroblasts,and its protein expressions decreased at 14d after chronic hypoxia than normal control groups(P < 0.05).Conclusions PKCβI protein expression is involved in the development of pulmonary vascular remodeling of chronic hypoxia-induced rat PH.
Protein kinase C βI(PKC βI);Chronic hypoxia;Pulmonary hypertension(PH);Membrane translocation;Protein expression
R332
A
1671-7856(2012)09-0026-05
10.3969.j.issn.1671.7856.2012.009.006
2012-08-25
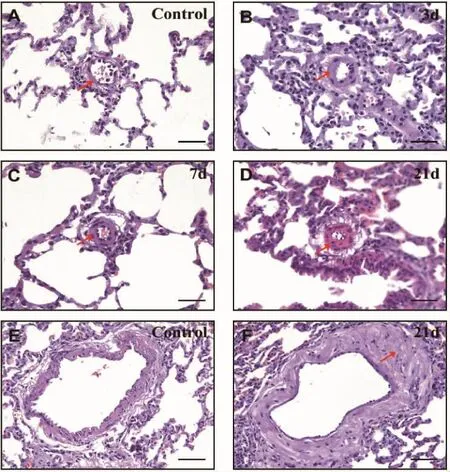
圖2 大鼠HE染色病理學觀察(缺血后2 d)
Fig.2 Histopathological changes of the brain tissue at 2 days post-occlusion (HE staining)
注:A:假手術組-CA1區 B:假手術組-CA3區 C:假手術組-皮層D:模型組-CA1區 E:模型組-CA3 F:模型組-皮層
Note: A: Sham group - CA1; B: Sham group - CA3; C: Sham group - cortex;D: pMCAO group - CA1; E: pMCAO group - CA3; F: pMCAO group - cortex

圖6 肺血管PKC I的蛋白表達水平
Fig.6 The PKC I protein levels in pulmonary vasculars
注:圖中紅箭頭所指為平滑肌細胞層,黑箭頭所指為成纖維細胞層
Note: The red arroW for smooth muscle cells, The black arroW for fibroblasts
程振玲(1986-),碩士生,研究方向:低氧與肺動脈高壓基礎及臨床研究。E-mail:zhenlingch@yahoo.com.cn。
杜永成(1955-),博士生導師。Email:hxkdyc@yahoo.com.cn。

