多胺代謝與植物抗逆性研究進展
宋永駿 刁倩楠 齊紅巖
(沈陽農業大學園藝學院,設施園藝省部共建教育部重點實驗室,遼寧省設施園藝重點實驗室,遼寧沈陽 110866)
多胺(Polyamines,PAs)廣泛存在于生物細胞中,是生物代謝過程中產生的一類具有生物活性的低分子量脂肪族含氮堿,主要包括腐胺(Put)、尸胺(Cad)、亞精胺(Spd)、精胺(Spm),此外還有高亞精胺(Hspd)、高精胺(Hspm)、降亞精胺(Nspd)和降精胺(Nspm)等稀有多胺。多胺主要以 3種形式在植物中存在,分別為游離態、共價結合態以及非共價結合態,其中共價結合態又可分為可溶性共價結合態和不溶性共價結合態兩種形態。20世紀60年代,美國耶魯大學Galston試驗小組開始對多胺進行系統研究,發現多胺具有刺激植物生長和延緩衰老的作用,其作用開始引起人們的重視。隨著多胺研究的不斷深入、技術手段的不斷進步,多胺的生理作用和功能也被進一步發現。
多胺具有一定的陽離子功能,所以它能夠和一些帶負電荷的大分子相結合,如DNA、RNA、蛋白質以及帶負電荷基團的磷脂等,對穩定細胞結構起到一定的作用(Liu et al.,2006;Kusano et al.,2008),并且參與植物多種基本生理過程,如葉片衰老、花器官的形成與發育、果實發育與成熟以及植物對逆境的響應(Groppa & Benavides,2008;Kusano et al.,2008;齊紅巖 等,2012)。多胺作為一種與植物抗逆性有關的物質,能夠緩解植物所受到的傷害。本文就多胺與植物抗逆性關系的研究進展做一概述,旨在為其在農業生產中的應用提供理論依據。
1 植物體中多胺的代謝
1.1 植物體中多胺的合成
植物體中有兩條合成Put的途徑(圖1),Put作為合成過程中最初的一種多胺在特定酶的作用下不斷地添加氨丙基形成Spd和Spm,與此同時,甲硫氨酸脫去羧基也能形成Spd與Spm(Kusano et al.,2007)。
精氨酸脫羧酶(ADC)、鳥氨酸脫羧酶(ODC)和 S-腺苷蛋氨酸脫羧酶(SAMDC)是多胺合成過程中主要的關鍵酶。ADC在植物中廣泛分布,主要定位于細胞質內,對外界刺激、各種脅迫的反應最敏感,在擬南芥中已經發現有兩個ADC編碼基因:ADC1和ADC2(Watson et al.,1997)。ADC1在所有植物組織中均有所表達,而ADC2的表達與一些逆境脅迫有關,如干旱與機械損傷(Soyka & Heyer,1999;Peréz-Amador et al.,2002)。ODC廣泛存在于動物組織細胞,是一種磷酸吡哆醛依賴性酶,脅迫條件下 ODC活性變化較小,一般認為ODC催化的反應在細胞分裂周期和生殖器官分化中起作用。SAMDC是Spd和Spm合成的關鍵酶,在植物體內存在3種類型,分別為Mg2+刺激型、Put刺激型、Mg2+和Put均不敏感型。其至少通過 4個基因SAMDC1、SAMDC2、SAMDC3和SAMDC4編碼(Urano et al.,2003;Ge et al.,2006)。目前已在馬鈴薯、菠菜、長春花等體內克隆了SAMDC基因,并發現該基因表達受鹽脅迫誘導。同樣的,亞精胺合成酶(SPDS)與精胺合成酶(SPMS)在多胺的合成中也起到了一定的作用。SPDS催化Put生成Spd,擬南芥中研究表明,SPDS由兩個基因編碼:spd1和spd2(Watson et al.,1997)。SPMS催化Spd與氨丙基結合生成Spm。SPMS與SPDS存在較高的同源性,系統進化分析的結果顯示,SPMS可能起源于SPDS(Minguet et al.,2008)。
此外,影響鯡精胺向Put轉化的AIH以及CPA是由單基因所控制的。ACL5最初在擬南芥中被報道是合成Spm的酶類(Hanzawa et al.,2000)。然而,最近卻有研究表明ACL5并不是精胺合成酶,而是熱精胺合成酶,它催化Spd生成熱精胺(Knott et al.,2007;Kakehi et al.,2008)。
1.2 植物體中多胺的分解
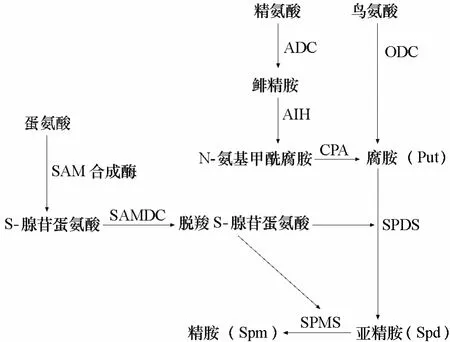
圖1 多胺在植物中主要的合成途徑
多胺的分解代謝(圖2)是通過二胺氧化酶(DAO)和多胺氧化酶(PAO)的氧化作用實現的。DAO是一類含銅酶,催化Put和Cad氧化分解。DAO在雙子葉植物中含量較高,但至今僅在少數幾個物種中發現其編碼基因(Cona et al.,2006)。擬南芥含有12個類DAO編碼基因(Alcázar et al.,2006),但只有ATAO1的功能被確定,其余11個基因序列的功能分析是否與其相似還有待于研究(Moller & Mcpherson,1998)。與DAO不同,PAO以非共價鍵與黃素腺嘌呤二核苷酸(FAD)相連,在單子葉植物中含量較高,PAO是催化生物體內多胺(PAs)氧化的關鍵酶,能夠通過調節細胞內PAs的水平和生成物的濃度,參與植物體對各種逆境脅迫的反應和生長發育過程。植物中的多胺氧化酶按其功能不同可以分為三類,首次獲得的植物PAOs是從玉米細胞質外體導出的ZmPAO,其主要作用為分解Spd和Spm。第二類多胺氧化酶類似于哺乳動物的精胺氧化酶,可以催化 Spm向 Spd轉化(Vujcic et al.,2002)。第三類多胺氧化酶的蛋白質結構域與人類的賴氨酸脫甲基酶1(LSD1)有一定的親緣關系(Shi et al.,2004),在擬南芥上已經發現4種與LSD1相關的基因,有一些已經被證明參與抑制成花負調控子FLC的活性。
2 多胺與逆境脅迫之間的關系
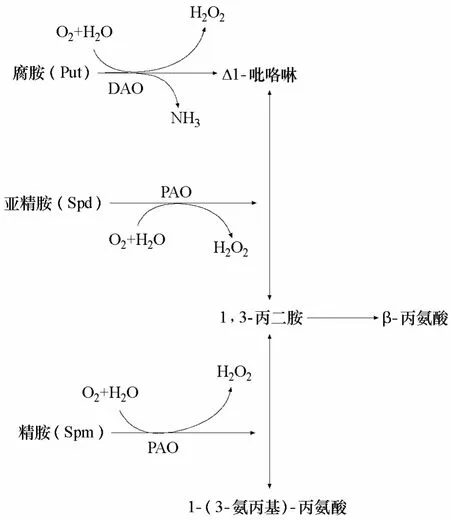
圖2 多胺在植物中主要的分解途徑
2.1 逆境脅迫下的多胺代謝
在多胺的早期研究階段,有研究表明:K+缺乏會導致植物體內 Put含量增加(Richards &Coleman,1952),從這以后越來越多的學者投入到多胺與植物抗逆性關系的研究中來。現在許多研究均表明多胺在低溫、高溫、鹽害、干旱、低氧脅迫等逆境下均會有不同程度的積累(Alcázar et al.,2006;Groppa & Benavides,2008)。但不同植物受到不同逆境脅迫時其Put、Spd和Spm的變化規律不盡相同。逆境脅迫下,植物體內的多胺含量也有可能降低。研究表明番茄在受到鹽脅迫時其體內多胺含量隨著脅迫時間的延長逐漸下降(Santa-Cruz et al.,1997)。郝敬虹等(2009)研究發現低夜溫下,甜瓜果實中 Put、Spd以及 Spm含量顯著下降。在鹽脅迫下,Put的合成主要通過ADC途徑,ADC活性會有所升高(Flores,1991)。編碼ADC的ADC1與ADC2對于逆境的響應是不同的,ADC1主要被冷害誘導(Armengaud et al.,2004),而ADC2的表達量在許多逆境,諸如干旱、鹽害、機械損傷中均較高(Peréz-Amador et al.,2002;Urano et al.,2003;Hummel et al.,2004 ;Alcázar et al.,2006)。ODC 途徑作為 Put合成的另一種途徑,在各種逆境下其活性的變化不盡相同(Aziz et al.,1997,1998;Lee et al.,1997),有研究顯示,控制ODC合成的相關基因在受到生物脅迫后其轉錄水平會有所上升(Yoo et al.,2004),這說明ODC基因有可能是在翻譯以及修飾水平上控制ODC的合成。SAMDC可以起到調節植物體內多胺合成的作用(Hanfrey et al.,2005),在低溫脅迫中、脅迫后的愈傷組織中,SAMDC基因的表達量均有所上升,并且與膜受傷害程度的表現一致,這說明在脅迫中愈傷組織通過提高SAMDC相關基因的表達量來提高體內多胺的含量以適應逆境環境(劉穎 等,2011)。CPA、AIH編碼基因以及ACL5基因在任何的逆境下都沒有發現其表達量變化(Alcázar et al.,2006)。
DAO與PAO作為兩種主要的多胺分解酶,其與抗逆性關系的研究也被廣泛地報道(高洪波和郭世榮,2005;周國賢 等,2006;徐春明 等,2010),有研究表明DAO與PAO是通過分解多胺產生H2O2來影響植物的抗逆性,但也有觀點認為通過多胺途徑產生的H2O2含量不足以對植物的抗逆性產生影響(Moschou et al.,2008)。
2.2 外源多胺及多胺抑制劑對植物抗逆性的影響
噴施外源多胺以及多胺抑制劑是研究多胺與植物抗逆性關系的一種重要手段。大量研究表明,外源多胺主要是通過參與清除活性氧,維持細胞膜的完整性以及保持離子平衡來減少逆境對植物所造成的傷害(Besford et al.,1993;Ha et al.,1998;Armengaud et al.,2004),然而由于植物種類不同,它們對于外源多胺的吸收、運輸以及利用均存在一定的差異,所以不同種類的多胺對提高植物抗逆性的作用也有所不同(Gill & Tuteja,2010)。例如:外源Put和Spd對減輕鹽敏感型水稻所受的脅迫傷害起一定作用,然而施用外源Spm卻沒有任何明顯效果(Alexis &Stanley,2007)。
與此同時,各種多胺抑制劑如二氟甲基精氨酸(DFMA)、二氟甲基鳥氨酸(DFMO)、甲基乙二醛(MGBG)能夠影響某種多胺的合成途徑,其中DFMA能夠抑制ADC的活性,DFMO抑制ODC的活性,MGBG抑制SAMDC的活性,DFMA和DFMO所造成的影響都能夠通過施加一定量的外源多胺逆轉(He et al.,2002;Navakoudis et al.,2003),而MGBG卻不能。利用多胺抑制劑能夠更加具體地描述特定多胺與植物抗逆性之間的關系。通過外源施用DFMA和DFMO研究得出,油菜在正常生長條件下只有ADC合成途徑是其Put合成的主要途徑,而在受到滲透脅迫時,ADC與ODC均參與其合成(Aziz et al.,1998)。Lee等(1997)研究表明,DFMA能夠降低耐低溫型水稻的耐冷性,增加其電解質的滲透率。
2.3 突變體與轉基因在研究多胺與植物抗逆性關系上的應用
研究多胺在逆境下的生理作用,運用突變體以及轉基因植物是一個不可或缺的手段。Watson等(1998)研究發現擬南芥EMS突變體缺少ADC基因(spe-1與spe-2)。這類突變體的多胺含量與野生型相比有所減少,其耐鹽性下降(Kasinathan & Wingler,2004)。acl5/spms擬南芥雙突變體不合成Spm,對鹽與干旱脅迫更加敏感,施用外源Spm可以緩解這一現象(Kusano et al.,2007)。
利用轉基因技術能夠調控與多胺有關的生理代謝途徑。將燕麥的ADC基因轉入到茄子中,發現轉基因植株表現出了對逆境更強的耐受性(Prabhavathi & Rajam,2007)。轉基因的擬南芥中,ADC1與ADC2過表達可以誘導高水平Put積累,增強抗逆性;ADC1基因過表達的擬南芥中Put含量明顯升高,提高其耐冷性(Altabella et al.,2009)。同樣,ADC2基因過表達的擬南芥中Put含量升高,提高其抗旱性(Alcázar et al.,2006)。
3 逆境脅迫下多胺代謝對其他生理活動的影響
3.1 多胺作為滲透調節物質
逆境脅迫下,可溶性物質的積累被看做是植物對逆境的一種積極的響應,它們能夠維持細胞膨壓以及基本結構(McNeil et al.,1999)。雖然多胺作為滲透調節物質的觀點尚存在爭議,但是多胺在逆境脅迫下確實能夠穩定生物大分子以及防止細胞膜變性(Liu et al.,2007)。這可能與以下幾個方面有關,首先,多胺的代謝產物,如β-丙氨酸能進一步轉化為甜菜堿,從而緩解逆境對植物所造成的傷害。其次,多胺代謝與脯氨酸的積累密切相關(Aziz et al.,1998),但具體的途徑仍不清楚,不過 Put與脯氨酸的合成都需要鳥氨酸,這有可能是二者之間相互作用的一個途徑(Mohapatra et al.,2010)。
3.2 多胺作為植物響應逆境脅迫的信號分子
ABA能夠參與調控植物對逆境脅迫如干旱、高鹽、低溫等產生的應答。有研究表明ABA能夠誘導ADC2、SPDS1和SPMS基因的表達(Peréz-Amador et al.,2002;Urano et al.,2003)。為了進一步研究逆境、ABA與多胺代謝三者之間的關系,有學者利用遭受水分脅迫條件下的擬南芥,針對 ABA缺失型(aba2-3)以及 ABA不敏感型(abi1-1)這兩個突變體的ADC2、SPDS1以及SPMS基因的表達情況進行分析,發現這3個基因在突變體中的表達與野生型相比明顯降低,這表明水分脅迫有可能首先提高了ABA的含量,隨后ABA又誘導了這3個與多胺合成相關基因的表達(Alcázar et al.,2006)。多胺的分解代謝經常會產生H2O2,H2O2作為一種信號分子能夠激活植物自身的防御系統,提高植物的抗逆性(Neill et al.,2002)。另一方面,Spd以及Spm可以通過某一未知酶或者多胺分解酶產生一氧化氮(NO)(Rinukshi et al.,2011),NO作為一種重要的信號分子,可以調節植物的多種生理功能和抵御逆境脅迫(Neill et al.,2003;Shapiro,2005)。
ABA、H2O2以及NO這3種與多胺代謝密切相關的信號分子,在逆境脅迫下往往相互關聯,發揮著特定的生理作用。有研究表明,H2O2和NO是ABA誘導氣孔關閉所需的基本信號,它們共同發揮作用調節氣孔關閉(Neill et al.,2008)。
3.3 逆境下多胺對離子通道的影響
最近已經發現多胺能夠影響植物的離子通道(Kusano et al.,2007),多胺是帶有正電荷的分子,能夠與離子通道相互作用,因此可以作為離子通道的阻滯劑(Brüggemann et al.,1999)。多胺可能通過影響離子通道蛋白(蛋白激酶或磷酸酶)的活性或者細胞膜組分來調節離子通道,但這一理論并不適用于所有作物,對豌豆肉細胞的研究表明,多胺調節離子通道是通過細胞質途徑來實現的(Shabala et al.,2007)。
多胺可以通過調節離子通道來緩解脅迫對植物的傷害。例如:高鹽脅迫能夠誘導大麥幼苗多胺的合成,從而維持大麥幼苗K+/Na+在體內的平衡,提高其耐鹽性(Brüggemann et al.,1999)。
細胞內 Ca2+作為第二信使能夠通過信號途徑來增強植物的抗逆性。鈣離子通道作為離子通道的一種,同樣能夠被多胺所調控。細胞內 Ca2+的水平可能與質外體或者細胞內磷酸酯酶的活性有關(Mahajan &Tuteja,2005)。Wilson等(2009)報道,擬南芥SAL1酶突變體(磷酸酯酶過表達)alx8表現出更強的抗旱性,與此同時突變體alx8也表現出了極高的 Put水平,ADC2的表達量也有所增加。由此可以推斷Put可能改變了鈣離子通道,從而提高了植物的抗旱性。
4 展望
最近幾十年的研究表明,多胺代謝過程與植物對逆境的響應機制密切相關。但對于不同的植物以及所處的逆境來說,不同種類多胺的變化有所區別,這說明其作用于植物抗性機制的過程非常復雜。再者,多胺合成代謝中主要的3個關鍵酶ADC、ODC和SAMDC已在許多植物中得到了純化和鑒定,一些基因也從多種植物中克隆,并采用轉基因技術獲得了一些認為多胺可提高植物抗性的研究結果,但多胺在植物中的載體是什么,植物對多胺的信號感受和傳遞途徑是怎樣的,多胺通過怎樣的信號轉導通路作用于植物的抗性基因,作用于哪些抗性基因,進而在轉錄和翻譯水平上調控這些基因的表達,控制脅迫蛋白的水平,都還不清楚。因此,需要通過遺傳與分子生物學的方法來進一步了解多胺在此過程中的作用,這方面的工作今后應該受到更多的重視。
高洪波,郭世榮.2005.低氧脅迫對無土栽培網紋甜瓜幼苗多胺含量的影響.園藝學報,32(1):121-123.
郝敬虹,杜哲,王延迪,李天來.2009.夜間溫度對薄皮甜瓜果實膨大及多胺含量的影響.園藝學報,36(3):421-426.
劉穎,王瑩,龍萃.2011.植物多胺代謝途徑研究進展.生物工程學報,27(2):147?155.
齊紅巖,黃鶴,張多嬌.2012.外源多胺對薄皮甜瓜花芽分化及花發育的影響.中國蔬菜,(10):42-47.
徐春明,陳文浩,趙兵.2010.外源多胺對鋁脅迫下番紅花的生理響應.中國農學通報,26(11):148-151.
周國賢,郭世榮,王素平.2006.外源多胺對低氧脅迫下黃瓜幼苗光合特性和膜脂過氧化的影響.植物學通報,23(4):341-347.
Alcázar R,Cuevas J C,Patron M,Altabella T.2006.Abscisic acid modulates polyamine metabolism under water stress inArabidopsis thaliana.Physiol Plant,128:448-455.
Alexis N,Stanley L.2007.Long term exogenous putrescine application improves grain yield of a salt-sensitive rice cultivar exposed to NaCl.Plant Soil,291:225-238.
Altabella T,Tiburcio A F,Ferrando A.2009.Plant with resistance to low temperature and method of production thereof:Spanish.WO2010/004070.2010-03-09.
Armengaud P,Breitling R,Amtmann A.2004.The potassium-dependent transcriptome ofArabidopsisreveals a prominent role of jasmonic acid in nutrient signaling.Plant Physiol,136:2556-2576.
Aziz A,Martin-Tanguy J,Larher F.1997.Plasticity of polyamine metabolism associated with high osmotic stress in rape leaf discs and with ethylene treatment.Plant Growth Regul,21:153-163.
Aziz A,Martin-Tanguy J,Larher F.1998.Stress-induced changes in polyamine and tyramine levels can regulate proline accumulation in tomato leaf discs treated with sodium chloride.Physiol Plant,104:195-202.
Besford R T,Richardson C M,Campos J L,Tiburcio A F.1993.Effect of polyamines on stabilization of molecular complexes in thylakoid membranes of osmotically stressed oat leaves.Planta,189:201-206.
Brüggemann L,Pottosin I,Sch?nknecht G.1999.Selectivity of the fast activating vacuolar cation channel.Exp Bot,50:873-876.
Cona A,Rea G,Angelini R,Federico R.2006.Functions of amine oxidases in plant development and defence.Trends Plant Sci,11(2):80-88.
Flores H E.1991.Changes in polyamine metabolism in response to abiotic stress//Slocum R,Flores H E.The biochemistry and physiology of polyamines in plants.Boca Raton,FL:CRC Press:214-225.
Ge C,Cui X,Wang Y,Hu Y,Fu Z.2006.BUD2,encoding anS-adenosylmethionine decarboxylase,is required forArabidopsisgrowth and development.Cell Res,16:446-456.
Gill S,Tuteja N.2010.Polyamines and abiotic stress tolerance in plants.Plant Signal Behav,5(1):26-33.
Groppa M D,Benavides M P.2008.Polyamines and abiotic stress:recent advances.Amino Acids,34:35-45.
Hanfrey C,Elliott K A,Franceschetti M,Mayer M,Michael A.2005.A dual upstream open reading frame-based autoregulatory circuit controlling polyamine-responsive translation.J Biol Chem,280(47):39229?39237.
Ha H C,Sirisoma N S,Kuppusamy P,Zweier J L.1998.The natural polyamine spermine functions directly as a free radical scavenger.Proc Natl Acad Sci USA,95:11140-11145.
Hanzawa Y,Takahashi T,Michael A J,Burtin D,Long D,Pineiro M,Coupland G,Komeda Y.2000.ACAULIS5,anArabidopsisgene required for stem elongation,encodes a spermine synthase.EMBO J,19:4248-4256.
He L,Nada K,Kasukabe Y,Tachibana S.2002.Enhanced susceptibility of photosynthesis to low temperature photohibition due to interruption of chill-induced increase ofS-adenosylmethionine decarboxylase activity in leaves of spinach(Spinacia oleraceaL).Plant Cell Physiol,43:196-206.
Hummel I,Gouesbet G,El Amrani A,Couee I.2004.Characterization of the two arginine decarboxylase(polyamine biosynthesis)paralogues of the endemic suban tarctic cruciferous speciesPringlea antiscorbuticaand analysis of their differential expression during development and response to environmental stress.Gene,342:199-209.
Kakehi J I,Kuwashiro Y,Niitsu M,Takahashi T.2008.Thermospermine is required for stem elongation inArabidopsis thaliana.Plant Cell Physiol,49:1342-1349.
Kasinathan V,Wingler A.2004.Effect of reduced arginine decarboxylase activity on salt tolerance and on polyamine formation during salt stress inArabidopsis thaliana.Plant Physiol,121:101-107.
Knott J M,Romer P,Sumper M.2007.Putative spermine synthases fromThalassiosira pseudonanaandArabidopsis thalianasynthesize thermos permine rather than spermine.FEBS Lett,581:3081-3086.
Kusano T,Yamaguchi K,Berberich T,Takahashi Y.2007.Advances in polyamine research.J Plant Res,120:345-350.
Kusano T,Berberich T,Tateda C,Takahashi Y.2008.Polyamines:essential factors for growth and survival.Planta,228:367-381.
Lee T M,Lur H S,Chu C.1997.Role of abscisic acid in chilling tolerance of rice(Oryza sativaL.)seedlings:Ⅱ.Modulation of free polyamine levels.Plant Sci,126:1-10.
Liu J H,Nada K,Honda C,Kitashiba H,Wen X P,Pang X M,Moriguchi T.2006.Polyamine biosynthesis of apple callus under salt stress:importance of arginine decarboxylase pathway in stress response.J Exp Bot,57:2589-2599.
Liu J H,Kitashiba H,Wang J,Ban Y.2007.Polyamines and their ability to provide environmental stress tolerance to plants.Plant Biotechnol,24:117-126.
Mahajan S,Tuteja N.2005.Cold,salinity and drought stresses:an overview.Arch Biochem Biophys,444:139-158.
McNeil S D,Nuccio M L,Hanson A D.1999.Betaines and related osmoprotectants.Targets for metabolic engineering of stress resistance.Plant Physiol,120:945-949.
Minguet E G,Vera-Sirera F,Marina A,Blázquez M A.2008.Evolutionary diversification in polyamine biosynthesis.Mol Biol Evol,25(10):2119-2128.
Mohapatra S,Minocha R,Long S,Minocha S.2010.Transgenic manipulation of a single polyamine in poplar cells affects the accumulation of all amino acids.Amino Acids,38:1117-1129.
Moller S G,McPherson M J.1998.Developmental expression and biochemical analysis of theArabidopsis ATAO1gene encoding an H2O2-generating diamine oxidase.Plant J,13:781-791.
Moschou P N,Delis I D,Paschalidis K A.2008.Transgenic tobacco plants overexpressing polyamine oxidase are not able to cope with oxidative burst generated by abiotic factors.Physiol Plant,133:140-156.
Navakoudis E,Lütz C,Langebartels C,Lütz- meindl U,Kotzabasis K.2003.Ozone impact on the photosynthetic apparatus and the protective role of polyamines.Biochem Biophys Acta,1621:160-169.
Neill S,Desikan R,Hancock J.2002.Hydrogen peroxide signaling.Curr Opin Plant Biol,5:388-395.
Neill S J,Desikan R J,Hancock T.2003.Nitric oxide signalling in plants.New Phytol,159:11-35.
Neill S,Barros R,Bright J,Morris P,Ribeiro D.2008.Nitric oxide,stomatal closure,and abiotic stress.Exp Bot,59:165-176.
Peréz-Amador M A,Leon J,Green P J,Carbonell J.2002.Induction of the arginine decarboxylaseADC2gene provides evidence for the involvement of polyamines in the wound response inArabidopsis.Plant Physiol,130:1454-1463.
Prabhavathi V R,Rajam M V.2007.Polyamine accumulation in transgenic eggplant enhances tolerance to multiple abiotic stresses and fungal resistance.Plant Biotechnol,24:273-282.
Richards F J,Coleman R G.1952.Occurrence of putrescine in potassium-deficient barley.Nature,170:460.
Rinukshi W,Corina V,Tahmina B.2011.Copper amine oxidase1(CuAO1)ofArabidopsis thalianacontributes to abscisic acid- and polyamine induced nitric oxide biosynthesis and abscisic acid signal transduction.Mol Plant,4(4):663-678.
Santa-Cruz A,Esta? M T,Rus A,Acosta M.1997.Effects of NaCl and mannitol iso-osmotic stresses on the free polyamine levels in leaf discs of tomato species differing in salt tolerance.Plant Physiol,151:754-758.
Shapiro A D.2005.Nitric oxide signaling in plants.Vitamins Hormones,72:339-398.
Shabala S,Cuin T A,PottosinⅠ.2007.Polyamines prevent NaCl-induced K+eZux from pea mesophyll by blocking non-selective cation channels.FEBS Lett,581:1993-1999.
Shi Y J,Lan F,Matson C,Whetstine J R.2004.Histone demethylation mediated by the nuclear amine oxidase homolog LSD1.Cell,119:941-953.
Soyka S,Heyer A G.1999.Arabidopsis knockout mutation ofADC2gene reveals inducibility by osmotic stress.FEBS Lett,458:219-223.
Urano K,Yoshiba Y,Nanjo T,Seki M,Igarashi Y.2003.Characterization ofArabidopsisgenes involved in biosynthesis of polyamines in abiotic stress responses and developmental stages.Plant Cell Environ,26:1917-1926.
Vujcic S,Diegelmann P,Bacchi C J,Kramer D L,Porter C W.2002.Identification and characterization of a novel Xavin-containing spermine oxidase of mammalian cell origin.Biochem J,367:665-675.
Watson M B,Yu W,Galloway G,Malmberg R L.1997.Isolation and characterization of a second arginine decarboxylase cDNA fromArabidopsis.Plant Physiol,114:1569.
Watson M B,Emory K K,Piatak R M,Malmberg R L.1998.Arginine decarboxylase(polyaminesynthesis)mutants ofArabidopsis thalianaexhibit altered root growth.Plant J,13:231-239.
Wilson P B,Estavillo G M,Field K J,Woo N S,Smith S.2009.The nucleotidase/phosphatase SAL1 is a negative regulator of drought tolerance inArabidopsis.Plant J,58:299-317.
Yoo T H,Park C J,Ham B K,Park C,Kim K.2004.Ornithine decarboxylase gene(CaODC1)is specifically induced during TMV mediated but salicylate-independent resistant response in hot pepper.Plant Cell Physiol,45(10):1537?1542.

