高效液相色譜法同時測定解風酒中阿魏酸、原兒茶酸和桂皮醛
王 寧
(湖南省懷化市食品藥品檢驗所,湖南懷化418000)
解風酒是由當歸、狗脊、桂枝、獨活等多味中藥制成的復方制劑。處方源于經驗方,具有祛風除濕,舒經通絡止痛的作用。用于風濕性關節炎及類風濕性關節炎。其現行質量標準只對制劑中活性成分當歸、狗脊、桂枝進行薄層色譜鑒別,無相關的定量測定標準,為了更有效控制本品內在質量,采用高效液相色譜法對方中的阿魏酸、原兒茶酸及桂皮醛進行定量測定。
1 儀器與試藥
島津高效液相色譜儀,包括LC-20AT輸液泵,SPD-M20Avp二極管陣列檢測器,LCsolution工作站;AUW220D十萬分之一電子天平(日本島津公司),CBL9960A超聲波清洗器(上海科導超聲儀有限公司)。
阿魏酸(批號:110773-200612)、原兒茶酸(批號:110810-200506)、桂 皮 醛 (批 號:110710-200513)對照品(均由中國藥品生物制品檢定所提供);解風酒(湖南懷化市中醫院制劑,批號為100322、100902、101003);甲醇、乙腈、冰醋酸均為色譜純;水為超純水;其它試劑均為分析純。
2 方法和結果
2.1 色譜條件 kromasil C18色譜柱(250 mm×4.6 mm,5 μm);流動相 A乙腈-B 0.1%冰醋酸溶液,梯度洗脫(0~35 min,75%B ~55%B);體積流量1.0 mL/min;柱溫30℃;檢測波長260 nm;進樣量10 μL。按阿魏酸峰計算,理論板數不低于4000;按原兒茶酸、桂皮醛計算,理論板數不低于5000。
2.2 對照品溶液制備 精密稱定經減壓干燥18 h的阿魏酸 12.13 mg,原兒茶酸 12.51 mg,桂皮酸對照品5.24 mg,置100 mL量瓶中,用甲醇定容至刻度,作為混合對照品溶液,避光備用。
2.3 供試品溶液的制備 精密量取解風酒20 mL,置50 mL量瓶中加70%甲醇適量溶解,超聲處理(功率250 W,頻率40 kHz)25 min,再加70%甲醇至刻度,搖勻,過濾,取續濾液即得。
2.4 陰性供試品溶液的制備 按處方比例稱取缺當歸、狗脊及桂枝以外的其余藥材,按制備工藝制成陰性制劑,再按2.3項下的方法制備陰性供試品溶液。
2.5 方法學考察
2.5.1 專屬性試驗 分別精密吸取陰性供試品溶液、混合對照品溶液、供試品溶液各10 μL注入液相色譜儀,依法測定。阿魏酸、原兒茶酸及桂皮醛的保留時間分別約為 12.8,21.2,27.6 min,與混合對照品溶液的色譜保留時間一致;陰性供試品溶液在該色譜條件下對測定無干擾。見圖1。
2.5.2 線性關系考察 精密吸取上述混合對照品溶液 2、4、6、8、10、20 μL 分別注入液相色譜儀,測定峰面積,以進樣量(μg)為橫坐標,峰面積為縱坐標,繪制標準曲線,得阿魏酸、原兒茶酸、桂皮醛的回歸方程分別為 A=2.33×106C-3.21×104(r=0.9999),A=2.42 × 106C - 1.39 × 104(r=0.9999),A=1.47 × 106C - 2.67 × 103(r=0.9999)。結果表明阿魏酸、原兒茶酸、桂皮醛分別在 0.02426 ~ 0.2426 μg、0.02502 ~ 0.2502 μg、0.01048 ~0.1048 μg 范圍內,進樣量與峰面積呈良好的線性關系。
2.5.3 精密度試驗 精密吸取同一混合對照品溶液,按2.1項下的方法連續進樣6次,分別測定阿魏酸、原兒茶酸、桂皮醛的峰面積,峰面積RSD分別為 0.48%、0.99% 、0.93%。
2.5.4 重復性試驗 取同一批號解風酒(批號:100322)6份 ,按2.3項下方法制備供試品溶液,依法測定,計算,結果阿魏酸、原兒茶酸、桂皮醛的RSD 分別為 1.01%、0.69%、0.98%。
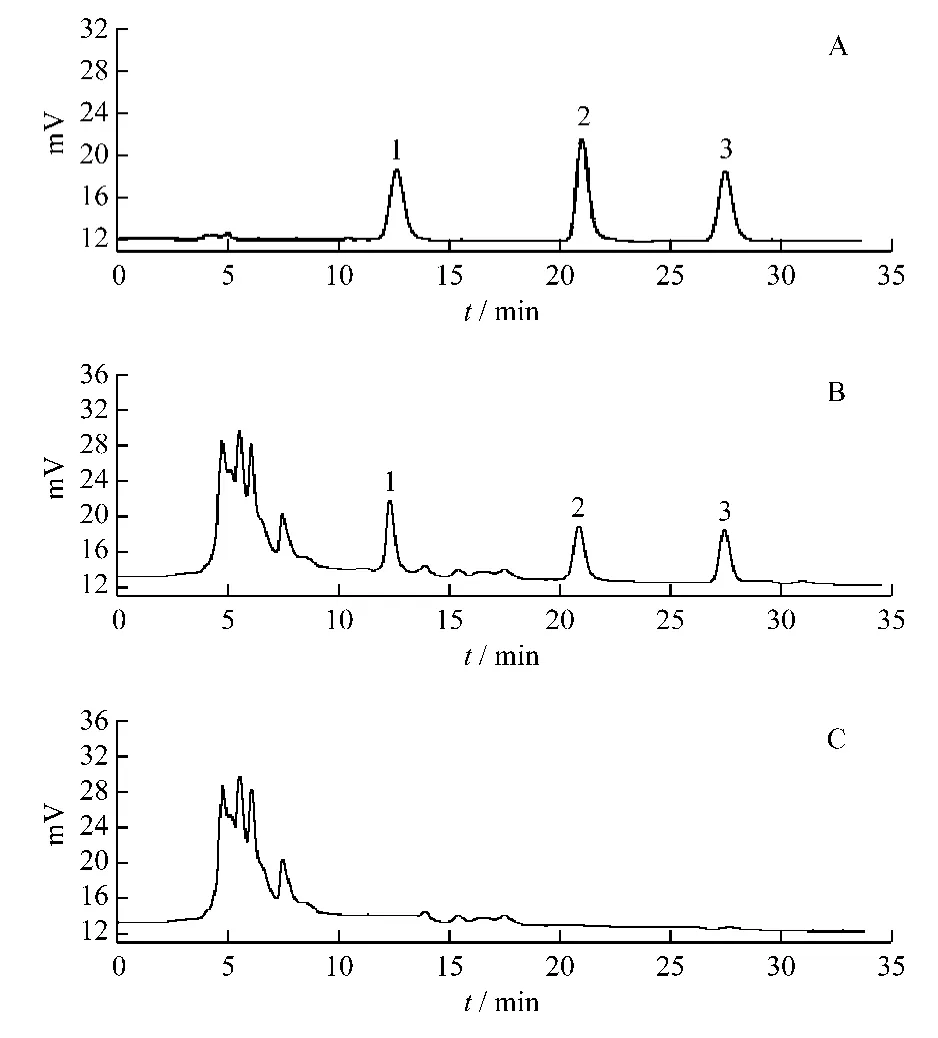
圖1 解風酒HPLC色譜圖Fig.1 HPLC chromatograms of Jiefeng Wine
2.5.5 穩定性考察 吸取供試品 (批號:100322),按2.3項下的制備條件,于室溫放置0、4、8、12、24 h后按2.1項下的色譜條件進行,分別測定阿魏酸、原兒茶酸、桂皮醛的峰面積,RSD分別為0.74%、0.80%、0.65%,表明供試品溶液在 24 h 內基本穩定。
2.5.6 加樣回收率試驗 精密吸取同一批號樣品(批號 100322,含阿魏酸 2.55 mg/瓶;原兒茶酸4.12 mg/瓶;桂皮醛 1.27 mg/瓶;每瓶 500 mL)10 mL,共9份,分別置50 mL量瓶中,分別精密加入混合對照品溶液(阿魏酸0.01213 mg/mL、原兒茶酸0.01251 mg/mL 和桂皮醛 0.00524 mg/mL)5.0,6.0和7.0 mL,按2.3項下的方法制備供試品溶液,并按2.1項下的色譜條件,依法測定,計算平均回收率,結果見表1。
2.5.7 樣品測定 取3批樣品,按2.2和2.3項下的方法分別制備對照品溶液和供試品溶液,依次對3批次樣品(批號:100322,100902,101003)進行測定,結果見表2。
3 討論
3.1 檢測波長的選擇 對阿魏酸、原兒茶酸及桂皮醛進行紫外全波段掃描,三者均在260 nm波長處有較大的紫外吸收,故采取260 nm為檢測波長。

表1 加樣回收率結果Tab.1 The results of Recovery test
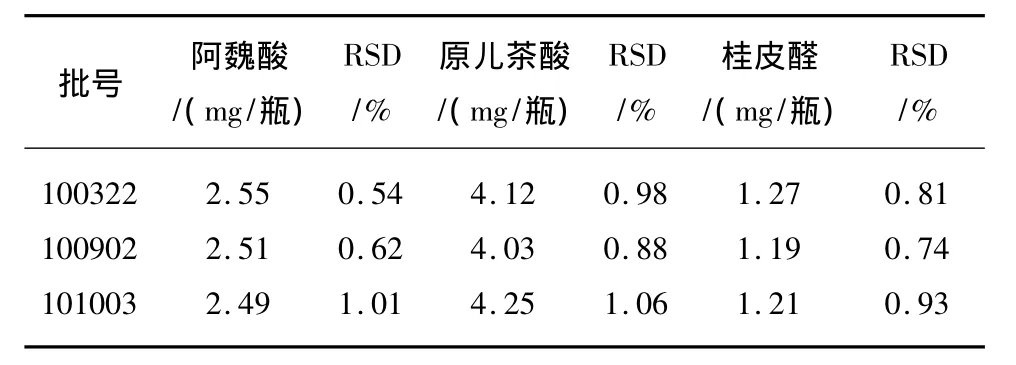
表2 解風酒中阿魏酸、原兒茶酸、桂皮醛測定結果(n=3)Tab.2 Test results of samples(n=3)
3.2 提取溶劑與提取時間的選擇 本實驗分別采用50%甲醇、70%甲醇、甲醇作為提取溶劑,結果發現70%甲醇提取的樣品含有量較其他溶劑高,且雜質影響較小;同時還考察了 15、25、35、45 min不同提取時間對樣品的影響,結果25 min時提取最完全,且所測成分穩定。
3.3 柱溫的設定 本方法采用的是梯度洗脫,在測定中不設柱溫,色譜峰基線漂移較嚴重,樣品峰拖尾明顯,設定柱溫后,可減少拖尾,基線漂移得到改善,峰形對稱,但柱溫設定不易過高,過高峰形變差,故柱溫設定為30℃為佳。
3.4 流動相及洗脫方式的選擇 參閱相關文獻[1-11],分別使用了甲醇-0.1%冰醋酸溶液、乙腈-0.1%冰醋酸溶液、乙腈-0.1%磷酸溶液等不同類型、比例的流動相進行實驗,選用乙腈-0.1%冰醋酸溶液且進行二元梯度洗脫,結果表明,此洗脫相能更好地分離阿魏酸、原兒茶酸與桂皮醛峰,各主峰之間的分離度均大于1.5,且陰性樣品對測定無干擾。
3.5 該品種為臨床常用制劑,為完善其質量標準,用本法同時測定解風酒中阿魏酸、原兒茶酸和桂皮醛,方法簡便、準確,能夠有效控制解風酒的內在質量,為臨床用藥提供安全保障。
[1]國家藥典委員會.中華人民共和國藥典:2010年版一部[S].北京:中國醫藥科技出版社,2010:124,209,259.
[2]袁麗霞,王 紅.HPLC法測定當歸苦參丸中阿魏酸的含量[J].中國藥事,2008,22(1):61.
[3]卞 凌.HPLC法測定養血化瘀合劑中阿魏酸的含量[J].黑龍江中醫藥,2009(5):49-50.
[4]魯健武,曾俊芬,宋金春.HPLC法同時測定復方川芎膠囊中阿魏酸和川芎嗪的含量[J].中國藥師,2008,11(7):814-816.
[5]劉忠民,郭利民.反相高效液相色譜法測定強肝糖漿中阿魏酸含量[J].中國藥業,2006,15(4):18.
[6]張 雪,褚文靜,劉偉娜,等.高效液相色譜-二極管陣列檢測法測定冠心寧注射液中丹參素、原兒茶酸、原兒茶醛、阿魏酸、迷迭香酸和丹酚酸 B[J].中草藥,2010,35(2):1425-1429.
[7]楊 濱,屈巧玲,王謙鵬,等.急支糖漿中原兒茶酸等4種成份的含量測定[J].中國中藥雜志,2007,12(9):565-569.
[8]王治平,楊 柯,孟祥平,等.RP-HPLC法測定滇桂艾納香中原兒茶酸與原兒茶醛含量[J].中藥材,2005,28(5):1245-1248.
[9]張淑芳,裴妙榮,裴香萍.反相高效液相色譜法測定炎立消膠囊中原兒茶酸、原兒茶醛和酪酸的含量[J].中國實驗方劑學雜志,2008,14(6):457-458.
[10]李麗嬌,張元桐,陳曉霞.HPLC法測定人參養榮丸中桂皮醛含量[J].遼寧中醫藥大學學報,2009,11(6):230-231.
[11]成差群,魏燕華,譚秀芬,等.HPLC法測定肉桂配方顆粒中的桂皮醛和桂皮酸[J].華西藥學雜志,2009,23(6):673-674.

