三種ED模型小鼠海綿體組織Cx43蛋白表達變化
王 曉,楊學成,陳 濤,王永華,曹延煒,牛海濤,邵世修
(青島大學醫學院附屬醫院,山東青島266003)
近年來,隨我國糖尿病(DM)發病率明顯提高,DM性陰莖勃起功能障礙(ED)日益成為我國ED發病的主要原因[1]。糖尿病性ED通常被認為主要以血管因素和神經因素為主,連接蛋白(Cx)43基因表達則被認為與陰莖海綿體平滑肌功能密切相關[2]。2008年10月,我們檢測了三種ED模型小鼠的勃起功能和海綿體中的Cx43蛋白表達變化,旨在進一步探討ED發生機制。
1 材料與方法
1.1 材料 2月齡清潔級Wistar大鼠125只,體質量200~250 g,經與生育期雌性大鼠交配證實具有正常性功能;Cx43多克隆抗體、SABC試劑盒和3,3二氨基聯苯胺(DAB)試劑盒(武漢博士德生物工程有限公司),Cx43多克隆抗體工作液濃度1∶100,鏈脲霉素(STZ)和阿樸嗎啡(美國Sigma公司)。
1.2 動物模型建立 將125只Wistar大鼠隨機分為DM因素組35只、血管因素組31只、神經因素組28只及對照組31只,其中前三組分別按如下方式建模:①DM因素組:DM組腹腔注射STZ 55 mg/kg, 1次/d,連續4 d。血糖≥16.67 mmlol/L為造模成功,未達血糖標準者淘汰。②血管因素組:于髂總動脈分叉處向左找到左髂總動脈,向下可見膀胱上動脈起自髂總動脈,于其深面找到左髂內動脈,游離血管周圍組織、筋膜,用6-0絲線于髂內動脈起始端結扎左髂內動脈,同法結扎右側髂內動脈。③神經因素組:在10倍外科顯微鏡下仔細游離前列腺兩側葉后方,暴露出盆腔星狀神經節,沿盆腔星狀神經節向周圍仔細分離、識別出盆神經、腹下神經(輸入支)及沿尿道側面走行的最大輸出支——海綿體神經,并予以切斷。
1.3 勃起功能試驗 各組均于制模后3周進行阿樸嗎啡試驗,即于每只大鼠頸項部皮下注射阿樸嗎啡(80 μg/kg)30 min后,觀察陰莖勃起(判定標準為陰莖頭膨脹及遠端陰莖體露出)情況,計數勃起次數。
1.4 陰莖海綿體組織Cx43蛋白表達檢測及結果判定方法 各組分別于8、12、16周分批斷頸處死,解剖分離出陰莖組織,于陰莖近段切取海綿體5 cm,10%中性甲醛固定,石蠟包埋,4 μm連續切片。用0.5%H2O2/甲醇室溫處理30 min滅活內源性過氧化物酶;蒸餾水洗滌3次,滴加3%檸檬酸新鮮稀釋的胃蛋白酶,37℃消化4 min,0.5 M的PBS洗滌;每張切片上滴加20 μL兔血清(1∶20),37℃濕盒20 min。20 μL的Cx43蛋白抗體37℃濕盒60 min; 0.5 M的PBS洗滌,滴加生物素化羊抗兔IgG,37℃、30 min;滴加SABC,37℃、30 min,0.5 M的PBS洗滌5 min×3次;DAB顯色20~30 min,蘇木素復染,二甲苯透明,中性樹膠封片保存。結果判定:每張切片隨機觀察10個不重復的高倍視野,以細胞質出現棕黃色顆粒作為陽性,計數染色陽性細胞百分率。其中細胞染色弱、陽性細胞<5%為陰性,陽性細胞5%~50%為弱陽性,陽性細胞>50%為強陽性。
1.5 統計學方法 采用SPSS11.0軟件進行統計學處理。計量資料以±s表示,組間比較采用t檢驗;計數資料比較采用χ2檢驗。P≤0.05為差異有統計學意義。
2 結果
2.1 陰莖勃起情況 與對照組相比,血管、神經、DM因素組大鼠勃起功能均有明顯喪失(P均 <0.01),見表1。
2.2 陰莖海綿體組織Cx43蛋白表達情況 DM因素組、血管因素組及神經因素組陰莖海綿體組織Cx43蛋白表達均明顯低于對照組(P均<0.01),見表2。

表1 各組陰莖勃起功能情況比較
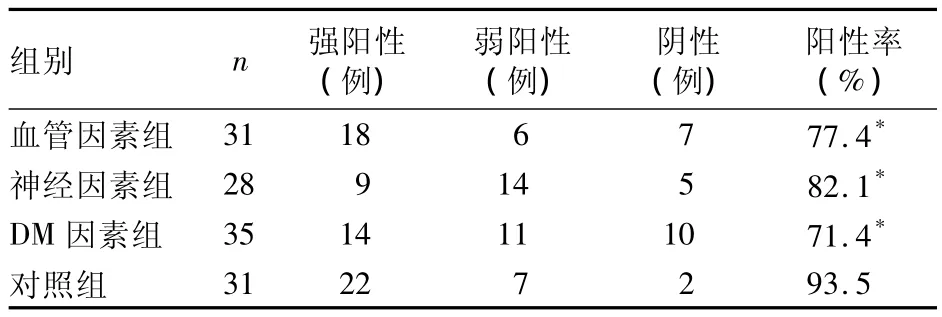
表2 各組陰莖海綿體組織Cx43蛋白表達比較
3 討論
ED是指各種原因導致陰莖血流動力學變化異常引發的陰莖勃起異常,表現為不能完成正常性生活。許多種因素均可引發ED,最主要的包括神經因素、激素性因素、動脈性因素和海綿體因素[3]。研究顯示,DM患者通常比正常人群早10~15 a出現性功能障礙[4]。DM性ED可能受到多種因素影響。DM引起的神經和血管病變被認為是導致DM性ED的兩大主要因素。DM的全身神經病變在DM早期即可出現,其可使陰莖神經傳導受到影響,并引起相關神經遞質濃度的改變。血管組織改變可能是DM性ED最主要的病理學改變[5],而DM可導致大血管和微血管改變,其中DM性大血管病變可造成陰莖供血改變,使陰莖血管管徑變細、彈性下降;而微血管病變可更進一步引起陰莖海綿體血流灌注不足,導致陰莖海綿體組織缺氧以及海綿體平滑肌功能損傷。
陰莖海綿體由網絡狀海綿體小梁和小梁間隙構成,其中小梁含大量平滑肌,平滑肌細胞間的縫隙連接是細胞間液體彌散的重要通道,對維持組織反應的整體性、協調性具有重要意義。縫隙連接蛋白包括很多基因家族(其中16種蛋白的作用比較明確),其命名源自相對分子質量(26~57 kD)。Cx43是縫隙連接蛋白家族中首要的海綿體平滑肌細胞功能相關蛋白[6],是陰莖海綿體平滑肌功能的一個重要分子生物學指標。李錚等[7]對9例ED患者以RT-PCR方法進行陰莖海綿體組織Cx43 mRNA檢測,結果發現ED患者陰莖海綿體Cx43 mRNA表達量明顯低于正常對照組。Brink等[8]通過對大鼠DM模型的研究發現,DM大鼠陰莖勃起功能下降的同時,其海綿體細胞中Cx43相關縫隙連接通道的電子傳導能力改變,但Cx43影響的機制和縫隙連接的電子傳導能力之間的相關性未能得到明確證實。本研究結果顯示,DM因素組、血管因素組及神經因素組陰莖勃起比例及次數均明顯低于對照組,陰莖海綿體組織Cx43蛋白表達顯著低于對照組,尤以DM因素組為著。進一步證實血管因素、神經因素及DM因素均可誘發ED;DM性海綿體功能損傷與DM性ED相關。可能機制是DM可能通過影響Cx43基因表達造成海綿體平滑肌細胞縫隙連接功能障礙,從而進一步導致陰莖海綿體平滑肌功能降低,陰莖勃起功能喪失。
總之,Cx43蛋白表達下降在各種因素所致ED發病中均具有重要作用,尤以DM性ED為著;此為DM性ED的預防和治療提供了新思路。
[1]Romeo JH,Seftel AD,Madhun ZT,et al.Sexual function in men with diabetes type 2:association with glycemic control[J].J Urol,2000,163(3):788-791.
[2]Grant PS,Lipscomb D.How often do we ask about erectile dysfunction in the diabetes review clinic development of a neuropathy screening tool[J].Acta Diabetologica,2009,46(4):285-290.
[3]Christ GJ,Lue T.Physiology and biochemistry of erections[J].Endocrine,2004,23(2-3):93-100.
[4]Price D,Hackett G.Management of erectile dysfunction in diabetes:an update for 2008[J].Curr Diab Rep,2008,8(6):437-443.
[5]Boulton AJ,Selam JL,Sweeney M,et al.Sildenafil citrate for the treatment of erectile dysfunction in men with TypeⅡdiabetes mellitus[J].Diabetologia,2001,44(10):1296-1301.
[6]Wang CY,Liu HJ,Chen HJ,et al.AGE-BSA down-regulates endothelial connexin43 gap junctions[J].BMC Cell Biol,2011,12 (1):19.
[7]李錚,蔣健航,張賢生,等.勃起障礙者陰莖海綿體Cx43和nNOS mRNA的表達[J].上海第二醫科大學學報,2005,25(4):399-400,403.
[8]Brink PR,Valiunas V,Wang HZ,et al.Experimental diabetes alters connexin 43 derived gap junction permeability in short-term cultures of rat corporeal vascular smooth muscle cells[J].J Urol,2006,175(1):381-386.

