聲電氧化處理亞甲基藍廢水的研究
馬文姣,戴啟洲,王家德,陳建孟 (浙江工業大學生物與環境工程學院,浙江 杭州 310014)
我國是全球第一大染料生產與使用國家.染料生產和使用過程中排放的廢水污染控制為當前環境工作的難點與重點之一[1-3].
聲化學和電化學法都是新型高級氧化水處理技術,聲化學利用空化效應可在常溫下實現局部高溫高壓;電化學氧化技術則具有處理效率高、操作簡單、無二次污染等優點[4-5].但是在廢水處理過程中,聲化學存在效率不高的不足,電化學法則存在電極鈍化、毒化及電流效率較低等問題.將聲化學引入到電化學過程中,一方面空化效應產生強氧化性物質,同時具有加速傳質、活化電極表面等特性;另一方面利用超聲的清洗作用,實現電極的原位再生,提高電化學體系的催化效果.因此,聲電氧化法是集成了聲化學及電化學優點的一種新型處理技術.
采用聲電氧化工藝處理時,可以從兩方面加強電化學降解:在 ECS(電化學體系)中導入超聲后,水溶液中會發生空化作用.這時物系可劃分為空化氣泡,空化氣泡表面層和液相主體 3個區域[6-7]:①空化氣泡,由易揮發溶質,水蒸氣及空化氣體的蒸汽組成,在空化氣泡崩潰的極短時間內,氣泡內的水蒸氣可發生熱解反應,產生大量的·OH[8-10].②氣泡表面層,它是氣相的一層很薄的超熱液相層,存在著高濃度的·OH,且水呈超臨界狀態,極性、難揮發溶質可在該區域內進行·OH氧化和超臨界氧化反應.③液相主體,該區域的反應量很小.超聲降解水體中化學污染物主要發生在空化氣泡及其表面層這2個區域,可單獨或同時發生直接熱分解,·OH等自由基的氧化和超臨界氧化等.
本研究開發了稀土摻雜二氧化鉛電極,并將其用于聲電氧化體系,考察了聲電耦合氧化條件下的協同效應及其作用規律,為染料廢水的污染控制提供基礎數據.
1 材料與方法
1.1 實驗裝置
實驗裝置由超聲發生器,不銹鋼反應槽和直流電源三部分組成.超聲發生器采用槽輻射式反應器,換能器型號 JPCQ0628(頻率范圍為 10~160Hz,功率為 60~600W).陽極電極尺寸為7cm×1cm,電極極距6cm,該電極制備在前期將氟樹脂摻雜到 β-PbO2鍍層中[11]基礎上,在電沉積過程中摻雜稀土氧化物(La2O3,CeO2)[12],制備了稀土摻雜含氟二氧化鉛電極.連接的直接電源型號為 MPS601,電源的正極接電極陽極,負極接陰極(純鈦電極).實驗開始時在反應器內加入250ml不同濃度的亞甲基藍模擬染料廢水.
1.2 電極制備
1.2.1 電極的粗化處理 首先將 1cm×7cm× 1mm的Ti基體分別用240目和600目砂紙打磨拋光,使之呈銀白色金屬光澤.打磨的目的是使金屬粗糙表面平坦、光滑.然后用蒸餾水沖洗干凈.再用10wt%的NaOH熱堿液脫油、水洗,除去Ti基體表面的油污.再用體積比為 1:2的鹽酸水溶液在80℃下刻蝕0.5h.處理后的Ti基體表面形成凹凸不平的均勻麻面狀.
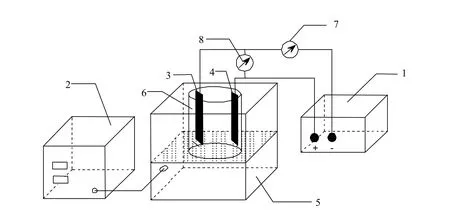
圖1 實驗裝置示意Fig.1 Schematic diagram of the experimental system
1.2.2 電極底層的制備 涂液組成:32gSbCl3, 150gSnCl4·5H2O,50mL濃鹽酸,300mL的 n-C4H9OH.用刷子或毛筆將涂層溶液均勻地涂刷至Ti基體表面,在100℃~150℃的管式電爐中烘20min,重復5~7次,再在500℃的管式電爐中熱分解2h,重復涂覆烘干和高溫分解1次,得到鍍有錫銻氧化物底層的電極.
1.2.3 堿性電鍍 α-PbO2層 堿性電鍍液組成:0.11mol/L的PbO+0.35mol/L的NaOH,槽電壓1~2V,將上述步驟處理后的電極置于 PbO溶于NaOH溶液的飽和溶液中,溫度為 50℃~60℃,電流密度為0.3~0.5A/dm2,電鍍時間30~60min,此過程可用純鉛板做陰極.
1.2.4 酸性電鍍 β-PbO2層 酸性電鍍液組成:0.45~0.6mol/L的HNO3,0.35mol/L的HNO3, 0.025~0.035mol/L的KF,60wt%的聚四氟乙烯乳液6~7mL/L.加入一定量的La、Ce,通氮氣曝氣下加熱至(80±2)℃,槽電壓 2.6~3.0V,pH0.5~1.5,電流密度為5~6A/dm2下電鍍1.5h,電鍍過程中用碳酸鉛調節鉛離子濃度,用過氧化氫消除電鍍時產生的NO2-離子.制備后可以得到 Ti/SnO2+ Sb2O3/PTFE+La+β-PbO2電極(以下簡稱 La-PbO2/Ti電極),未摻雜電極記為 PbO2電極和Ti/SnO2+Sb2O3/PTFE+Ce+β-PbO2電極(以下簡稱Ce-PbO2/Ti電極).
1.3 實驗對象
陽離子染料亞甲基藍(MB)在水溶液中形成一價有機陽離子型的季胺鹽離子基團,亞甲基藍分子式:C16H18ClN3S[13],所用溶液均用超純水配制,溶液pH值用H2SO4或NaOH調節.
1.4 分析方法
對亞甲基藍隔時取樣(0,5,10,20,30,60,90, 120,150,180min),對水樣進行分析.亞甲基藍去除率用 U-2910型紫外、可見分光光度分析,在180~900nm范圍內用石英比色皿掃描,吸收最大峰在663nm處.COD檢測采用CTL-12型化學需氧量測定儀.pH值采用雷磁pHs-3E型pH計進行分析.甲酸、乙酸、乙二酸、苯甲酸等小分子酸以及陰離子采用離子色譜Dionex ICS-2000分析來測定,中間產物用氣相色譜-質譜 GC7890/ MS5975來分析,測試方法如下:升溫程序 35℃,保持2min,以5℃/min升到200℃,保持15min,溶液延緩4min.
2 結果與分析
2.1 電極材料對聲電降解的影響
亞甲基藍初始濃度為 100mg/L,電流密度為71.43mA/cm2,硫 酸 鈉 為 17.75g/L,功 率 為34.71W/cm2,頻率為 50Hz.以鈦片為陰極,比較以上3種自制電極,反應進行3h后,對亞甲基藍的去除率.
電極材料的選擇是電化學反應器設計的重要部分,電極材料不同,不僅會影響電流密度、電流效率等工作特性,還可能導致電化學反應途徑的不同.目前用于水處理研究與應用的電極材料主要有碳和石墨電極、鉑電極氧化鉛電極、DSA電極、金剛石電極、SnO2-Sb2O5/Ti電極等.從圖2可以看出,隨著反應的進行,亞甲基藍的去除率逐漸增加,且 La-PbO2/Ti電極效果好于Ce-PbO2/Ti好于 PbO2/Ti電極.可見由于電極表面添加了稀土氧化物,增加了電極的比表面積,增大了電極與污染物的有效接觸面積,且摻雜稀土后,電極能有效地阻止 PbO2晶粒的連續生長,使得摻雜后的電極具有更均勻的微觀結構,從而改善了 PbO2電極的相關性能[14],有利于更好的降解有機污染物.
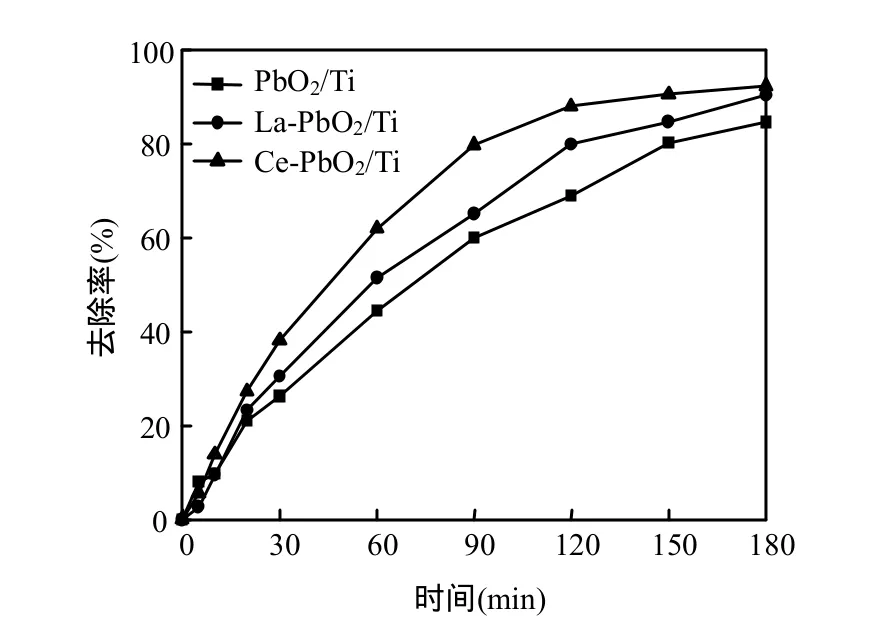
圖2 電極對亞甲基藍去除率的影響Fig.2 Effect of electrodes on the removal of methylene blue
由圖3可知,反應進行180min后,PbO2/Ti電極,Ce-PbO2/Ti電極和La-PbO2/Ti電極對COD的去除率分別達58.04%,68.94%和71.40%.說明添加稀土氧化物的電極作為陽極使污染物的礦化率明顯提高.
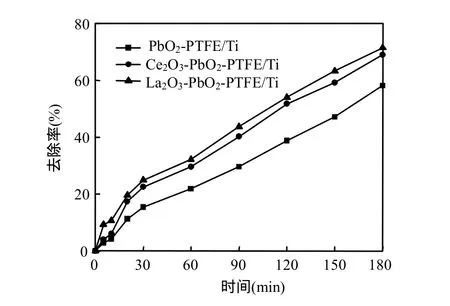
圖3 電極對染料COD去除率的影響Fig.3 Effect of electrode on the removal of dye COD
2.2 聲電協同體系
2.2.1 PbO2/Ti電極的聲電協同作用 (1)聲化學條件下亞甲基藍的降解:亞甲基藍初始濃度200mg/L,電解質14.2g/L,功率為49.58W/cm2, pH值為3,頻率為50 Hz,反應進行3h.(2)電化學條件下亞甲基藍的降解:亞甲基藍初始濃度200mg/L,電解質14.2g/L, pH值為3,電流密度為71.43mA/ cm2,陽極為 PbO2/Ti電極,鈦片為陰極,反應進行3h.(3)聲電氧化條件下亞甲基藍的降解:在聲化學(1)和電化學(2)的條件下共同作用于亞甲基藍3h,測定各時刻的去除率.
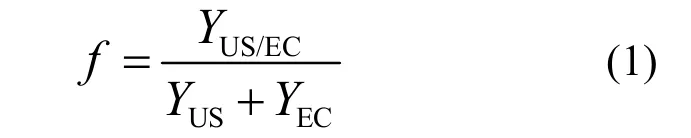
式中: f為聲電協同因子; YUS、YEC、YUS/EC,分別為聲化學條件下的去除率、電化學條件下的去除率、聲電氧化條件下的去除率.
分別在(1),(2),(3)條件下進行反應,由圖 4可知,采用PbO2/Ti做陽極時,測得亞甲基藍在單獨聲化學條件下,單獨電化學條件下,聲電氧化條件下的去除率依次為4.12%,66.05%,90.55%,按式(1)進行計算, f=1.29, f>1,表明聲電氧化降解污染物的過程中,不單是聲化學和電化學氧化降解簡單相加,兩者還具有協同作用.
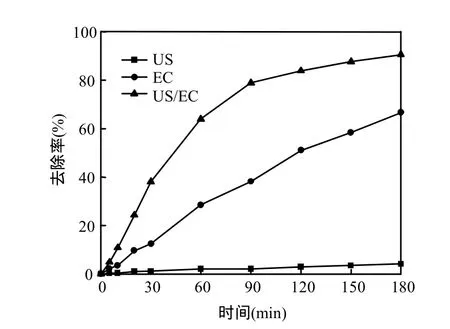
圖4 工藝降解對亞甲基藍去除率的影響Fig.4 Effect of processes on the removal of methylene blue
2.2.2 La-PbO2/Ti電極的聲電協同作用 (1)聲化學條件下亞甲基藍廢水的降解:亞甲基藍200mg/L,功率為49.58W/cm2,頻率為50Hz,電解質14.2g/L,pH值為3,反應進行3h.(2)電化學條件下亞甲基藍的降解:亞甲基藍 200mg/L,電解質14.2g/L, pH值為3,電流密度為71.43mA/cm2, La-PbO2/Ti為陽極,陰極為鈦片,反應進行3h.(3)聲電化學條件下亞甲基藍的降解:聲化學(1)和電化學(2)同時作用亞甲基藍 3h,測定各時刻的去除率.
采用La-PbO2/Ti為陽極時,測得亞甲基藍在單獨聲化學條件下的去除率僅為 4.12%,單獨電化學時的去除率為67.56%,而聲電氧化去除率為97.54%,按式(1)進行計算, f=1.36, f>1,則兩者具有協同作用.可見聲化學的引入對降解起到了明顯的促進作用,兩者協同較為明顯.La-PbO2/Ti電極比 PbO2/Ti電極具有更高的協同因子,因為添加少量的 La2O3,可以改善電極表面的微觀結構,減小鍍層內應力,增強電極的穩定性,提高電極的催化活性.
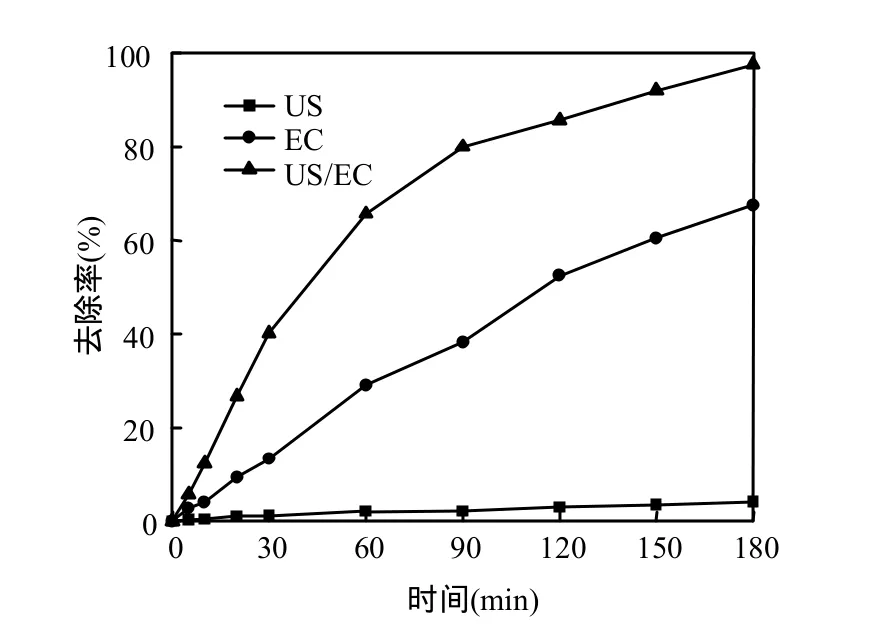
圖5 工藝降解對亞甲基藍去除率的影響Fig.5 Effects of processes on the removal of methylene blue
2.3 聲電氧化降解亞甲基藍作用規律研究
2.3.1 功率的影響 亞甲基藍初始濃度200mg/L,硫酸鈉加入 14.2g/L,電流密度為 71.43mA/cm2.陽極為 La-PbO2/Ti電極,鈦片為陰極,頻率為50Hz,考察不同功率下(12.40,36.71, 49.58W/cm2)亞甲基藍的去除率.
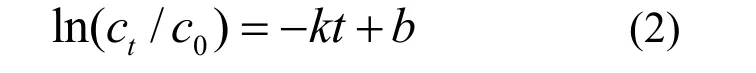
式中: ct為t時刻污染物的濃度,mg/L; c0為污染物的初始濃度,mg/L; k為表觀反應速率常數,10-2/min; t為時間, min; b為常數項.
聲功率指單位時間內輻射到反應系統中的實際總聲能,而聲強是單位超聲發射端面積的聲功率,只有當輸入到液體中的聲功率大于空化閾時,才能產生空化效應.頻率不變時,增加超聲功率能加快降解速度,增大空化強度,對氧化反應有利[15],即隨著功率的增大,反應速率逐漸升高[16],由圖6可見,當功率為12.40W/cm2時,亞甲基藍的脫色率為36.13%,當功率上升至36.71W/cm2時,亞甲基藍的脫色率提高到52.21%,功率49.58W/ cm2約為36.71W/cm2的1.35倍,按式(2)計算,表觀反應速率常數卻是它的3.08倍,所以較佳功率為49.58W/cm2.
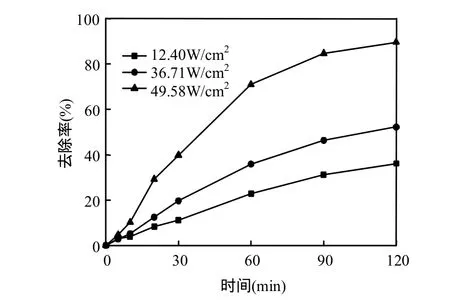
圖6 功率對亞甲基藍去除率的影響Fig.6 Effect of power on the removal of methylene blue
2.3.2 頻率的影響 在前期實驗的基礎上,選擇49.58W/cm2為較佳功率,其他條件固定不變.考察不同頻率下(10,50,100Hz)亞甲基藍的去除率.
由圖7可知,在頻率10Hz時亞甲基藍的去除率為 70.43%,50Hz時達 89.50%,而當頻率為100Hz時下降為56.45%,可見在一定頻率強度范圍內,污染物的去除率隨著超聲頻率的增大而增加,但當超過一定值后,隨著超聲的頻率增加,液體介質中的空化氣泡減少,空化作用強度下降,聲化學效應也相應地下降[17].由式(2)得,當頻率為50Hz時的表觀反應速率常數為 2.00×10-2min-1,而當頻率增加到 100Hz時表觀反應速率常數降低至 0.73×10-2min-1.因此,在聲電降解過程中,去除率和頻率之間可能有一個最佳匹配值,故選擇50Hz為較佳頻率.
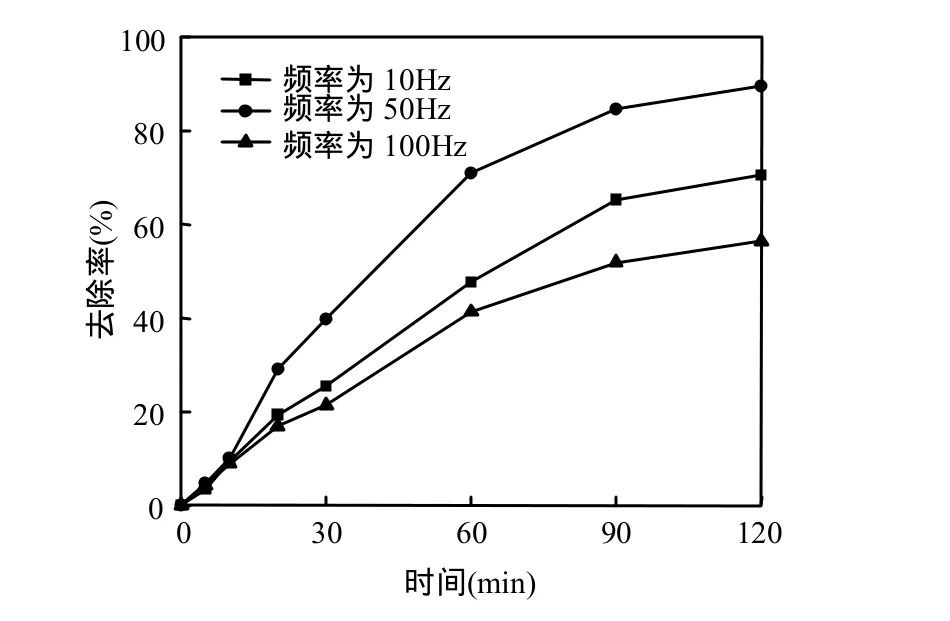
圖7 頻率對亞甲基藍去除率的影響Fig.7 Effect of frequency on the removal of methylene blue
2.3.3 電解質濃度的影響 電解質的加入,可以增加溶液的導電性能,會使槽電壓降低,也可以使電解過程中發生復雜的電化學反應.前期優化的條件固定不變,考察不同電解質(7.1,14.2,28.4g/L)對去除率的影響.
由圖 8可知當硫酸鈉濃度分別為 7.1,14.2, 28.4g/L時,2h后亞甲基藍的去除率依次為84.26%, 89.51%,88.88%,可見不同濃度電解液中亞甲基藍的去除率均在 84%~89%之間,可推知當電解質濃度在一定范圍內變化時,對污染物的去除率影響不大.這與王金麗等[18]的研究結果一致.按式(2)計算,表觀反應速率分別為 1.67×10-2,2.00× 10-2,1.90×10-2min-1,故綜合考慮選擇14.2g/L的為較優條件.
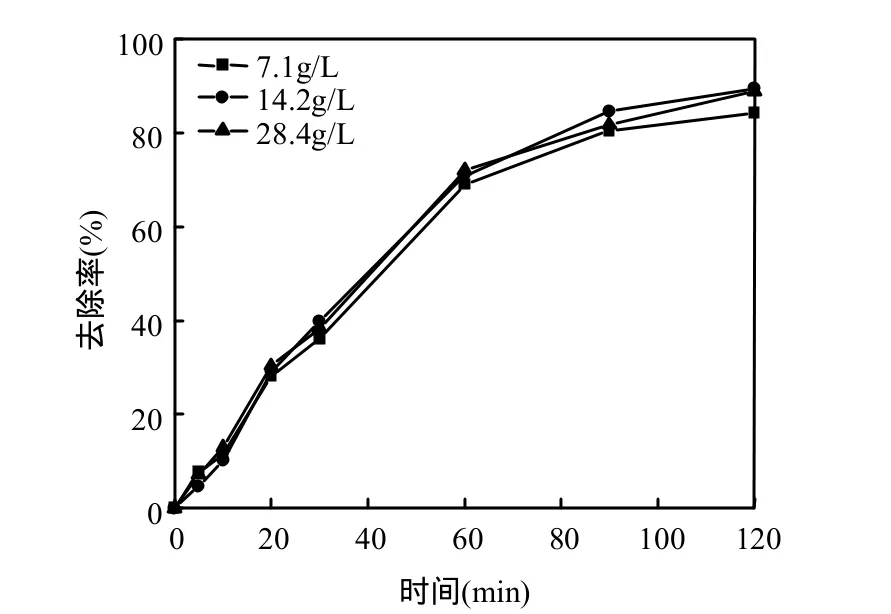
圖8 電解質濃度對亞甲基藍去除率的影響Fig.8 Effect of electrolyte concentration on the removal of methylene blue
2.3.4 電流密度的影響 保持其他因素不變,考察不同電流密度(14.29,71.43,285.71mA/cm2)條件下的去除率.
電流密度大小是影響污染物降解的重要因素之一,電流密度較大時,可以產生的更多的·OH,電子轉移速率加快,電極表面發生的氧化反應速率加快[19].當電流密度為 14.29,71.43,285.71mA/ cm2時,亞甲基藍的脫色率依次為55.86%,89.51%, 97.82%.由式(2)計算,表觀反應速率依次為 0.71× 10-2,2.01×10-2,3.22×10-2min-1. 電 流 密 度285.71mA/cm2為71.43mA/cm2的4倍,而表觀反應速率之比僅為1.61.故當電流已足夠大時,增加槽電壓無法明顯改善處理效果,綜合考慮經濟等因素選擇71.43mA/cm2為較優電流密度.
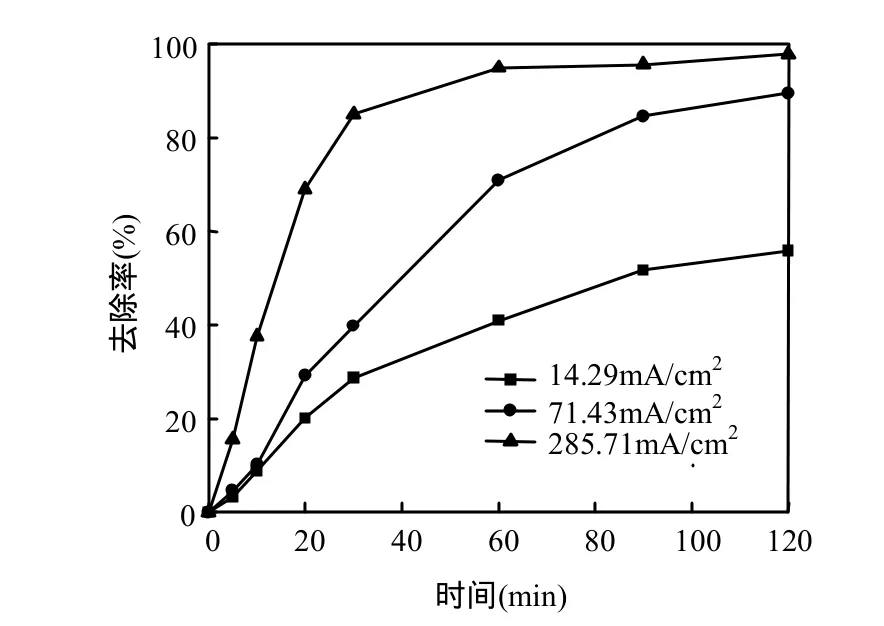
圖9 電流密度對亞甲基藍去除率的影響Fig.9 Effect of current density on the removal of methylene blue
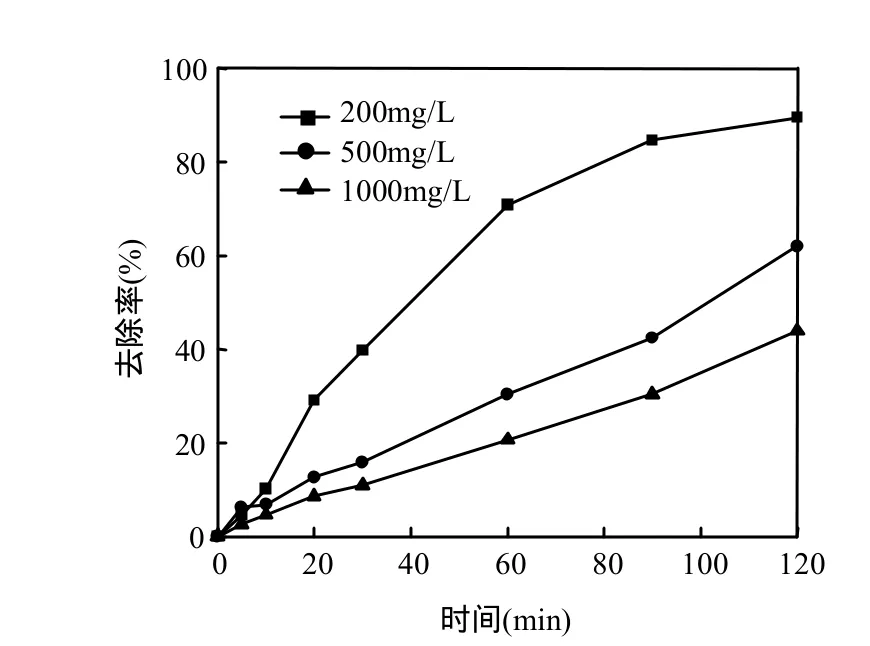
圖10 初始濃度對亞甲基藍去除率的影響Fig.10 Effect of concentration on the removal of methylene blue
2.3.5 初始亞甲基藍濃度的影響 在其他條件不變的前提下,考察不同濃度亞甲基藍(200,500, 1000mg/L)對去除率的影響.
一般來說因污染物的濃度足夠大時,單位污染物氧化能力下降[20].當亞甲基藍的濃度分別為200,500,1000mg/L時去除率依次為 89.51%, 62.00%,43.95%.由式(2)得,表觀反應速率常數依次為 2.00×10-2,0.73×10-2,0.45×10-2min-1.可能由于初始濃度高,有機物的濃度大,作用在單位濃度污染物上的·OH含量減少,導致去除效果下降.
2.4 聲電氧化處理亞甲基藍的降解途徑分析
2.4.1 聲電反應條件下小分子酸的測定 亞甲基藍初始濃度200mg/L,功率49.58W/cm2,頻率為50Hz,溶液pH值為3,電流密度71.43mA/cm2,硫酸鈉 14.2g/L,陽極為 La-PbO2/Ti電極,在 30,60, 120,180min時取樣.
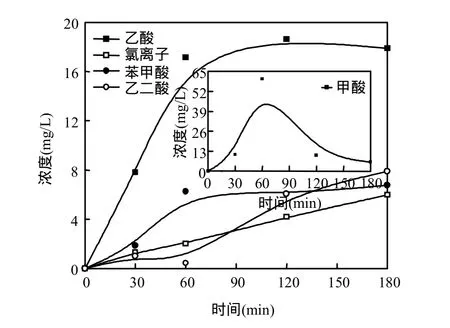
圖11 聲電氧化工藝下小分子酸的變化Fig.11 Change of acid molecules under sonoelectrochemical degradation
從圖11可以看出,在反應開始的60min內,甲酸含量逐漸增加,隨后下降,至180min時,甲酸含量為5.97mg/L.氯離子含量隨著反應時間的增大逐步上升,至180min處達5.97mg/L.但量較小,可能是亞甲基藍含氯率較低.在反應進行3h過程中硫酸根的含量大致不變.在 120min前,苯甲酸的含量高于乙二酸,120min后乙二酸的含量超過了苯甲酸,可能是由于苯甲酸部分轉化為乙二酸所致.與單獨超聲降解相比由于少量的氯離子存在,其可與自由基結合形成具有強氧化性的次氯酸、高氯酸等物質,在一定程度上更好地氧化了污染物.
2.4.2 聲電聯合條件下中間產物分析 為了進一步了解污染物的轉化,用GC-MS進行分析,在30,60,120,180min處以及混合各時間段取樣, GC-MS中間產物可能存在著2條途徑.
由圖12可知,在聲化學和電化學共同作用下,產生局部高溫高壓和大量的自由基,一方面亞甲基藍中間環的碳氮鍵先被打斷,部分甲基脫落,氧化成 M1,另一方面甲基一部分氧化成氨基,一部分脫落,碳氮鍵斷開即為物質M2, M1中的碳氮鍵進一步脫落生成M3, M2氧化為M4, M3和M4經脫環、酸化,進一步氧化形成 M5即苯甲酸,再繼續氧化成甲酸、乙酸、乙二酸等小分子酸,羥基自由基與大多數有機污染物可以發生快速的鏈式反應,無選擇地把有害物質氧化成CO2、H2O[21].各序號所對應中間產物如表1所示.
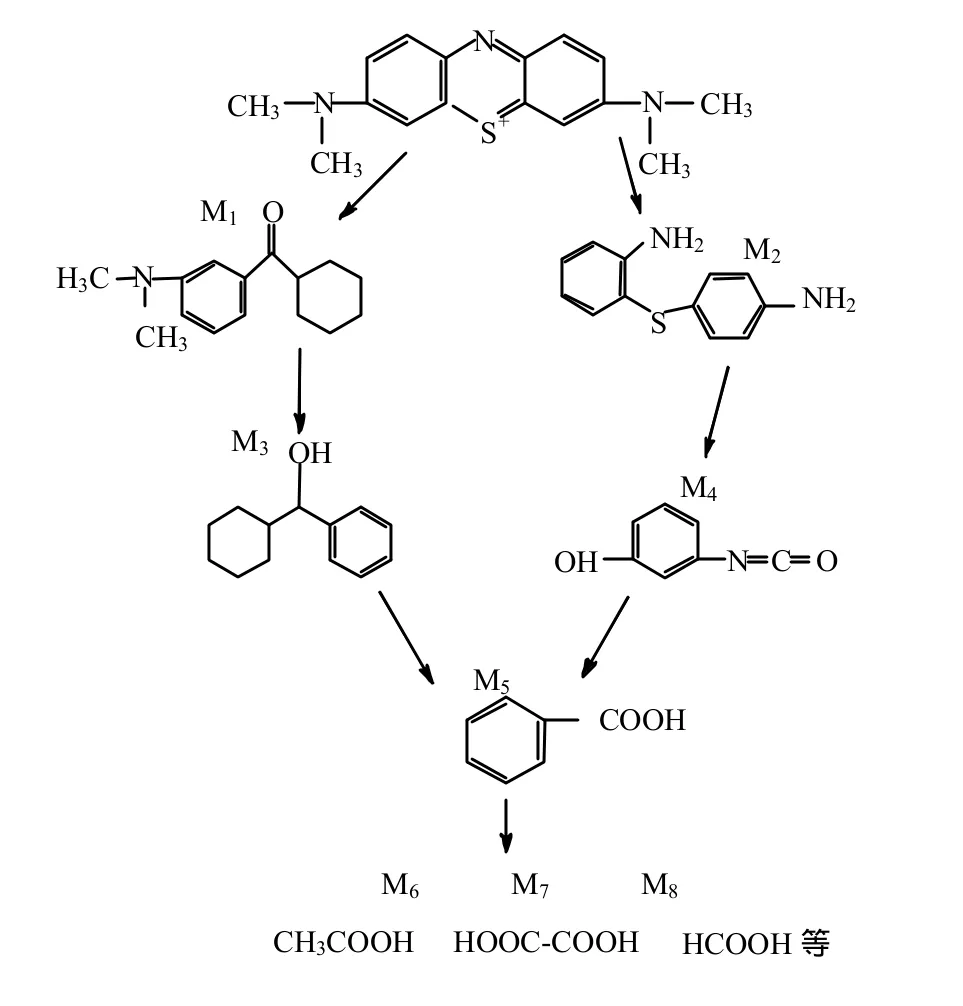
圖12 聲電條件下可能的降解途徑Fig.12 The possible degradation process under acoustic-electric degradation
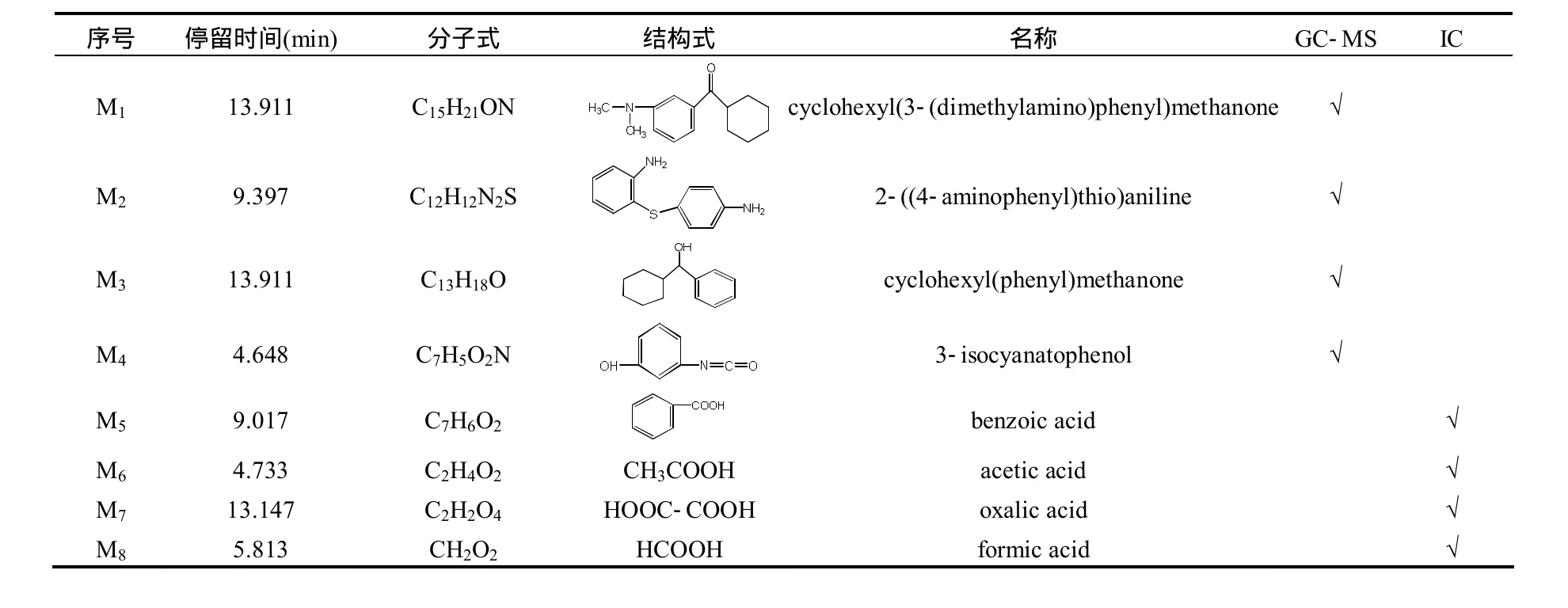
表1 聲電條件下可能的中間產物Table 1 Possible intermediate under acoustic-electric degradation
3 結論
3.1 制備的La/PTFE共摻雜二氧化鉛電極性能穩定,在聲電體系中具有良好的催化作用.其中PbO2/Ti和 La-PbO2/Ti電極作陽極時,聲電協同因子分別為1.29、1.36.
3.2 考察La/PTFE共摻雜二氧化鉛作為工作電極時聲電條件下的各影響因素作用規律,結果表明在優化條件下(200mg/L的亞甲基藍,功率為49.58W/cm2,頻率為50Hz,硫酸鈉為14.2g/L,電流密度為71.43mA/cm2,陽極為La-PbO2/Ti電極,鈦片為陰極)2h后的去除率為 89.51%.結合 IC、GC-MS分析檢測了各降解中間產物,推導了污染物可能的降解途徑.
[1] 丁徐紅,楊麗琴,朱成定.不銹鋼基 PbO2電極電催化氧化降解甲基橙性能的研究 [J]. 化學工程師, 2009,23(11):36-38.
[2] 劉高源,任建敏,趙子龍.印染廢水深度處理與評價 [J]. 重慶工商大學學報(自然科學版), 2008,25(6):618-623.
[3] 肖培平,謝永紅,張 雅.印染廢水治理方法研究與應用 [J]. 環境科技, 2008,21(A02):96-97, 100.
[4] Fockedey E, Vanlierde A. Coupling of anodic and cathodic reactions for phenol electro-oxidation using three-dimensional electrode [J]. Wat. Res., 2002,36(16):4169-4175.
[5] Korbahtj B K, Tanyolac A. Continuous electro-chemical treatment of phenolic wasterwater in a tubular reactor [J]. Wat. Res., 2003,37(7):1505-1514.
[6] 鄂利海,欒耕時,趙崇軍.功率超聲對電化學反應和電極表面的影響研究 [J]. 石油化工高等學校學報, 2001,14(2):54-58.
[7] Suslick K S, Didenko Y, Fang M M, et al. Acoustic cavitation and its chemical consequences [J]. Phil. Trans. R. Soc. Lond. A, 1999,35(1751):335-354.
[8] 何世傳,朱昌平,單鳴雷,等.超聲聯合臭氧用于廢水處理的研究進展 [J]. 聲學技術, 2005,24(3):173-177.
[9] 湯紅妍,羅亞田,查振林.超聲波降解苯酚溶液的研究 [J]. 環境技術, 2004,22(5):16-18.
[10] 朱昌平,馮 若,何世傳,等.用 3種方法研究雙頻超聲空化增強效應 [J]. 南京大學學報(自然科學), 2005,41(1):66-70.
[11] Zhou M H, Dai Q Z, Lei L C. Long life modified lead dioxide anode for organic wastewater treatment: electrochemical characteristics and degradation mechanism [J]. Environment Science and Technology, 2005,39(1):363-370.
[12] 周明華,戴啟洲,雷樂成,等.新型二氧化鉛陽極電催化降解有機污染物的特性研究 [J]. 物理化學學報, 2004,20(8):871-876.
[13] 趙立艷,王學凱,郭玉國,等.亞甲基藍在云母表面吸附狀態的研究 [J]. 物理化學學報, 2003,19(10):896-901.
[14] Casellato U, Cattarin S, Musiani M. Preparation of porous PbO2electrodes by electrochemical deposition of composites [J]. Electrochimica Acta, 2003,48(27):3991-3998.
[15] Liang J, Komarov S, Hayshi N. Improvement in sonochemical degradation of 4-chlorophenol by combined use of fenton-liked reagents [J]. Uitrasonic sonochemistry, 2007,14(2): 201-207.
[16] 鐘愛國.超聲波誘導降解甲胺磷 [J]. 化工環保, 2000,20(2): 17-19.
[17] 何德文,秦 艷,王偉良,等.超聲氧化聯合處理油墨廢水試驗研究 [J]. 中南大學學報(自然科學版), 2009,40(6):1482-1487.
[18] 王金麗,梁文艷,馬炎炎,等.Ti/RuO2電氧化法降解藻毒素MCLR影響因素的研究 [J]. 中國環境科學, 2008,28(8):709-713.
[19] 傅 敏,丁培道,蔣永生,等.超聲波與電化學協同作用降解硝基苯溶液的實驗研究 [J]. 應用聲學, 2004,23(5):36-40.
[20] 尚 巖,尚 琳,彭亞男,等.超聲降解有機廢水影響因素的探討[J]. 哈爾濱商業大學學報(自然科學版), 2003,19(3):277-281.
[21] 龐雅寧,趙國華,劉 磊,等.金剛石膜電極電化學氧化提高廢水可生化性的研究 [J]. 中國環境科學, 2009,29(12):1255-1259

