微波消解-氫化物發生原子熒光光譜法同時測定化肥中砷、汞含量
閔紅,劉曙,羅夢竹,金櫻華,任麗萍,李晨
(1.上海出入境檢驗檢疫局,上海 200135; 2.復旦大學環境科學與工程系,上海 200433)
微波消解-氫化物發生原子熒光光譜法同時測定化肥中砷、汞含量
閔紅1,劉曙1,羅夢竹2,金櫻華1,任麗萍1,李晨1
(1.上海出入境檢驗檢疫局,上海 200135; 2.復旦大學環境科學與工程系,上海 200433)
采用微波消解樣品前處理手段以及雙道原子熒光光度計,建立了微波消解-氫化物發生原子熒光光譜法同時測定化肥中砷、汞含量的方法。通過試驗確定了樣品前處理方法,對負高壓、燈電流,載氣、屏蔽氣、原子化器高度、酸度等測試條件進行了優化。在優化的工作條件下,砷、汞含量分別在0~50ng/mL和0~1.0ng/mL范圍內與熒光強度呈良好的線性關系,線性相關系數分別為0.999 6,0.999 6,檢出限分別為0.085,0.008 ng/mL,回收率分別為88.8%~107.4%,90.0%~120%,測定結果的相對標準偏差均小于7%(n=6)。
微波消解;原子熒光光譜;化肥;砷;汞
在集約化農業生產高度發達的今天,化肥對農業的促進作用越來越顯著。隨著肥料使用量的不斷增加,我國面臨的肥料質量安全和環境安全問題日益突出[1,2]。根據2010年2月9日公布的中國首次污染源普查結果,中國主要水污染物排放量有4成以上來自農業污染源。化肥受其生產母料及加工流程的影響容易含有砷、汞兩種典型的有毒有害元素,它們隨著化肥的施用進入生態系統,危害農作物、環境和人體健康[3,4]。
化肥中砷、汞的分析方法很多,但多數都存在著試樣的前處理復雜,消化試劑用量大,消化試劑分解對大氣產生污染重,易引起被測元素的損失等不足,且對于砷、汞兩種元素多為單獨測定,分析流程長[5,6]。筆者借助微波消解樣品前處理手段[7],充分利用原子熒光光譜法檢測靈敏度高、抗干擾性強、可進行兩種元素同時檢測等特點[8-10],建立了微波消解-氫化物發生原子熒光光譜法同時測定化肥中砷、汞含量的方法,實現了對化肥中砷、汞元素的快速、準確測定。
1 實驗部分
1.1 主要儀器與試劑
雙道原子熒光光譜儀:AFS 9800型,北京科創海光儀器有限公司;
砷、汞空心陰極燈:北京科創海光儀器有限公司;
微波消解/萃取工作站:MARS型,美國CEM公司;
水純化系統:Milli-Q Integral型,美國Millippore公司;
砷、汞標準儲備液:濃度均為1 000μg/mL,使用時逐級稀釋至需要濃度,國家標準物質研究中心;
硝酸、鹽酸:優級純;
硼氫化鉀、氫氧化鈉、硫脲、抗壞血酸:分析純;
實驗用水為二次蒸餾水。
1.2 儀器工作條件
負高壓:280V;原子化器高度:8 mm;燈電流:As 50mA,Hg 25 mA;輔助電流As 20mA,Hg 0mA;載氣流量:400mL/min;屏蔽氣流量:800mL/min。
1.3 實驗方法
(1)標準系列溶液配制
逐級稀釋砷、汞標準儲備液,配制成砷、汞雙元素標準混合使用溶液,含砷1 μg/mL,汞20ng/mL。分別移取0,0.25,0.50,1.00,2.50mL上述標準混合使用溶液于50mL容量瓶中,加入5 mL 50%鹽酸-硝酸混合酸(1+1)、10mL 5%硫脲-抗壞血酸溶液,用水稀釋至刻度,搖勻,靜置30min。
(2)樣品前處理
準確稱取0.1 g(精確至0.1 mg)化肥樣品于100mL消解罐中,加入10mL 50%鹽酸-硝酸混合酸(1+1),待反應緩和后,裝入外罐,旋緊密封,置于微波消解儀中,按表1設定的微波消解程序(消解條件應根據消解儀及壓力罐的不同而需驗證其合適性)進行消解,至消解完全。消解液冷卻后,用去離子水沖洗消解罐內壁,小心地將消解液轉移至50mL容量瓶中,加入10mL 5%硫脲-抗壞血酸溶液,用水稀釋至刻度,搖勻,靜置30min。同時做樣品空白試驗。
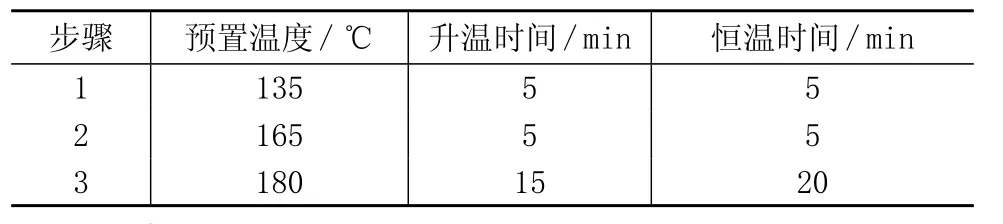
表1 微波消解條件
(3)樣品測定
將標準系列溶液、樣品空白和樣品溶液依次放入自動進樣器中,在儀器分析條件下進行測定。
2 結果與討論
2.1 樣品前處理方法
實驗比較了微波消解和濕法消解兩種不同樣品前處理方法對樣品檢測結果的影響。微波消解條件見表1。濕法消解條件:使用10mL 50%鹽酸-硝酸混合酸(1+1)在100℃電熱板加熱1 h,小心將消解液轉移至50mL容量瓶中,加入10mL 5%硫脲-抗壞血酸溶液,用水稀釋至刻度,搖勻,靜置30min。測定結果顯示,對于樣品中砷含量,兩種處理方法所得最終結果沒有明顯差異,但對于樣品中的汞含量,濕法消解處理的樣品最終檢測結果明顯低于微波消解處理的樣品,可能是由于濕法消解前處理過程處于敞開體系,容易引起汞揮發而損失。通過比較,作為化肥中砷、汞含量測定的前處理手段,微波消解對環境污染小,消解效率高,所測結果準確度高,尤其適合汞元素的檢測,是一種較為理想的樣品前處理手段。
2.2 儀器測量條件的優化
(1)負高壓和燈電流
負高壓和燈電流是影響熒光強度的主要因素。實驗考察了在200~320V范圍內負高壓對熒光強度的影響,結果表明,熒光強度隨著負高壓的增加而增大,但隨著負高壓的增加,噪聲也明顯增大,負高壓過高或過低時,熒光強度均不穩定,呈現出一定的波動。實驗將負高壓設定為280V,既能滿足檢測靈敏度的需要,又有利于延長空心陰極燈和光電倍增管的壽命。
試驗考察了燈電流對砷、汞熒光強度的影響,在10~100mA范圍內,砷的熒光強度隨燈電流的增大而增大;在10~50mA范圍內,汞的熒光強度先增大后減小,汞的燈電流在10~40mA范圍內比較合適。燈電流過大,噪聲隨之增大,實驗穩定性下降;燈電流過小,樣品的原子熒光強度較弱,信噪比較差。綜合考慮各方面因素,實驗選擇燈電流為砷燈50mA,汞燈 25 mA。
(2)載氣、屏蔽氣和原子化器高度
載氣流量的大小會影響進入原子化器中待測原子的濃度,進而影響檢測結果。載氣流量過大會稀釋反應產生的氫化砷蒸氣和汞蒸氣,使進入原子化器的砷原子和汞原子的濃度下降,從而削弱了其熒光強度;載氣流量過小則使形成的蒸汽無法迅速進入原子化器而產生記憶效應。實驗選擇載氣流量為 400mL/min。
屏蔽氣主要是為了防止周圍空氣進入原子化器,保證火焰形狀穩定,對熒光強度沒有顯著影響,實驗選擇屏蔽氣流量為800mL/min。
實驗表明,原子化器高度與原子的熒光強度有一定的關聯性。原子化器較低,爐口的反射光線較強烈,熒光強度較高;原子化器較高,原子的濃度較低,火焰不穩定,熒光強度有所減弱,實驗重復性不佳,實驗選擇原子化器高度為8 mm。
(3)酸度
考察了鹽酸-硝酸混合酸(1+1)酸度對混合標準溶液中砷、汞熒光強度的影響,酸度(體積分數)0.5%~10.0%的范圍內,對汞的測量影響不大;當酸度大于4.0%時,砷的熒光強度趨于穩定。考慮樣品消解用酸的情況,選擇5%鹽酸-硝酸混合酸(1+1)作為氫化物發生反應用酸。
(4)硼氫化鉀溶液濃度
考察了硼氫化鉀溶液的濃度對混合標準溶液中砷、汞熒光強度的影響,結果見圖1。由圖1可知,0.25%的硼氫化鉀溶液能夠使汞還原完全;在0.25%~5.0%范圍內,隨著硼氫化鉀含量的增加,氫氣氣流增大,導致汞的熒光強度下降。砷的熒光強度受硼氫化鉀含量的影響較大,硼氫化鉀含量在0.5%以下,由于生成氫化砷的反應難以進行,砷的熒光強度很小;當硼氫化鉀的含量大于0.5%時,砷的熒光強度隨著硼氫化鉀含量的增加而顯著增加,并在硼氫化鉀含量為2%時達到峰值;硼氫化鉀含量大于2%時,隨著氫氣氣流的增大,砷的熒光強度開始下降。實驗選擇2%的硼氫化鉀溶液進行氫化物發生反應。
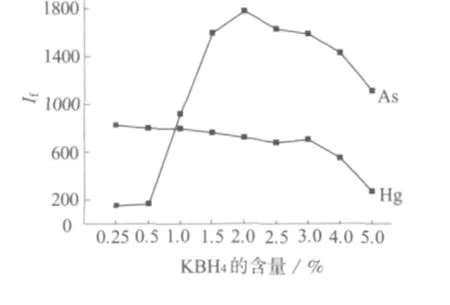
圖1 熒光強度與硼氫化鉀濃度的關系
(5)預還原劑用量與反應時間
化肥中的砷經50%鹽酸-硝酸混合酸(1+1)體系溶解后,以五價態存在于溶液中,采用氫化物發生法測定溶液中的砷,需要使用預還原劑將五價的砷預還原到三價砷,進行測定。實驗以抗壞血酸溶液為預還原劑,抗壞血酸還原過程需要一定的反應時間。在室溫下,15 min后還原反應完全,測定值穩定,實驗選擇30min后進行測定。實驗考察了抗壞血酸的用量,結果表明,配制50mL的測定溶液時,加入10mL 5%的抗壞血酸溶液能夠滿足測定要求。
2.3 共存離子干擾及消除
化肥中除了主要養分氮、磷、鉀之外,還含有微量的鈣、鎂、硫、硼、錳、鋅、鐵、銅、鎘、鉛、鉻等元素,這些元素含量很低,且大部分不能形成氫化物并對熒光信號產生干擾。對于部分能形成氫化物從而產生干擾的元素[11],通過加入10mL 5%的硫脲-抗壞血酸溶液后,存在的干擾基本能夠消除。
2.4 線性范圍與檢出限
對1.3(1)中配制的標準系列溶液用氫化物發生-原子熒光光譜儀進行測定,分別繪制砷和汞的標準曲線。砷的標準曲線回歸方程為If=-0.67+25.76c,相關系數r=0.999 6;汞的標準曲線回歸方程為If=-1.66+216.74c,相關系數r=0.999 6。
連續測量11次樣品空白的熒光信號,根據DL=3×s/k(s為11次樣品空白的標準偏差,k為線性回歸方程斜率),計算出方法的檢出限,砷、汞的檢出限分別為0.085,0.008 ng/mL。當稱樣量為0.1000g并定容至50mL時,以5倍檢出限計算樣品的測定限,以此方法計算得化肥中砷、汞的測定限分別為 0.21,0.02 μg/g。
2.5 精密度試驗
選取5個化肥樣品,平行進行6次試驗,按實驗方法進行溶樣,測定其砷、汞含量,計算精密度,結果見表2。對于不同含量水平的砷,相對標準偏差平均值為2.3%,對于不同水平含量的汞,相對標準偏差平均值為6.0%。
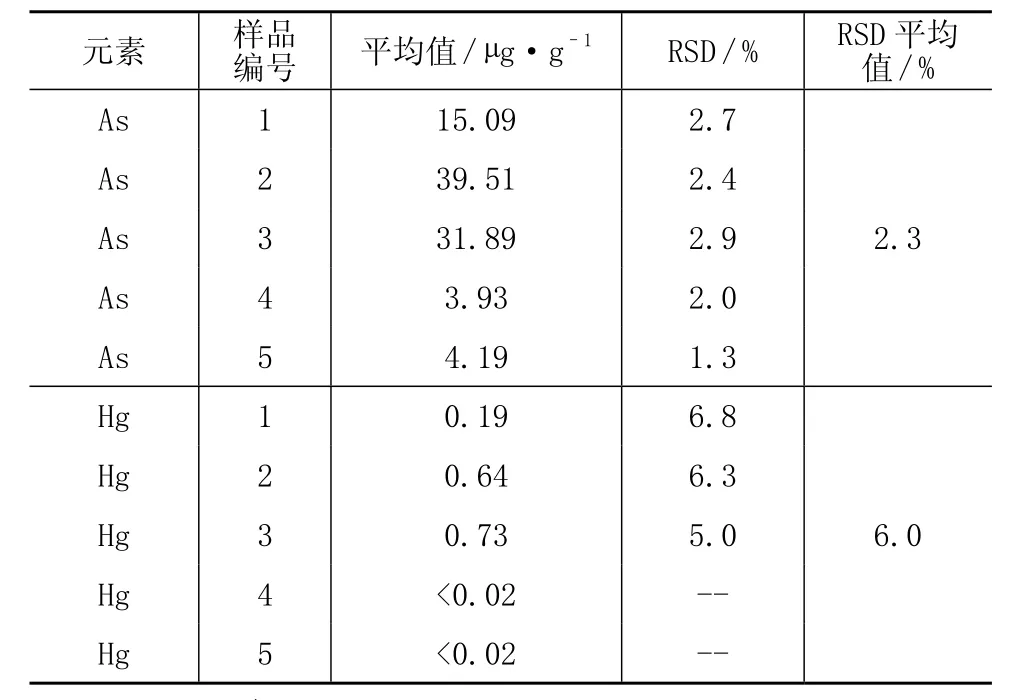
表2 精密度試驗結果(n=6)
2.6 回收試驗
對2.5中化肥樣品進行加標回收試驗,計算回收率,結果見表3。由表3可知,砷的回收率為88.8%~107.4%,汞的回收率為 90.0%~120%。
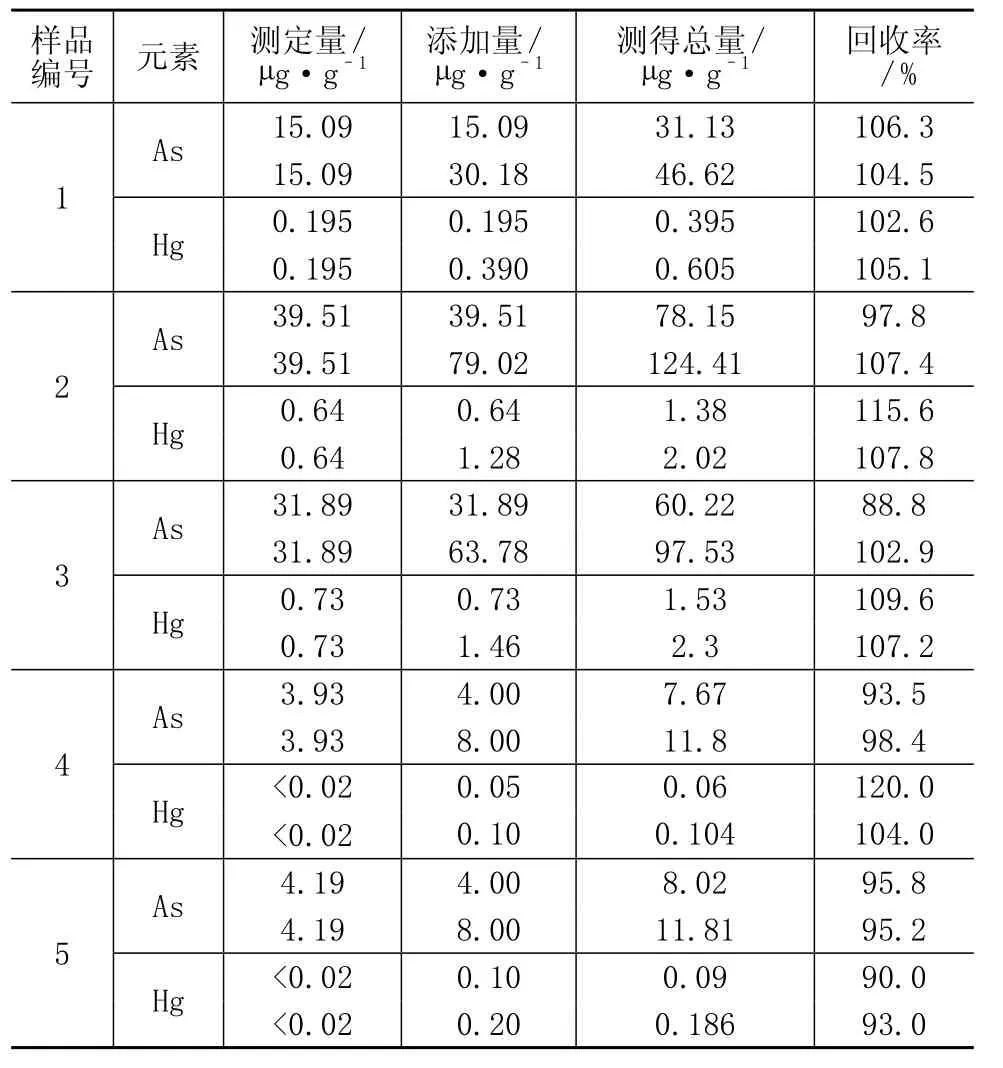
表3 加標回收試驗結果
3 結語
建立的微波消解-氫化物發生原子熒光光譜法能對化肥中的砷、汞兩種有毒有害元素進行同時檢測,樣品處理簡便快捷,基體干擾小,測出限低,能夠滿足大批量化肥樣品中痕量砷、汞的檢測。
[1]劉志紅,劉麗,李英.進口化肥中有害元素砷、鎘、鉛、鉻的普查分析 [J].磷肥與復肥,2007,22(2):77-78.
[2]封朝暉,劉紅芳,王旭.我國主要肥料產品中有害元素的含量與評價[J].中國土壤與肥料,2009(4):44-47.
[3]杜永,王艷,徐敏權,等.重金屬污染來源及對水稻生長與發育的影響[J].耕作與栽培,2004(2):13-16.
[4]康家琦,金銀龍.砷對健康危害的研究進展[J].衛生研究,2004,33(3):372-376.
[5]NY 1110-2006 水溶肥料汞、砷、鎘、鉛、鉻的限量及其含量測定[S].
[6]GB/T 23349-2009 肥料中砷、鎘、鉛、鉻、汞生態指標[S].
[7]周勇義,谷學新,范國強,等.微波消解技術及其在分析化學中的應用 [J].冶金分析,2004,4(2):30-34.
[8]駱斌.氫化物發生-原子熒光分析法進展及應用[J].西南民族大學學報,2006,32(2) :254-257.
[9]倪海燕,羅琦林.試論原子熒光現狀與發展[J].化工時刊,2008,22(5):47-48.
[10]曾澤,蔣維旗,謝琰.微波溶解-氫化物發生原子熒光光譜法測定氟石中的砷和汞[J].檢驗檢疫科學,2008,18(6):32-34.
[11]魏復盛,徐曉白,閻吉昌.水和廢水監測分析法指南(下冊[M].北京:中國環境科學出版社,1994:23.
Simultaneous Determ ination of As and Hg in Fertilizer by M icrowave Digestion and Hydride Generation Atom ic Fluorescence Spectroscopy
Min Hong1,Liu Shu1,Luo Mengzhu2, Jin Yinghua1,Ren Liping1,Li Chen1
(1.Shanghai Entry-Exit Inspection and Quarantine Bureau, Shanghai 200135, China; 2.Department of Environmental Science and Engineering, Fudan University, Shanghai 200433, China)
A method was proposed for the simultaneous determination of As and Hg in fertilizer by microwave digestion and hydride generation atomic fluorescence spectroscopy. Sample pretreatement method, negative high pressure,burner current, carrier gas, shieding gas, atomizer height acidity and so on were optimized. 0n optimal conditions,As correlation coefficient was 0.9996 in the linear range of 0~50ng/mL,while Hg correlation coefficient was 0.999 6 in the linear range of 0-1.0ng/mL. The detection limits of As and Hg were 0.085,0.008 ng/mL, respectively, and recoveries were 88.8%-107.4%,90.0%-120%,respectively. The relative standard deviations of As and Hg detetion results were less than 7%(n=6).
microwave digestion; atomic f luorescence spect roscopy; fer til izer; As; Hg
0657.34
A
1008-6145(2012)01-0020-04
10.3969/j.issn.1008-6145.2012.01.006
聯系人:閔紅;E-mai l:hongmin333_83@hotmail.com
2011-10-12

