氫過氧化物裂解酶的篩選及純化*
龍禎,阮奇珺,孔祥珍,張彩猛,華欲飛,江波
(江南大學食品科學與技術國家重點實驗室,江蘇無錫,214122)
氫過氧化物裂解酶的篩選及純化*
龍禎,阮奇珺,孔祥珍,張彩猛,華欲飛,江波
(江南大學食品科學與技術國家重點實驗室,江蘇無錫,214122)
研 究了不同植物原料中氫過氧化物裂解酶的含量,并最后篩選出莧菜作為提取原料。利用高速離心、表面活性劑溶解、硫酸銨分級沉淀、羥基磷灰石柱層析和離子交換色譜對莧菜氫過氧化物裂解酶進行純化至電泳純。結果表明,純化的莧菜氫過氧化物裂解酶分子量約為55ku,對于13-亞麻酸氫過氧化物的活力高于13-亞油酸氫過氧化物,最適pH6.0,最適溫度為25℃,在常溫下酶能保持較高水平的活力。
氫 過氧化物裂解酶,莧菜,純化,特性
植物氫過氧化物裂解酶(HPL)是植物脂氧化途徑中脂肪氧合酶(LOX)下游的酶,可將脂肪氧合酶和多不飽和脂肪酸形成的氫過氧化脂肪酸裂解形成含氧酸和揮發性醛類。它是植物產生清香風味成分基本途徑(LOX/HPL)的關鍵組成部分之一,且其催化產物還與植物抗病、抗蟲害有關[1]。近年來由于人們對天然香料的青睞,氫過氧化物裂解酶也逐漸受到人們的關注。
本課題對不同植物中氫過氧化物裂解酶含量進行比較和篩選,并選擇莧菜氫過氧化物裂解酶為研究對象進行初步分離純化和性質研究。本研究為酶法生產C6揮發性醛類奠定堅實的基礎。這是首次從中國種植莧菜中分離純化得到氫過氧化物裂解酶。
1 材料與方法
1.1 實驗材料
青椒、莧菜、茄子、豌豆苗、菠菜和綠豆芽均購于當地農貿市場。二硫蘇糖醇(DTT)、大豆脂肪氧合酶typeⅠ-B(LOX)、亞油酸、亞麻酸、己醛、己烯醛均購于Sigma公司。其他試劑為分析純。
CXG-I型電腦恒溫層析柜、HL-2型恒流泵、BS2-100型自動部分收集器,上海滬西設備廠;羥基磷石灰柱填料,上海Bio-red公司;DEAE-Tog-opeval柱頂料,上海TOSOH公司;柱套、上海錦華層析設備廠。
1.2 實驗方法
1.2.1 亞油酸氫過氧化物和亞麻酸氫過氧化物的制備
100 mg亞麻酸或亞油酸溶于2 mL無水乙醇中,后轉移至預先通氧氣至飽和的100 mL 0.2 mol/L pH9.0的硼酸鹽緩沖液中,隨后加入3 mg溶入少量的硼酸鹽緩沖液的LOX。快速攪拌均勻后在冰浴和持續通氧條件下反應1.5 h,隨后用6 mol/L HCl調節反應液至pH3.0以下結束反應。用等體積無水乙醚萃取反應液2次后合并有機相,加入無水MgSO4干燥,過濾后在30℃下旋轉蒸發除去乙醚,殘留部分為亞麻酸氫過氧化物(13-HPOT)或亞油酸氫過氧化物(13-HPOD)溶于一定量乙醇,充氮后分裝于 -20℃下密封保存。
1.2.2 同原料中氫過氧化物裂解酶的提取方法
100 g不同原料(青椒去籽去蒂、茄子去心去籽、綠豆芽子葉、豌豆苗葉、菠菜葉、莧菜葉)與300 mL 0.1 mol/L pH6.8的Tris-HCl(含0.5%PVP),勻漿3次共1 min得粗均漿液。4層紗布過濾,濾液于30 000 g、4℃離心20 min,棄去上清液,沉淀為氫過氧化物裂解酶(HPL)膜組分。而后用50 mL含0.5%Triton-X100的0.1 mol/L pH 8.5的Tris-HCl(和5 mmol/L DTT)溶解沉淀,4℃下攪拌1 h,在30 000 g、4℃下離心20 min,上清液即為溶解膜組分待用。
1.2.3 氫過氧化物裂解酶酶活的測定
采用分光光度法測定氫過氧化物裂解酶(HPL)的酶活。取x μL酶液(15~40 μL,因原料不同而不同)和 15 μL 10 mmol/L底物(13-HPOD 或 13-HPOT)與合適pH下的(2985-x)μL 0.02酸鹽緩沖液混合,在234 nm、1 min內測定其吸光值的線性下降。空白用x μL酶液和(3000-x)μL磷酸鹽緩沖液混合。1U酶活定義為每分鐘每裂解1 μmol/L 13-HPOD/13-HPOT所需的酶量(ε=25 000mol/(L·cm)[2].
1.2.4 蛋白含量的測定
采用的BCA法測定[3]。
1.2.5 各種來源氫過氧化物裂解酶液最適pH值測定
所用的緩沖液為pH 5.0的0.02 mol/L檸檬酸-磷酸氫二鈉緩沖液,pH 6.0、pH 7.0、pH 8.0的0.02 mol/L磷酸鹽緩沖液,pH 9.0的0.02 mol/L硼酸鹽緩沖液。
1.2.6 莧菜氫過氧化物裂解酶的純化
莧菜經1.2.2所述處理后經硫酸銨分級沉淀(5% ~35%飽和度)再于40 000g、4℃下離心30 min得沉淀,用少量0.01 mol/L,pH6.8的磷酸鈉緩沖液(其中含1 mmol/L DTT和0.5%Tritron X-100(緩沖液A))溶解后在相同緩沖液中透析過夜,在40 000 g、4℃下離心30 min,取上清液過0.22 μm 微孔濾膜。
過膜后酶液上經緩沖液A平衡過的羥基磷灰石柱(2.6 cm ×15 cm),用含 0.01、0.25和 0.4 mol/L磷酸鈉的緩沖液A進行階段洗脫,流速為3.0 mL/min,收集有酶活部分,用35%硫酸銨沉淀,離心,倒掉上清液,用少量0.02 mol/L,pH 8.5的Tris-HCl緩沖液(其中含1m mol/L DTT和0.5%Tritron X-100(緩沖液B))溶解,再在緩沖液B中透析過夜。
將透析液離心后,去上清,上經緩沖液B平衡的DEAE-Toyopearl柱((1.1 cm × 8.0 cm),用含 0,0.15,0.25和1.0 mol/L NaCl的緩沖液B進行階段洗脫,流速為1.0 mL/min,收集有酶活部分,用100 ku的超濾管濃縮(15 mL,Millipore,上海,中國)待用。
1.2.7 十二烷基硫酸鈉凝膠電泳(SDS-PAGE)
依照Laemmli[4]進行純化HPL樣品的十二烷基硫酸鈉凝膠電泳(SDS-PAGE)。分離膠和濃縮膠的聚丙烯酰胺終濃度分別為12%(w/v)和4%(w/v)。蛋白用考馬斯亮藍染色。標準分子量蛋白為:兔磷酸化酶b(97 400u),牛血清白蛋白(66 200u),兔肌動蛋白(43 000u),牛碳酸酐(31 000u),胰蛋白酶抑制劑(20 100u)和雞蛋清溶菌(14 400u)。
1.2.8 熱穩定性的測定
將粗酶液與0.01 mol/L磷酸鹽緩沖溶液的反應體系,分別在 25、30、35、40、45、50℃以及 55℃水浴中保溫一定時間后立即冰浴冷卻至室溫后,測定HPL的殘留活性。
2 結果與討論
2.1 各原料氫過氧化物裂解酶最適pH的比較
為了更準確地比較不同原料中HPL的酶活,先對其最適pH值進行了測定。由表1可以看出,幾種原料的最適pH值在5.5~7.0,且對于13-HPOD和13-HPOT其最適pH基本相同;而據報道,梨、茶葉和大豆子葉中最適pH都在中性[5,7]。不同來源的HPL對pH的敏感程度不同。青椒、莧菜HPL的最適pH在6.0附近,對pH的上升較敏感;而豌豆苗和菠菜最適pH在7.0左右,且對pH下降比較敏感。茄子HPL在pH值6.0~8.0酶活能夠維持在90%以上,在pH5.0時大約為80%,在pH9.0時仍能維持在60%以上,說明茄子HPL有著一個較寬的工作pH。
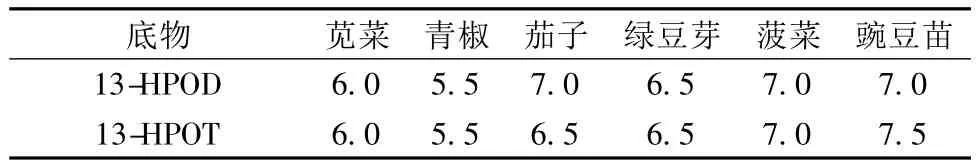
表1 不同原料中氫過氧化物裂解酶的最適pH
2.2 不同原料中氫過氧化物裂解酶酶活的比較
根據表1,在不同來源HPL的最適pH下分別測定其活力,結果見圖1。莧菜HPL的活性顯著高于其他被選原料。因此選用莧菜葉作為原料提取HPL。
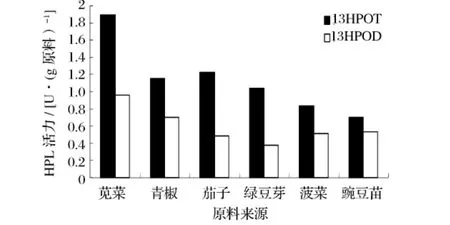
圖1 不同原料中氫過氧化物裂解酶的酶活
由圖1可知,所選原料中HPL對13-HPOT的活力更高。與 Fauconnier等人[10]和 Shibata 等人[5]發現番茄和青椒中的HPL也有類似的底物特異性的報道相吻合。然而,Olias等人[7]報道,在大豆幼苗中,HPL對13-HPOD的特異性高于13-HPOT。據報道,酶的特異性與生物體內真實脂肪酸組成是一致的。在莧菜葉中,亞麻酸是主要脂肪酸(占42%)[8],這符合HPL的底物特異性。相類似的亞麻酸在青椒中尤為豐富,而亞油酸是在大豆幼苗中占有優勢。
2.3 莧菜氫過氧化物裂解酶的分離純化
莧菜葉經均漿,高速離心,表面活性劑溶解和硫酸銨沉淀得到部分純化HPL,具體結果見表2。
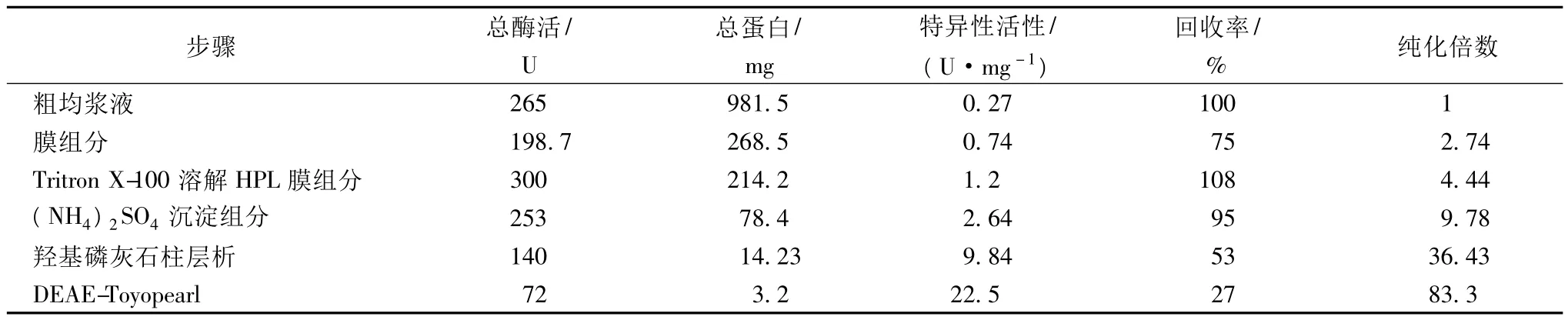
表2 莧菜中氫過氧化物裂解酶的分離純化
通過高速離心得到膜組分回收了莧菜葉粗均漿液中絕大部分的HPL,而0.5%Triton X-100能將HPL從膜組分上溶解和分離,比酶活提高1.8倍。隨后通過硫酸銨沉淀對HPL進行進一步純化。
經硫酸銨沉淀后的HPL粗酶液上羥基磷灰石柱,收集磷酸鹽濃度為0.25 mol/L的洗脫峰(見圖2)用硫酸銨進行濃縮,進行下一步分離純化。
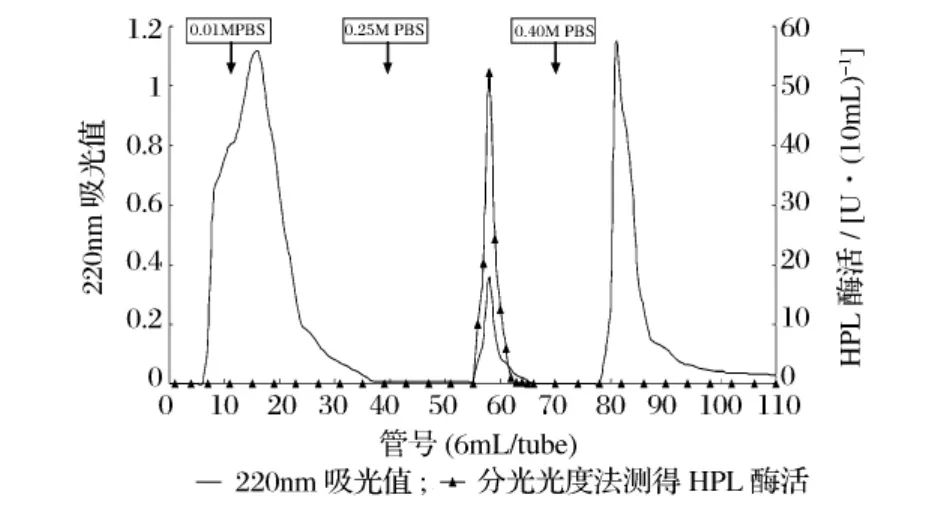
圖2 羥基磷灰石層析譜圖
將經羥基磷灰石柱層析的酶液上DEAEToyopearl柱,結果見圖3。收集活性組分,得到純化倍數為83.3倍的HPL,酶比活為22.5U/mg,回收率為27%。
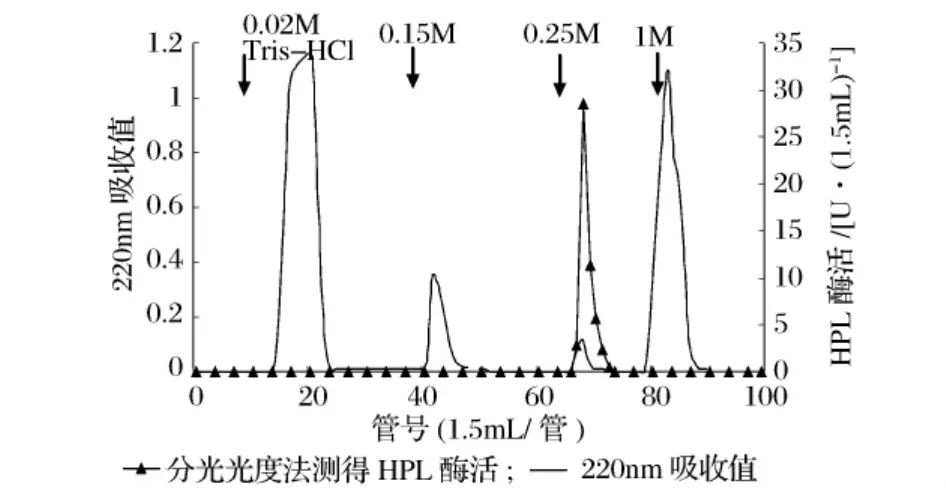
圖3 DEAE-Toyopearl離子交換柱層析譜圖
2.4 莧菜氫過氧化物裂解酶的SDSPAGE
由圖4可知,經過一系列過程的純化,得到電泳純的HPL,在SDSPAGE圖譜上基本為單一條帶條帶,分子質量約為 55ku,與報道一致[9-10]。
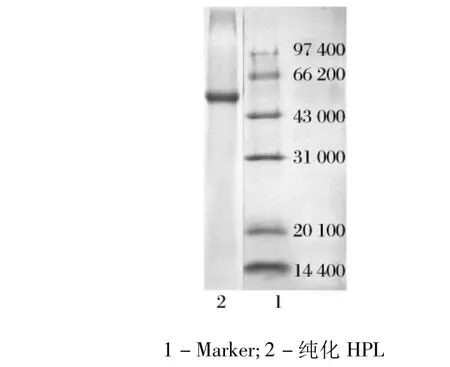
圖4 莧菜氫過氧化物裂解酶的SDS-PAGE
2.5 莧菜氫過氧化物裂解酶最適溫度及熱穩定性
由圖5可以看出,莧菜HPL的合適反應溫度為20~35℃,反應最適溫度為25℃。
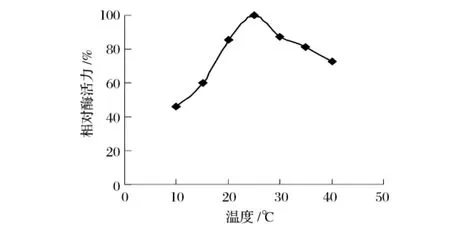
圖5 莧菜氫過氧化物的最適溫度
由圖6可知,在10~45℃加熱10 min,莧菜HPL活性能維持在80%以上,而高于45℃,隨溫度的上升,酶活迅速下降,在55℃保溫10 min后酶活基本完全喪失。可見HPL對溫度敏感,稍高的溫度就有可能使酶失活。因此,游離酶的利用和處理都應盡量在常溫下操作,以便保持較高的酶活。
3 結論
本課題組選取幾種常見植物為原料,比較篩選出莧菜作為氫過氧化物裂解酶的提取原料。并對其進行部分純化和性質研究。結果表明,莧菜中富含氫過氧化物裂解酶,其分子量大約為55 ku,最適pH6.0,最適溫度25℃,在常溫下酶能保持較高水平的活力。
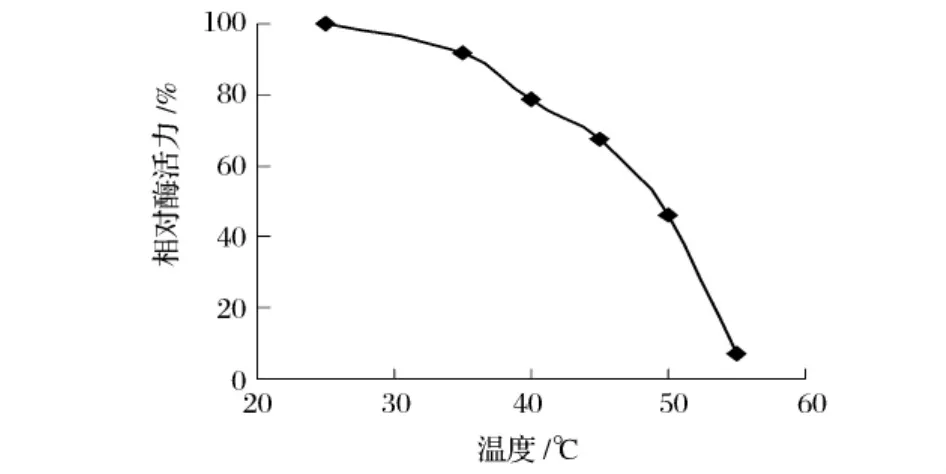
圖6 莧菜氫過氧化物裂解酶的熱穩定性
[1] Noordermeer M A,Gerrit A Veldink,Vliegenthart J F G.Fatty acid hydroperoxide lyase:a plant cytochrome P450 enzyme involved inwound healing and pest resistance[J].Chembiochemistry,2001,2:494 - 504.
[2] Noordermeer M A,Dijken A J H V,Smeekens SCM,et al.Characterization of three cloned and expressed hydroperoxide lyase isoenzymes from alfalfa with unusual N-terminal sequences and different enzyme kinetics[J].FEBS Lett,2000,267:2 473 -2 482.
[3] Hill H D,Straka J G.Protein determination using bicinchoninic acid in the presence of sulfhydryl reagents[J].Analytical Biochemistry 1988,170:203-208.
[4] Laemmli U K.Cleavage of structural proteins during the assembly of the head of bacteriophage T4[J].Nature,1970,227:680-685.
[5] Kim I S,Grosch W.Partial purification and properties of a hydroperoxide lyase from fruits of pear[J].Journal of agrictual and Food Chemistry,1981,29:1 220-1 225.
[6] Shibata Y,Matsui K,Kajiwara T,et al.Purification and properties of fatty acid hydroperoxide lyase from green bell pepper fruits[J].Plant physiology,1995,36:147 -156.
[7] Olias J M,Rios J J,Valle M,et al.Fatty acid hydroperoxide lyase in germinating soybean seedlings[J].Journal of Agrictual and Food Chemistry,1991,38:624-630.
[8] Fernando T,Bean G.Fatty acids and sterols of Amarantus tricolor L[J].Food Chemistry,1984,15:233 -237.
[9] Hornostaj A R,Robinson D S,Hornostaj A R,et al.Purification of hydroperoxide lyase from cucumbers[J].Food Chemistry,1999,66:173-180.
[10] Fauconnier M L,Perez A G,Sanz C,et al.Purification and characterization of tomato leaf(Lycopersicon esculentum Mill.)hydroperoxide lyase[J].Journal of Agrictual and Food Chemistry,1997,45:4 232-4 236.
Screen and Purification of Hydroperoxide Lyase
Long Zhen ,Ruan Qi-Jun,Kong Xiang-zhen,Zhang Cai-meng,Hua Yu-fei,Jiang Bo
(State key Laboratory of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Amaranthus tricolor leaves were identified as a particularly rich source of HPL activity.Hydroperoxide lyase(HPL)was purified to electrophoretic homogeneity from high speed centrifigation,solubilized by Tritron X-100,ammonium sulfate precipitation,hydroxypatite chromatography and DEAE Toyopearl chromatography.The purified HPL preparation consisted of a single band with a molecular mass of about 55 ku in SDSPAGE.The HPL showed higher activity against 13-hydroperoxy-linolenic acid compared to 13-hydroxy-linoleic acid.Maximum HPL activity was observed at pH 6.0 and 25℃,and room temperature sustains high enzyme activity.
hydroperoxide lyase,amaranth tricolor,purification,characteristics
在讀博士(華欲飛教授為通訊作者)。
*國家863計劃基金((2008AA10Z305);中央高校基本科研業務費專項資金資助(JUSRP10919)。
2010-08-05,改回日期:2010-11-15

