甲醇在FeS2(100)完整表面的吸附和分解
杜玉棟 趙偉娜 郭 欣 章永凡 陳文凱,*
(1福州大學化學系,福州350108; 2華中科技大學煤燃燒國家重點實驗室,武漢410074)
甲醇在FeS2(100)完整表面的吸附和分解
杜玉棟1趙偉娜1郭 欣2章永凡1陳文凱1,*
(1福州大學化學系,福州350108;2華中科技大學煤燃燒國家重點實驗室,武漢410074)
采用基于第一性原理的密度泛函理論結合周期平板模型方法,研究了甲醇分子在FeS2(100)完整表面的吸附與解離.通過比較不同吸附位置的吸附能和構型參數發現:表面Fe位為有利吸附位,甲醇分子通過氧原子吸附在表面Fe位,吸附后甲醇分子中的C―O鍵和O―H鍵都有伸長,振動頻率發生紅移;甲醇分子易于解離成甲氧基CH3O和H,表面Fe位仍然是二者有利吸附位.通過計算得出甲醇在FeS2(100)表面解離吸附的可能機理:甲醇分子首先發生O―H鍵的斷裂,生成甲氧基中間體,繼而甲氧基C―H鍵斷裂,得到最后產物HCHO和H2.
密度泛函理論;甲醇;FeS2(100)表面;吸附;過渡態
1 引言
礦物質表面在腐蝕、風化,重金屬吸附及催化過程中具有重要的作用.二硫化亞鐵作為地球表面最豐富的硫礦物之一,其表面活性涉及到廢水處理,煤礦去硫等眾多領域.作為吸附劑,它對海底沉淀物中微量元素的循環起到一定作用.1煤炭燃燒過程中,由于FeS2的存在會產生大量的SO2等有毒氣體.人們研究用泡沫浮選技術除去煤炭中的FeS2,王淀佐等人2做了硫化礦的氧化與浮選機理的量子化學研究.有機小分子作為表面活性劑能夠促進FeS2與煤炭的分離,3-5表面活性劑與FeS2表面的相互作用是表面活性劑的官能團與FeS2表面的化學吸附作用.此外,硫鐵礦的氧化分解所產生的硫化物及有毒重金屬會給地球帶來巨大的環境污染,如酸性礦物質水.6-8人們通過讓其吸附惰性官能團,如有機酸磷酸鹽等來減少其氧化分解的速率.3,9其次FeS2的禁帶寬度合適(0.95 eV),光吸收系數高(當波長λ<1 μm時,吸收系數α>105cm-1),可制作極薄的太陽能薄膜電池,被認為是一種極具發展潛力的太陽能電池材料.10
人們利用X射線光電子能譜(XPS),11-17掃描隧道顯微鏡(STM)18以及密度泛函理論(DFT)19-26研究了FeS2的電子結構,表面性質以及小分子在其表面的吸附機理.結果發現,FeS2(100)表面為其最穩定的表面,基本不發生弛豫與重構.Guevremont等18利用光電子吸附氙(PAX),程序升溫脫附(TPD)及電子能量損失能譜(EELS)研究了H2O分子及甲醇分子在FeS2(100)表面的吸附與解離,結果發現,甲醇解離后有O原子與表面Fe成鍵.
本文通過密度泛函理論結合周期平板模型,研究了甲醇分子在FeS2(100)表面的吸附方式、相互作用機理及解離可能過程,從而為理解FeS2(100)表面與界面奠定基礎.
2 理論模型和計算方法
2.1 理論模型
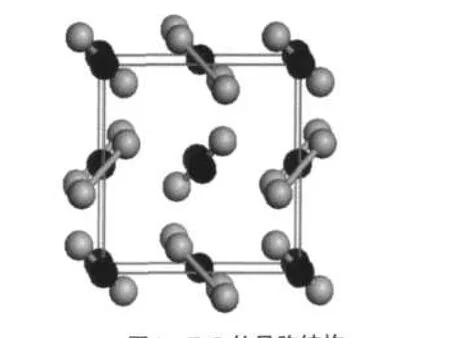
圖1 FeS2的晶胞結構Fig.1 Unit cell of the pyrite structureGrey and black spheres represent S and Fe atoms,respectively.
FeS2結構類似于NaCl晶體結構,晶胞參數a= 0.5416 nm,27Fe原子位于單胞的角頂和面心,啞鈴型的S原子對位于立方體單胞的12條棱上.由于單胞中啞鈴狀的S原子具有不同的或相反的取向,使其對稱性從NaCl的面心立方Fm3m空間群變為Pa3空間群.具體構型如圖1所示.
本文采用如圖2所示的(2×2)超晶胞9層平板模型來模擬FeS2(100)表面.體相Fe原子和S原子分別為六配位和四配位,而表面Fe原子和S原子分別為五配位和三配位.計算時超晶胞表面三層原子放開自由度,下面六層固定.應用此模型成功計算了CO在其表面的吸附.28
2.2 計算方法
采用廣義梯度密度泛函理論29和周期平板模型方法30模擬甲醇在FeS2(100)面的吸附和解離.所有的計算均由Dmol3軟件包31,32實現.計算采用PBE泛函,Fe原子和S原子內層電子由有效核電勢(ECP)代替,C、H和O采用全電子基組.價電子波函數采用雙數值基加極化函數(DNP)展開,計算過程精度設為精細,優化收斂精度取程序內定值.相鄰兩層平板間的真空層厚度為1.2 nm.以確保平板間相互作用足夠小.過渡態搜索采用Dmol3程序包中的com-plete LST/QST方法.采用相同方法優化氣相的甲醇,構型參數分別為:dC-O=0.1447 nm,dC-H=0.1100 nm,dO-H=0.0989 nm,θHCH=109.5°,θCOH=109.1°分別與實驗值0.1425 nm、0.1094 nm、0.0945 nm、108.6°和108.5°33相符合.
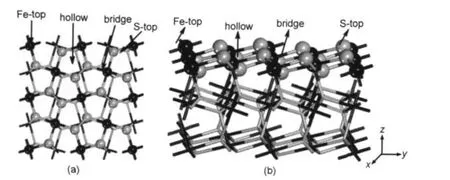
圖2 超晶胞模型的俯視圖(a)和側視圖(b)Fig.2 Top view(a)and side view(b)for the slab model
吸附能定義為吸附前后各物質總能量的變化: Eads=Emethanol+Esubstrate-Eadsorptionsystem,其中Emethnaol和Esubstrate分別表示吸附前甲醇分子和底物的能量,Eadsorptionsystem表示吸附后體系的總能量.
3 結果和討論
3.1 甲醇在FeS2(100)表面的吸附
3.1.1 吸附構型和吸附能
根據FeS2(100)表面和甲醇分子的結構,甲醇分子分別以C―O鍵垂直和平行兩種取向吸附.在FeS2(100)面選擇Fe-top、S-top、bridge和hollow共四種吸附位,如圖2所示.其中Fe-top和S-top吸附模式是指吸附分子分別以兩種取向位于表面Fe和S原子的上方,吸附分子位于Fe―S鍵上方的吸附模式稱為bridge,位于Fe―S形成穴位上方的稱為hollow模式.本文用Vert-和Para-分別表示C―O鍵垂直和平行吸附于表面.
構型優化后,發現所有不同吸附位的構型共轉化為兩種構型,如圖3所示.其中穩定構型為Vert-Fe-top(圖3(a)),另一種為不穩定構型Para-top (圖3(b)),吸附分子懸于底物上方.在穩定構型中,甲醇分子以C―O鍵傾斜吸附于表面,通過O原子與底物表面Fe成鍵,與實驗結果18一致.Eads=69.3 kJ· mol-1,略高于實驗值(46.2 kJ·mol-1),34屬于弱的化學吸附.具體的構型參數列于表1,由于Vert-Fe-top為最穩定構型,表中只列出其構型參數.由表可見,甲醇吸附后整個分子結構的變化不大,C―O鍵由0.1425 nm伸長到0.1447 nm,O―H鍵伸長了0.0044 nm,C―H鍵只伸長了0.0006 nm,角度θCOH增大了1.6°左右.由此可見,甲醇與FeS2(100)表面之間的相互作用很弱.
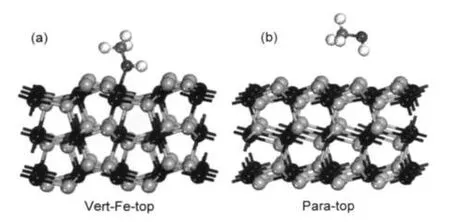
圖3 甲醇分子在FeS2(100)面的兩種吸附構型Fig.3 Two adsorption structures of methanol on FeS2(100)surface

表1 甲醇在FeS2(100)面吸附的吸附能和幾何構型參數Table 1 Adsorption energy and geometrical parameters for methanol adsorbed on FeS2(100)surface
3.1.2 Mulliken電荷布居和軌道分析
甲醇在FeS2(100)表面吸附后的Mulliken電荷布居列于表2,吸附后甲醇帶正電荷.C原子吸附后2s和2p軌道得電子,O原子2s和2p軌道失電子,H原子失電子;吸附位的Fe2+的4s和4p軌道得電子, 3d軌道失去0.04個電子,凈結果為甲醇通過O原子把電子轉移給底物.由此可見:H原子轉移電子給C原子,C原子又把電子部分轉移給O原子,O原子把得到的電子轉移給Fe2+.結果與甲醇分子在Cu(111)35及Pt-Fe(111)/C36表面吸附過程相似.
在甲醇分子中,C和O都采取sp3雜化,O原子帶有兩對孤電子.甲醇分子的HOMO是n軌道,處于全充滿狀態,其主要成分來自于O原子的孤對電子;LUMO是σ*軌道,能量較高,無法從表面接受電子.37甲醇主要通過O原子的孤對電子與底物作用.表面五配位的Fe原子最高占據軌道主要是eg軌道,最低空軌道也包含eg軌道.38由于甲醇分子中O的p軌道與底物的Fe原子的eg軌道不相匹配,相互之間成鍵能力較弱,所以甲醇與底物之間的作用不強,吸附能不高,為弱的化學吸附.
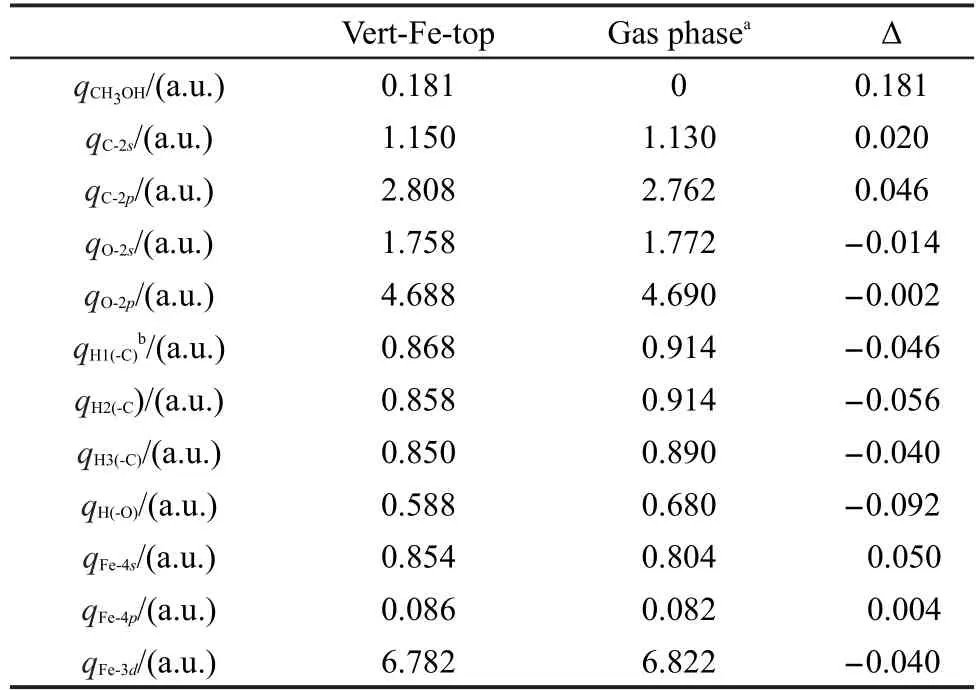
表2 甲醇各原子和Fe2+吸附前后的軌道電荷布居Table 2 Orbital charge populations for atoms of methanol and Fe2+before and after adsorption

表3 甲醇吸附前后振動頻率的實驗值與計算值Table 3 Experimental and calculated vibrational frequencies for free and adsorbed methanol
3.1.3 紅外振動頻率分析
本文還計算了甲醇分子吸附前后的振動頻率,并與實驗值39一起列于表3.由表可見,吸附后C―O和O―H鍵振動頻率降低,發生紅移,尤其是νO―H降低最多,從3723紅移至3337 cm-1,說明O―H鍵活化程度高.由此可預測,甲醇分子的解離途徑是斷裂O―H鍵,生成甲氧基(CH3O―)中間體.
3.2 甲氧基在FeS2(100)表面的吸附
3.2.1 吸附能與吸附構型
同樣考慮甲氧基分別以C―O鍵垂直和平行方式吸附于FeS2(100)表面的四個吸附位,計算后發現CH3O―吸附后都轉化為同一種構型.即甲氧基以C―O鍵傾斜吸附于表面,通過O原子與表面Fe成鍵,構型如圖4所示.吸附能Eads=151.5 kJ·mol-1,可見甲氧基與底物發生較強的相互作用.
具體構型參數和實驗值40列于表4,由于吸附后轉化為同一種構型,表中只列出Vert-Fe-top構型參數.由表可見C―O鍵鍵長伸長比較明顯,由0.1344 nm伸長到0.1394 nm,C―H鍵鍵長基本沒有變化,角度θCOH有所擴大.O原子與Fe2+形成的O―Fe鍵長為0.1883 nm,小于甲醇與底物形成的O―Fe鍵長0.2122 nm,再次表明了甲氧基與底物的相互作用較強.
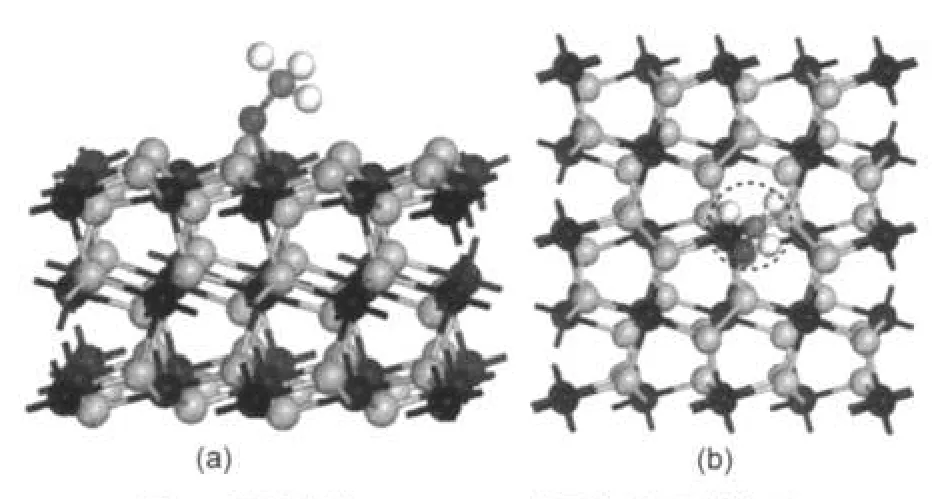
圖4 甲氧基在FeS2(100)表面穩定吸附構型的側視圖(a)和俯視圖(b)Fig.4 Side view(a)and top view(b)of stable structure of CH3O―adsorbed on FeS2(100)surface

表4 甲氧基在FeS2(100)面吸附的吸附能和幾何構型參數Table 4 Adsorption energy and geometrical parameters for methoxy adsorbed on FeS2(100)surface
3.2.2 Mulliken電荷布居和軌道分析
表5給出了甲氧基各原子和Fe2+的軌道電荷布居,由表可見,甲氧基吸附后帶負電荷,體系的電子由底物轉移到吸附質.在吸附過程中,O原子與Fe2+成鍵,Fe2+3d電子轉移到電負性較強的O原子的2p軌道,因此吸附后甲氧基得電子.由吸附體系的分子軌道圖也可以看出,甲氧基主要通過氧原子與底物作用,圖5給出了甲氧基自由態和吸附后體系的前線分子軌道.由圖可見,甲氧基的HOMO是n軌道,主要成分來自于O原子的孤對電子.在吸附體系中,O原子的2p軌道與Fe2+的3d軌道相互作用成鍵,Mulliken電荷布居分析與軌道分析結果一致.
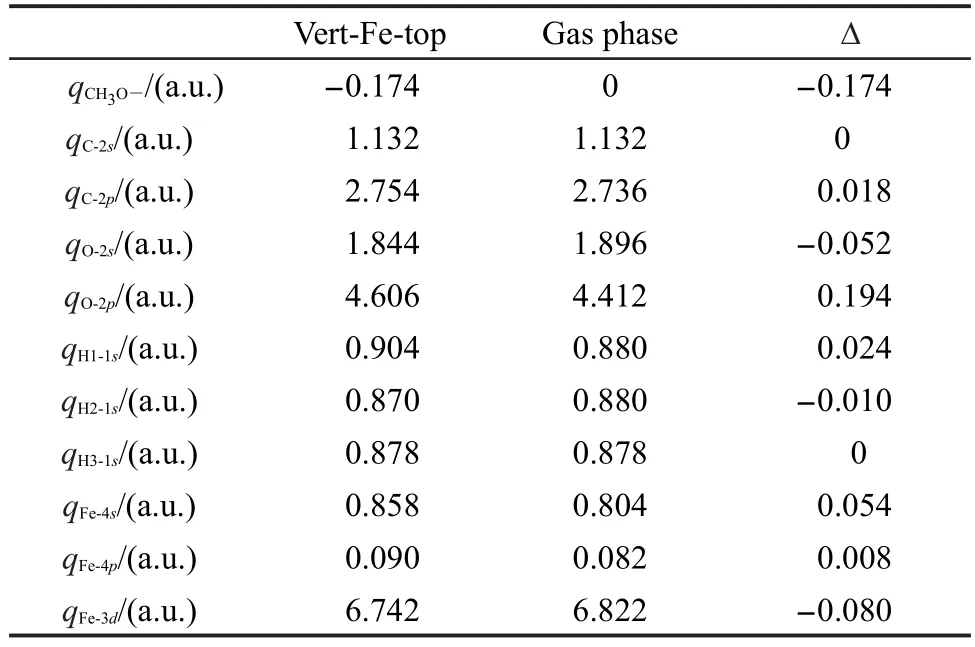
表5 甲氧基各原子和Fe2+的軌道電荷布居Table 5 Orbital populations for atoms of methoxy and Fe2+before and after adsorption
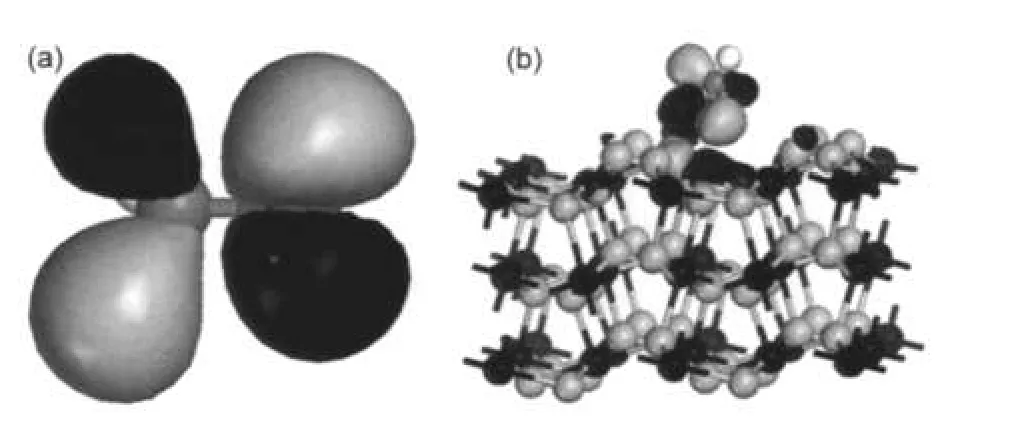
圖5 自由甲氧基(a)和吸附后吸附體系(b)的HOMO圖Fig.5 HOMOs of free CH3O―(a)and the adsorption system(b)
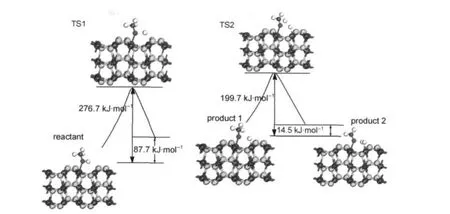
圖6 甲醇在FeS2(100)表面的可能的解離途徑示意圖Fig.6 Possible decomposition pathway of methanol on FeS2(100)surface
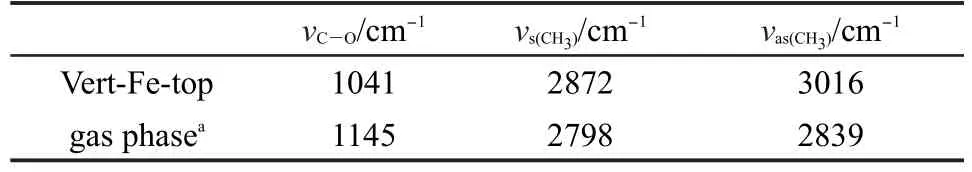
表6 甲氧基吸附前后的振動頻率Table 6 Vibrational frequencies for free and adsorbed methoxy
3.2.3 紅外振動頻率分析
本文還計算了甲氧基吸附前后的振動頻率,由表6可見,吸附后C―O鍵振動頻率降低,發生紅移,從1145 cm-1紅移至1041 cm-1,說明CH3O得電子, C―O鍵得到活化,與前面結果分析一致.CH3―的對稱反對稱伸縮振動頻率提高,發生藍移.
3.3 甲醇在FeS2(100)表面的解離吸附
本文還探討了甲醇分子在FeS2(100)面可能的解離途徑,通過前面的討論可知,甲醇以C―O鍵傾斜吸附于底物的Fe-top位,甲氧基也是如此.我們還計算了H原子在Fe(100)表面的吸附,結果是表面Fe位是H原子的穩定吸附位,吸附能為197.7 kJ· mol-1.根據文獻報道,18,41我們認為甲醇分子解離的途徑可能為:首先,甲醇分子斷裂羥基的O―H鍵,生成甲氧基和H原子分別吸附于底物表面的兩個Fe2+;其次,甲氧基斷裂一個C―H鍵,生成甲醛和H原子,而兩個H原子結合成氫氣吸附于Fe2+.計算采用complete LST/QST的方法尋找過渡態,計算方法以及其他參數均與前面構型優化時相同.解離的起點(反應物reactant)取甲醇吸附后的穩定構型Vert-Fe-top,經歷過渡態(TS1),得到第一步解離產物甲氧基和H原子(product 1);進一步搜索第二步的過渡態(TS2),得到主要產物HCHO和H2(product 2),如圖6所示.
在解離吸附過程中,甲醇的羥基H―O鍵先斷裂,生成產物甲氧基和氫原子.搜索到過渡態中的氫氧之間的距離由分子時的0.0989 nm增加到0.2017 nm,隨著羥基的斷裂以及Fe―H鍵和Fe―O鍵的形成,該反應能壘為276.7 kJ·mol-1,小于在氣相中斷裂羥基所需要的能量(430 kJ·mol-1).由此說明在FeS2(100)表面甲醇更容易解離,FeS2對甲醇的解離起到了一定的催化作用.該反應屬于吸熱反應,反應熱需要87.7 kJ·mol-1.形成的Fe―O鍵鍵長為0.1879 nm,比Fe原子與O原子的半徑和0.1940 nm短,說明甲氧基的O原子與Fe2+之間產生了強烈的化學作用.而Fe―H鍵鍵長為0.1521 nm,與Fe原子和H原子的半徑和0.1490 nm非常接近,表明H與Fe2+之間也形成了化學鍵,兩者的相互作用也較強.
甲醇進一步解離,最后產物為HCHO和H2.該解離反應的能壘為199.7 kJ·mol-1,反應需要吸熱14.5 kJ·mol-1.說明O―H鍵的斷裂需要較大的能量,由此可見甲醇在FeS2表面解離中第一步解離為速控步驟,從而為理解煤礦中FeS2的分離及抑制FeS2的氧化提供理論基礎..
4 結論
本文采用密度泛函理論結合周期平板模型的方法,計算了甲醇在(2×2)超晶胞九層平板模型FeS2(100)面的吸附,并探究了甲醇可能的解離途徑.甲醇以及解離產物甲氧基、氫原子和甲醛均傾向于吸附在Fe-top位,甲醇與甲氧基的吸附能分別為69.3和151.5 kJ·mol-1.在吸附過程中,甲醇分子的構型發生變化,C―O鍵與O―H鍵的鍵長均有不同程度的伸長,C―H鍵的鍵長變化較小.
Mulliken電荷布居分析揭示吸附過程中電子由甲醇轉移到FeS2(100)面,而紅外振動頻率的計算表明C―O和O―H鍵振動頻率發生紅移,特別是O―H的活化程度更高.過渡態的計算發現甲醇在FeS2(100)表面解離過程中,生成甲氧基中間體時需要反應能壘較高,為反應的決速步驟,并最終生成甲醛和氫氣,從而為理解FeS2(100)表面與界面提供理論基礎.
(1) Brown,J.R.;Bancroft,G.M.;Fyfe,W.S.;Mclean,R.A.N. Environ.Sci.Technol.1979,13(9),1142.
(2)Wang,D.Z.;Long,X.Y.;Sun,S.Y.Chin.J.Nonfer.Metals 1991,1(1):15.[王淀佐,龍翔云,孫水裕.中國有色金屬學報,1991,1(1),15.]
(3) Lalvani,S.B.;DeNeve,B.A.;Weston,A.Corrosion Sci.1991, 47(1),55.
(4) Ogunsola,O.M.;Osseo-Assare,K.Fuel 1987,66(4),467.
(5) Olson,T.J.;Aplan,F.F.Processing and Utilization of High Sulfur Coal;Chug,Y.P.,Cauldle,R.D.Eds.;Elsevier: Amsterdam,1987;p 71.
(6) Singer,P.C.;Stumm,W.Science 1970,167(1),1121.
(7) Lowson,R.T.Chem.Rev.1982,82(5),461.
(8) Nordstrom,D.K.SSSA Special Publication 1982,10(5),37.
(9) Huang,X.;Evangelou,V.P.Environmental Geochemistry of Sulfide Oxidation,ACS Symp.Ser.550,1994;Alpers,C.N., Blowes,D.W.Eds.;Oxford University Press:New York; Chapter 34,p 562.
(10) Ennaoui,A.;Fiechter,S.;Jaegermann,W.;Tributsch,H. J.Electrochem.Soc.1986,133(1),97.
(11) Nesbitt1,H.W.;Scaini,M.;H?chst,H.;Bancroft,G.M.; Schaufuss,A.G.;Szargan,R.Am.Mineral.2000,85(5-6),850.
(12) Uhlig,I.;Szargan,R.;Nesbitt,H.W.;Laajalehto,K.Appl.Surf. Sci.2001,179,222.
(13) Descostes,M.;Mercier,F.;Beaucaire,C.;Zuddas,P.;Trocellier, P.Nucl.Instru.Meth Phys.Res.B 2001,181(1-4),603.
(14) Mattila,S.;Leiro,J.A.;Laajalehto,K.Appl.Surf.Sci.2003, 212,97.
(15) Leiro,J.A.;Mattila,S.S.;Laajalehto,K.Surf.Sci.2003,547 (1-2),157.
(16) Mattila,S.;Leiro,J.A.;Heinonen,M.Surf.Sci.2004,566-568, 1097.
(17) Kim,E.J.;Batchelor,B.Environ.Sci.Technol.2009,43(8), 2899.
(18) Guevremont,J.M.;Strongin,D.R.M.;Schoonen,A.A.Surf. Sci.1997,391(1-3),109.
(19) Stirling,A.;Bernasconi,M.;Parrinello,M.J.Chem.Phys. 2003,118(19),8917.
(20) Stirling,A.;Bernasconi,M.;Parrinello,M.J.Chem.Phys. 2003,119(9),4934.
(21) Boehme,C.;Marx,D.J.Am.Chem.Soc.2003,125(44),13362.
(22)Sun,W.;Hu,Y.H.;Qiu,G.Z.;Qin,W.Q.J.Cent.South Univ. Technol.2004,11(4),386. [孫 偉,胡岳華,邱冠周,覃文慶.中南工業大學學報,2004,11(4),386.]
(23)Von Oertzen,G.U.;Skinner,W.M.;Nesbitt,H.W.Phys.Rev.B 2005,72(23),235427.
(24) Nair,N.N.;Schreiner,E.;Marx,D.J.Am.Chem.Soc.2006, 128(42),13815.
(25) Li,Q.;Qin,W.Q.;Sun,W.;Qiu,G.Z.J.Cent.South Univ. Technol.2007,14(5),618.[黎 全,覃文慶,孫 偉,邱冠周.中南工業大學學報,2007,14(5),618.]
(26) Blanchard,M.;Wright,K.;Gale,J.D.;Catlow,C.R.A.J.Phys. Chem.C 2007,111(30),11390.
(27) Kleppe,A.K.;Jephcoat,A.P.Mineralogical Magazine 2004,68 (3),433.
(28)Du,Y.D.;Chen,W.K.;Zhang,Y.F.;Guo,X.J.Nat.Gas Chem. 2011,20(1),60.
(29) Parr,R.G.;Yang,W.Density Functional Theory of Atoms and Molecules;Oxford University Press:New York,1989;p 1.
(30) Cao,M.J.;Chen,W.K.;Liu,S.H.;Xu,Y.;Li,J.Q.Acta Phys.-Chim.Sin.2006,22(1),11. [曹梅娟,陳文凱,劉書紅,許 瑩,李俊籛.物理化學學報,2006,22(1),11.]
(31) Delley,B.J.Chem.Phys.1990,92(1),508.
(32) Delley,B.J.Chem.Phys.2000,113(18),7756.
(33) Lide,D.R.CRC Handbook of Chemistry and Physics.84th ed; CRC Press:Boca Raton,2003-2004;pp 9-34.
(34) Redhead,P.A.Vacuum 1962,12(4),203.
(35)Chen,W.K.;Liu,S.H.;Cao,M.J.;Lu,C.H.;Xu,Y.;Li,J.Q. Chin.J.Chem.2006,24(7),872.
(36)Wang,Y.W.;Li,L.C.;Tian,A.M.Acta Chim.Sin.2008,66 (22),2457.[王譯偉,李來才,田安民.化學學報,2008,66 (22),2457.]
(37) Jiang,S.Y.;Teng,B.T.;Lu,J.Q.;Liu,X.S.;Yang,P.F.;Yang, F.Y.;Luo,M.F.Acta Phys.-Chim.Sin.2008,24(11),2025. [蔣仕宇,滕波濤,魯繼青,劉雪松,楊培芳,楊飛勇,羅孟飛.物理化學學報,2008,24(11),2025.]
(38) Rosso,K.M.;Becker,U.;Hochella,M.F.Am.Mineral.1999, 84(10),1535.
(39) Herzberg,G.Molecular Spectra and Molecular Structure ??. Infrared and Raman Spectra of Polyatomic Molecules;D.Van Nostrand Company:New York,1945;p 335.
(40) Jackels,C.F.J.Chem.Phys.1982,76(1),505.
(41) Lu,J.P.;Albert,M.;Bernasek,S.L.Surf.Sci.1990,239(1-2), 49.
December 15,2010;Revised:March 6,2011;Published on Web:March 24,2011.
Adsorption and Dissociation of Methanol on Perfect FeS2(100)Surface
DU Yu-Dong1ZHAO Wei-Na1GUO Xin2ZHANG Yong-Fan1CHEN Wen-Kai1,*
(1Department of Chemistry,Fuzhou University,Fuzhou 350108,P.R.China;
2State Key Laboratory of Coal Combustion,Huazhong University of Science and Technology,Wuhan 410074,P.R.China)
First-principles calculations based on density functional theory(DFT)and the periodical slab model were used to study the adsorption and dissociation of methanol on the perfect FeS2(100)surface. The adsorption energy and the geometric parameters on the different adsorption sites showed that the Fe site was the most favorable adsorption site and O atoms were found to bind to Fe atoms.After adsorption, the C―O and O―H bonds of methanol were elongated and the vibrational stretch frequency was red shifted.The calculation results proved that methanol was prone to decomposition resulting in methoxy groups and hydrogen.We calculated the adsorption behavior of these methoxy groups and hydrogen on the FeS2(100)surface and found that the Fe sites were also the most favorable adsorption sites.A possible decomposition pathway was investigated using transition state searching methods:first the O―H bond of methanol was decomposed producing the intermediate methoxy group and subsequently the C―H bond of the methoxy group was broken resulting in final products of formaldehyde and hydrogen.
Density functional theory;Methanol;FeS2(100)surface;Adsorption;Transition state
O641
?Corresponding author.Email:qc2008@fzu.edu.cn;Tel:+86-591-22866162.
The project was supported by the National Natural Science Foundation of China(90922022),State Key Laboratory of Coal Combustion Foundation of Huazhong University of Science and Technology,China(FSKLCC0814),and New Century Excellent Talents Program in University of Fujian Province,China(HX2006-103).
國家自然科學基金(90922022),華中科技大學煤燃燒國家重點實驗室基金(FSKLCC0814)和福建省高等學校新世紀優秀人才計劃(HX2006-103)資助項目

