殼聚糖抗壞血酸鹽的制備及其抗氧化性的研究
劉靜娜,莊遠紅,耿微微
(漳州師范學院生物科學與技術系,福建漳州363000)
殼聚糖抗壞血酸鹽的制備及其抗氧化性的研究
劉靜娜,莊遠紅,耿微微
(漳州師范學院生物科學與技術系,福建漳州363000)
制備了殼聚糖抗壞血酸復合鹽,并研究了抗氧化性。以殼聚糖和抗壞血酸為原料制備了復合鹽,對其結構進行了表征,并測定了其溶解性、穩定性、抗氧化性等性質。對原料配比、反應溫度和反應時間進行探討,發現最優工藝條件為原料配比為1∶6、溫度為25℃、時間為120min,在此條件下制得的復合鹽有較好水溶性,在溶液中的穩定性優于抗壞血酸,清除羥基自由基的能力優于殼聚糖,從紅外光譜圖上可看出抗壞血酸結合于殼聚糖的氨基上。該復合鹽的制備改善了其原料的性質,有利于進一步的應用。
殼聚糖,抗壞血酸,抗氧化
殼聚糖(Chitosan)是由甲殼素(Chitin)經過脫乙酰化得到的聚氨基葡萄糖,具有良好的生物相容性、安全性,有多種生物活性,在食品、化工、醫藥及生物醫學工程等諸多領域的應用研究取得了重大進展[1]。近年來的研究發現,殼聚糖還是一種良好的抗氧化劑,在體外和體內實驗中,殼聚糖都表現出良好的對自由基的清除作用、提高體內抗氧化酶的活性等作用[2-5]。但殼聚糖不能直接溶于水中,也不溶于一般的有機溶劑,只能溶于酸性溶液中,這在很大程度上限制了它的應用[6]。殼聚糖大分子上分布著許多活潑的羥基、氨基,可以通過化學改性改善殼聚糖的溶解性能,進而提高其功能活性[7]。維生素C(vitamin C),又名L-抗壞血酸(L-ascorbic acid),是含有6個碳原子的酸性多羥基化合物,也是一種人體必需的水溶性維生素。抗壞血酸可以提高人體的免疫力,增強人體抵抗能力,這可能與抗壞血酸是一種人體抗氧化劑有關,它可以消除人體內多余的活性氧和自由基,使人體細胞保持健康狀態[8]。殼聚糖是自然界唯一的堿性多糖,而抗壞血酸呈酸性,因此,本文制備了殼聚糖抗壞血酸復合鹽,從而改善殼聚糖不溶于水的缺點,同時殼聚糖的大分子結構可以保護抗壞血酸、延緩其被空氣中的氧氣氧化。此外,還對其物化性質及抗氧化性進行了探討,為殼聚糖的進一步應用提供理論基礎,具有一定的學術意義。
1 材料與方法
1.1 材料與儀器
殼聚糖 購自浙江金殼生物有限公司,脫乙酰度90%,粘度50cP·s;L-抗壞血酸、異丙醇、無水乙醇、冰醋酸、鄰二氮菲等 均為分析純。
DHG-9070A型電熱恒溫鼓風干燥箱、DKZ-1型電熱恒溫振蕩水槽 上海精宏實驗設備有限公司;UV-754分光光度計 上海第三分析儀器廠;HH-2數顯恒溫水浴鍋 金壇市江南儀器廠;LG-D2型真空冷凍干燥機 沈陽新陽儀器設備有限公司;90-2恒溫磁力攪拌器 上海亞榮生化儀器廠。
1.2 實驗方法
1.2.1 殼聚糖抗壞血酸鹽的制備 在500mL的三口燒瓶中加入150mL異丙醇和50mL水配制異丙醇水溶液,稱取一定量的抗壞血酸并以異丙醇水溶液溶解,再加入一定量的殼聚糖,將燒瓶放入振蕩器中,在一定溫度下恒溫振蕩一定時間。反應結束后,將反應體系進行抽濾、洗滌,然后將濾餅進行真空冷凍干燥,最后得到產物。選擇反應配比(殼聚糖的-NH2和抗壞血酸的摩爾比),反應時間和反應溫度進行殼聚糖抗壞血酸鹽制備的三因素三水平正交實驗,因素水平見表1。
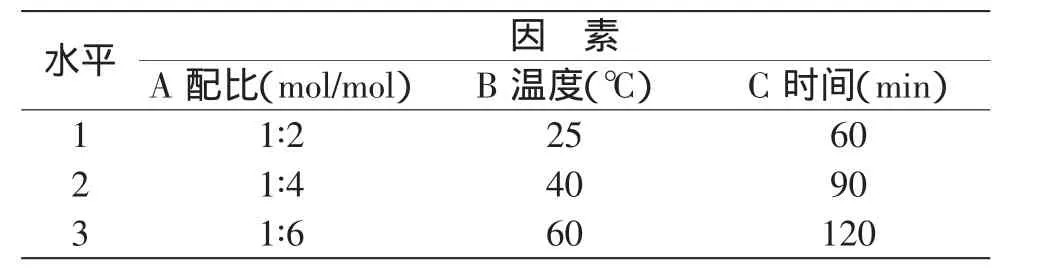
表1 制備殼聚糖抗壞血酸鹽的因素水平表
1.2.2 殼聚糖抗壞血酸鹽中有效Vc含量的測定 分別準確稱取抗壞血酸0.025、0.05、0.075、0.1、0.125g,溶于0.1mol/L的鹽酸溶液中,用紫外分光光度計在242.5nm處測其吸光度,并制作其標準曲線[9-10]。
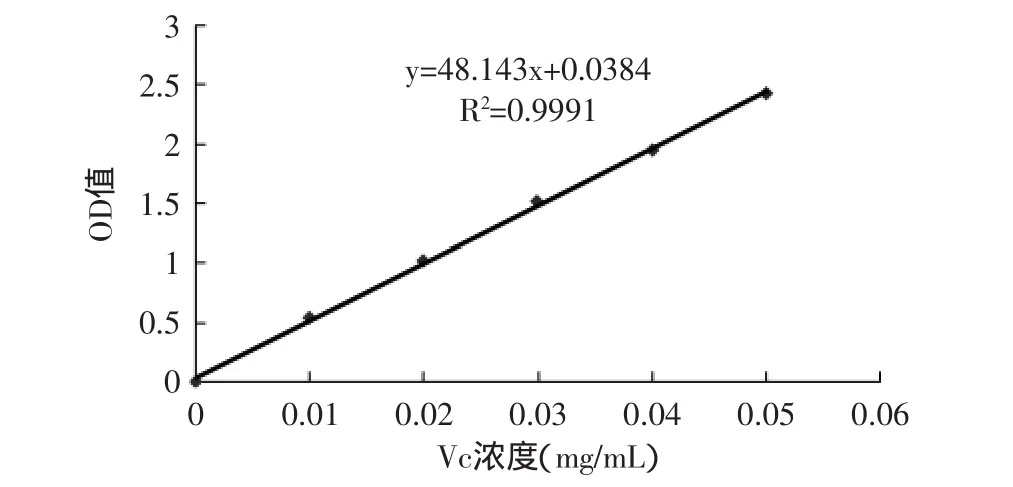
圖1 抗壞血酸含量標準曲線
取按不同因素水平制備的抗壞血酸鹽產物0.1g溶于0.1mol/L的鹽酸中,用紫外分光光度計在242.5nm處測其吸光度,計算殼聚糖抗壞血酸鹽中有效Vc含量。
1.2.3 產物結構表征 取殼聚糖原料及殼聚糖抗壞血酸鹽產物,用KBr壓片后在傅立葉紅外儀(FTIR)上進行結構分析。
1.2.4 溶解性的測定 取制得的適量(0.1g)殼聚糖抗壞血酸鹽置于試管,加10mL去離子水、HCl(1%)、乙酸(1%)、丙酮、乙醇溶劑,放入振蕩培養箱中振蕩24h,觀察其溶解現象。
1.2.5 穩定性的測定 將純L-抗壞血酸和殼聚糖抗壞血酸鹽分別溶解在pH=4.8的乙酸-乙酸鈉緩沖溶液、蒸餾水、pH=10.0的碳酸鈉-碳酸氫鈉緩沖溶液,在室溫下放置,定期測定其最大吸收波長處的吸光度值[9]。
1.2.6 對羥基自由基的清除 采用鄰二氮菲-Fe2+氧化法[11]。計算不同樣品對·OH的清除率:

式中:A樣為樣品組的吸光值;A損為損傷管的吸光值;A未損為未損傷管的吸光值。
2 結果與討論
2.1 殼聚糖抗壞血酸鹽的制備
抗壞血酸容易失去活性,在60℃以上就會分解,所以選擇比較溫和的實驗條件來制備殼聚糖抗壞血酸鹽,反應時間也不宜過長。通過反應配比、反應時間和溫度三因素的水平變化來討論其對殼聚糖抗壞血酸鹽有效Vc含量和溶解性的影響,實驗結果見表2。
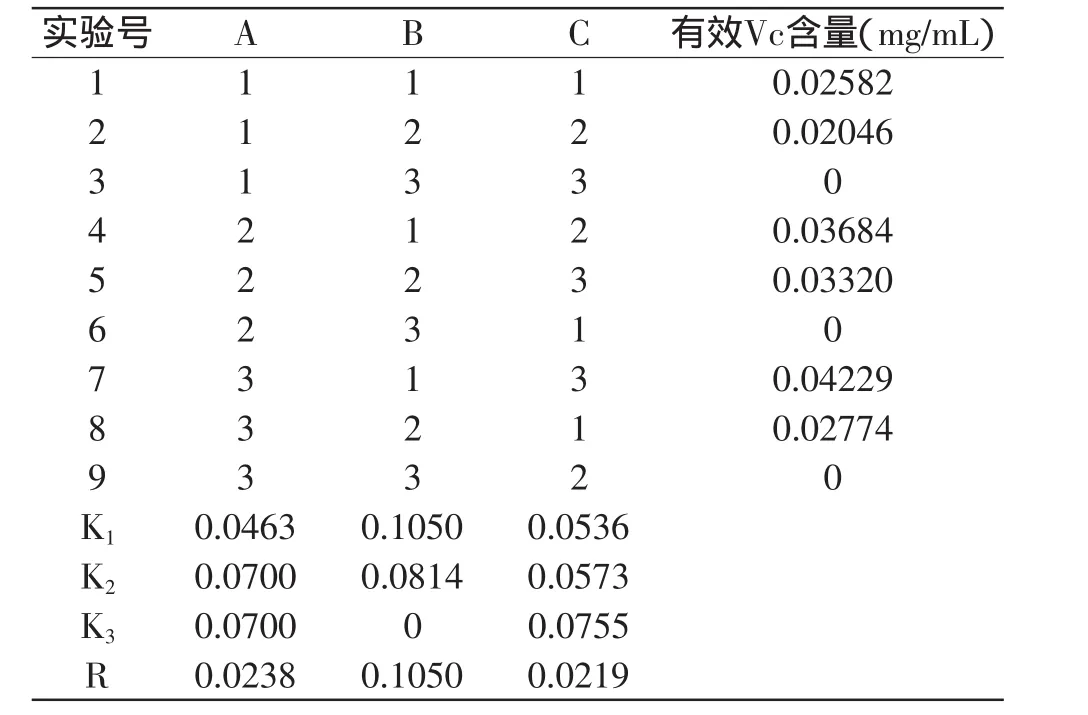
表2 殼聚糖抗壞血酸鹽制備的正交實驗結果
從表2中可以看出,反應時間延長有助于提高產物殼聚糖抗壞血酸鹽中有效Vc含量;而且抗壞血酸的濃度越大,有效Vc含量也就越大;但在一定溫度范圍內,抗壞血酸的活性會隨著溫度升高而被破壞,因此25℃時比40℃時反應得到的產物抗壞血酸含量更高。由結果分析可知,制備殼聚糖抗壞血酸鹽的最優條件組合為A2B1C3或A3B1C3,后者即為實驗7的條件組合,從表中可看出,該條件下所制得的產品中有效Vc含量最高,因此最終確定反應配比1∶6,溫度25℃,時間120min為最佳反應條件,此時反應程度最高,產物中有效Vc含量最大,而且該產物在水中可以全部溶解。由極差分析可知,對正交結果的影響為溫度>配比>時間,即溫度對殼聚糖抗壞血酸鹽的制備影響最大,配比次之,時間影響最小。
2.2 殼聚糖抗壞血酸鹽的紅外表征
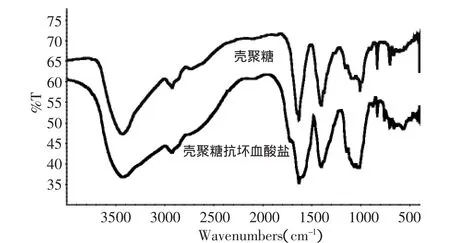
圖2 殼聚糖及殼聚糖抗壞血酸鹽的紅外光譜圖
將殼聚糖及殼聚糖抗壞血酸鹽用紅外光譜進行結構表征,結果如圖2所示。從圖中可知,經過成鹽反應后,3428cm-1處的N-H伸縮峰由原來的尖而窄變得鈍而寬,表明抗壞血酸通過殼聚糖的-NH2鍵進行結合。在殼聚糖抗壞血酸鹽的譜圖中,增加了1032cm-1和1062cm-1的峰,這是C-O伸縮振動,表明結合上了抗壞血酸分子。
2.3 殼聚糖抗壞血酸鹽的溶解性
將殼聚糖原料及產品殼聚糖抗壞血酸鹽溶解于水、鹽酸及常用有機溶劑,結果如表3所示。結果表明,殼聚糖抗壞血酸鹽在水溶液中的溶解性比殼聚糖原料提高很多,能完全溶于水;在稀鹽酸和乙酸這兩種酸性溶劑中的溶解速度也大大加快,但是在常用有機溶劑中仍然不溶解。殼聚糖抗壞血酸復合鹽的水溶性使其在食品和營養領域的應用范圍大大拓寬。

表3 殼聚糖及殼聚糖抗壞血酸鹽的溶解性
2.4 不同pH環境中殼聚糖抗壞血酸鹽的穩定性
2.4.1 純L-抗壞血酸濃度隨靜置時間的變化 將分別溶于水、乙酸鹽緩沖液、碳酸鹽緩沖液的L-抗壞血酸溶液在室溫下靜置,定時測定其最大吸收波長處的吸光度,以觀測Vc濃度隨時間的變化情況,結果如圖3所示。由圖可知,Vc在pH=10.00的碳酸鹽緩沖體系中濃度變化速度最快,平均每分鐘下降1.3%;而在水中和在pH=4.8的乙酸鹽緩沖液中吸光度值下降趨勢幾乎相同,下降速率分別約為0.5%/min和0.44%/min。
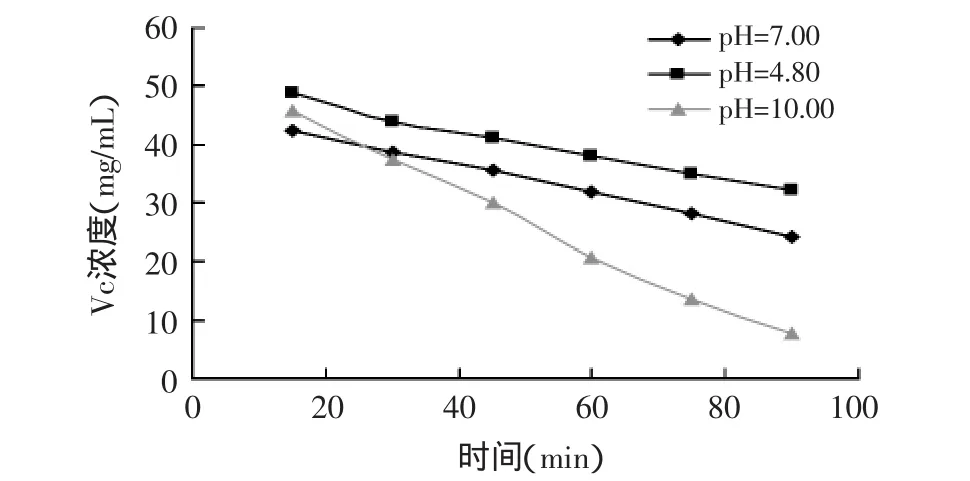
圖3 純L-抗壞血酸在不同pH下靜置時間對Vc濃度的影響
2.4.2 殼聚糖抗壞血酸鹽濃度隨靜置時間的變化 將殼聚糖抗壞血酸鹽分別溶于pH為4.8、7.0和10.0的溶液中,觀測其中有效Vc含量隨時間的變化。由圖4可以看到,殼聚糖抗壞血酸鹽在水體系中最不穩定,Vc濃度每天下降最快;而在pH=10.00的碳酸鹽緩沖體系中下降次之,在pH=4.8的乙酸鹽緩沖液中每天下降則為最慢。
圖3和圖4反映的是Vc在不同pH體系中的穩定性,純L-抗壞血酸在水中的穩定時間不超過3h,即使是在pH=4.8的乙酸鹽緩沖液中也不過數小時。而對殼聚糖抗壞血酸鹽而言,穩定性有所提高,在pH=4.8的乙酸鹽緩沖液中一周內都未觀察到明顯的分解,在水和pH=10.00的碳酸鹽緩沖體系中要完全分解也至少需要一周的時間。這是因為抗壞血酸成鹽,對酸、氧的穩定性大大提高,殼聚糖與抗壞血酸反應成鹽,保護了其抗氧化性。結果表明了殼聚糖抗壞血酸鹽穩定性明顯高于純L-抗壞血酸。
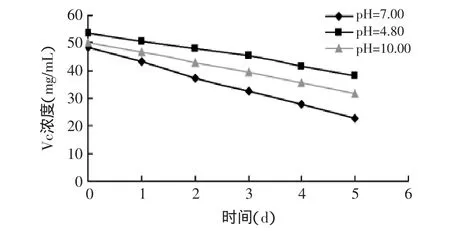
圖4 殼聚糖抗壞血酸鹽在不同pH下靜置時間對Vc濃度的影響
2.5 殼聚糖抗壞血酸鹽對羥基自由基的清除
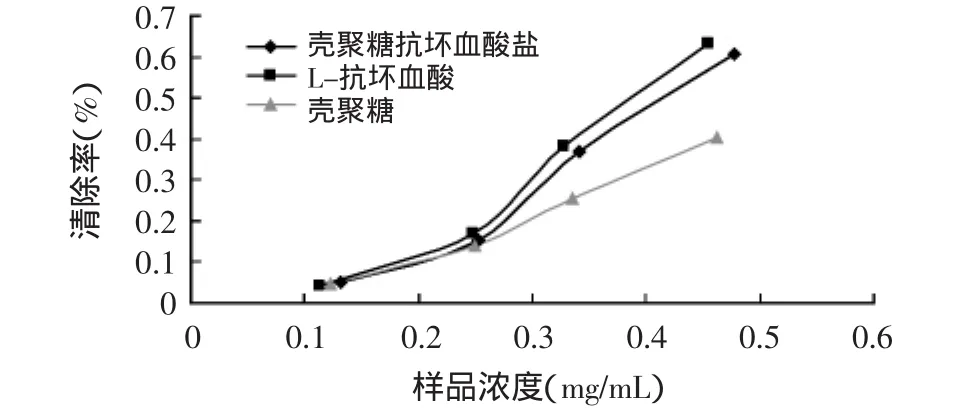
圖5 原料和產物對羥基自由基的清除效果
羥基自由基是自由基對人體造成損傷,導致人體衰老的重要原因之一,其損害作用主要體現在對生命大分子的損害。羥基自由基是已知的最強氧化劑,可以與幾乎所有的細胞成分發生反應,對機體危害極大,與衰老、腫瘤等密切相關[12]。不同濃度的殼聚糖、抗壞血酸及殼聚糖抗壞血酸鹽對羥基自由基(·OH)清除作用的結果見圖5。由圖可知,隨著濃度的升高,抗壞血酸及殼聚糖抗壞血酸鹽對羥基自由基的清除能力增強較明顯,其半抑制濃度IC50(當清除率達到50%時,所需自由基清除劑的濃度)分別為0.38、0.39mg/mL,二者之間的羥基自由基清除能力大致相同,而殼聚糖原料對羥基自由基的清除能力相對較差。由此可見殼聚糖與抗壞血酸反應成鹽后,殼聚糖起到了很好地保護抗壞血酸的載體作用,并未影響其抗氧化能力,而且增強了殼聚糖本身的抗氧化能力。
3 結論
本文利用殼聚糖在異丙醇介質中與抗壞血酸進行反應,在原料配比1∶6,溫度25℃,時間120min的最優工藝條件下,制備了水溶性較好的殼聚糖抗壞血酸鹽。對產物的結構用紅外光譜進行表征,表明抗壞血酸結合在殼聚糖的活性氨基上。對產物的物化性質進行了測定,表明產物的水溶性和對羥基自由基的清除能力都優于原料殼聚糖;穩定性優于原料抗壞血酸。該結果表明,殼聚糖與抗壞血酸結合之后,產物的性能得到了改良,將更有利于其在食品、醫藥等領域的應用,具有較高的使用價值。
[1]蔣挺大.甲殼素[M].北京:中國環境科學出版社,1999:376.
[2]Li W,Jiang X,Xue P,et al.Inhibitory effects of chitosan on superoxideanionradicalsandlipidfreeradicals[J].ChineseScience Bulletin,2002(11):887-889.
[3]Yena M T,Tsengb Y H,Lia R C,et al.Antioxidant properties of fungal chitosan from shiitake stipes[J].LWT-Food Science and Technology,2007,40(2):255-261.
[4]Jeon T,Hwang S G,Park N G,et al.Antioxidative effect of chitosan on chronic carbon tetrachloride induced hepatic injury in rats[J].Toxicology,2003,187(1):67-73.
[5]劉靜娜,張家驪,夏文水.殼聚糖降低脂質過氧化作用的研究[J].食品與生物技術學報,2010,29(6):836-841.
[6]胡章,李思東,李先文.新型殼聚糖季銨鹽衍生物的合成與表征[J].廣東海洋大學學報,2009,29(1):58-59.
[7]姚倩,孫濤,周冬香,等.殼聚糖衍生物的抗氧化性能研究進展[J].食品科技,2007(10):109-111.
[8]黎觀紅,瞿明仁,晏向華,等.Vc的營養和應用研究進展[J].糧食與飼料業,2001(4):28-32.
[9]韓穎達.新型殼聚糖/抗壞血酸復合物的制備與應用性能研究[D].天津大學,2007:20-21.
[10]袁葉飛,甄漢深,歐賢紅.分光光度法測定大棗中的維生素C含量[J].安徽中醫學院學報,2006,25(2):1-5.
[11]張敬晗,金黎明,張盼,等.殼聚糖及其衍生物清除羥自由基的能力[J].大連民族學院生命科學學院,2008,10(7): 23-24.
[12]金惠銘.病理生理學[M].上海:復旦大學出版社,2005:81-83.
Study on preparation and antioxidation of chitosan-ascorbic acid compound
LIU Jing-na,ZHUANG Yuan-hong,GENG Wei-wei
(Department of Biological Sciences and Biotechnology,Zhangzhou Normal University,Zhangzhou 363000,China)
Chitosan-ascorbic acid compound was prepared and its antioxidation was studied.The compound was prepared with chitosan and ascorbic acid,and the structure,solubility,stability and antioxidation were determined.The optimal technology was 1∶6 of material ratio,25℃ of temperature and 120min of time.The compound prepared under this condition showed better solubility and hydroxyl free radical scavenging ability than chitosan,and better stability in the solution than ascorbic acid.Infrared spectrum exhibited that ascorbic acid bound with the amino group.The product improved the ability of materials,which was good to the further application.
chitosan;ascorbic acid;antioxidation
TS201.2
A
1002-0306(2011)10-0139-04
2011-07-29
劉靜娜(1980-),女,博士,講師,主要從事生物活性物質與功能性食品的研究。
福建省青年科技人才創新項目(2009J05038);漳州師范學院博士啟動課題項目(L20812)。

