光度法研究八元瓜環與食用色素-日落黃和靛藍的相互作用
鄭利梅,王秋麗,豆超群,展海軍,陶 朱
(1.河南工業大學化學化工學院,河南鄭州 450001; 2.鄭州大學,河南鄭州 450001; 3.貴州大學應用化學研究所,貴州貴陽 550025)
光度法研究八元瓜環與食用色素-日落黃和靛藍的相互作用
鄭利梅1,王秋麗2,豆超群1,展海軍1,陶 朱3
(1.河南工業大學化學化工學院,河南鄭州 450001; 2.鄭州大學,河南鄭州 450001; 3.貴州大學應用化學研究所,貴州貴陽 550025)
利用紫外可見吸收光譜法研究了八元瓜環(Q[8])與食用色素靛藍(g2)和日落黃(g3)的相互作用情況。考察了溶液的酸度對作用體系的影響。計算了穩定常數,測定了作用體系的校正曲線。結果表明,八元瓜環與客體的相互作用隨客體及溶液pH的不同而有所改變。pH>5.3,Q[8]與日落黃(g3)能夠發生明顯的相互作用,形成作用比為2∶1的穩定配合物,而Q[8]與靛藍(g2)則在pH<10.8時,才能形成配比為1∶2的穩定配合物。這對于研究瓜環與食用色素的包結和緩釋等在食品添加劑的開發和應用方面具有重要的研究價值。
分光光度法,八元瓜環,日落黃,靛藍,相互作用
瓜環(cucurbit[n]urils n=5~8)Q[n][1-3]是超分子化學中繼冠醚、環糊精、杯芳烴之后備受矚目的一類新型籠狀大環主體分子化合物,由于瓜環具有獨特的疏水性籠體空腔,可以包合多種有機物;兩端分布的多個脲羰基可以通過離子-偶極作用或氫鍵作用來鍵合陽離子或有機分子的帶電部分,形成各種自組裝主-客體包結物、分子膠囊或超分子實體。進而改變這些物質的性能。隨著主客體化學理論的不斷完善,瓜環作為一種新型主體化合物受到了廣泛的關注,并逐漸成為超分子化學研究領域中的一個熱點[4-10]。然而相對于環糊精等前幾代超分子在生物、食品和藥物分析等方面的廣泛研究及應用而言,對于瓜環在食用色素方面的已有的研究工作僅處于起步階段。日落黃和靛藍是目前被我國食品添加劑食用衛生標準(GB2760-1996)列入的人工合成色素,合成色素由于顏色更加鮮艷,不易褪色,且價格較低,而被企業廣泛使用。目前此類色素的測定方法主要有紫外可見光譜,熒光光譜,紅外光譜,電化學方法等。本文采用分光光度法考察了八元瓜環與食用色素日落黃和靛藍相互作用的性質及影響作用的因素;測定了包結物的穩定常數;初步探討了pH的變化對作用體系的影響,并得到了較好的結果。
1 材料與方法
1.1 材料與儀器
八元瓜環(Q[8]) 貴州大學應用化學研究所提供,配制成1.00×10-4mol/L的水溶液;食用色素靛藍和日落黃 分別記為g2和g3,分析純,購自成都貝斯特試劑有限公司,配制成濃度為1.00×10-3mol/L的溶液;實驗用水 二次蒸餾水。
722型分光光度計 上海第三分析儀器廠; pHS-3C型酸度計 上海雷磁儀器廠。
1.2 實驗方法
1.2.1 光譜的測定 分別移取一定體積的g2和g3溶液于25mL的容量瓶中,加入適量Q[8]溶液,用水定容后配成具有不同主體和客體物質的量之比的系列溶液。分別采用摩爾比法和等摩爾比連續變化法測定它們之間的相互作用比。
1.2.2 pH的影響 用鹽酸和氫氧化鈉調節溶液的酸堿度,使pH在一定范圍內形成梯度,固定體系中客體的濃度,改變瓜環的加入比例配制成主客體物質的量之比分別為0∶1,0.5∶1,1∶1,2∶1等具有不同配比,不同pH的系列溶液,在客體最大吸收波長處測定體系的吸收強度。
2 結果與討論
2.1 pH對Q[8]與g2,g3相互作用體系的影響
酸度的變化對瓜環主客體相互作用的影響非常顯著,在一定范圍內pH的變化甚至可以改變主客體相互作用的模式和穩定性[11-12]。實驗考察了pH對體系吸光度及相互作用物質的量之比的影響。
配制主客體比分別為0.5∶1、1∶1、2∶1的溶液,測量在不同pH時體系吸光度的變化。圖1(a)是純客體g2及Q[8]-g2體系(0.5∶1、1∶1)在不同pH下體系吸光強度的變化。
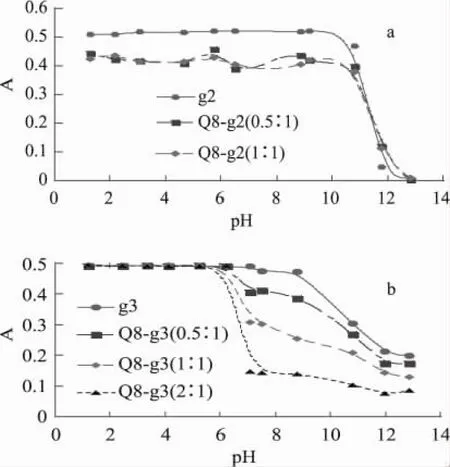
圖1 Q[8]與客體g2和g3作用體系的A~pH(a-b)關系曲線
在pH>10.8時,Q[8]與g2的三條曲線重合在一起,說明Q[8]與g2沒有發生包結配合作用,以游離的客體存在;當pH=0.5~10.8時,Q[8]-g2的吸光強度與g2明顯不同,游離客體的A-pH曲線的位置最高,主客體物質的量之比為0.5∶1體系的A-pH曲線位置最低。說明在pH=0.5~10.8的范圍內,Q[8]與客體發生了包結配合作用,并且作用比例為0.5∶1,當固定客體的量,增加Q[8],使主客體物質的量比為1∶1時,客體完全被包結,吸光度不發生變化,故兩條曲線粘合在一起,實驗結果正是如此,并且在實驗時發現此時溶液的顏色開始變綠,隨著pH的進一步升高,顏色變黃,此時客體靛藍的結構可能發生改變。對于Q[8]-g3體系,從圖1(b)可以看出,pH大約在5.3以下,Q[8]與g3的四條曲線重合在一起,說明Q[8]與g3沒有發生包結配合作用;當pH值大于5.3時,吸光強度發生明顯變化,游離客體g3的A-pH曲線的位置最高,主客體物質的量之比為2∶1混合體系的A-pH曲線位置最低,而主客體物質的量之比為0.5∶1與1∶1混合體系的A-pH曲線的位置基本上分別處于游離客體與1∶1和2∶1曲線的中間。說明在pH大于5.3時,Q[8]與客體明顯發生了包結配合作用,并且作用比例應為2∶1。
2.2 Q[8]與gn(n=2,3)相互作用的紫外-可見吸收光譜研究
控制溶液的pH=6.8,分別采用摩爾比法和等摩爾比連續變化法測定了Q[8]與g2和g3相互作用的吸收光譜(g2,λmax=612nm;g3,λmax=482nm)。在測量條件下Q[8]沒有吸收。

圖2 Q[8]與g2和g3作用體系A~NQ[8]/Ng和ΔA~NQ[8]/(NQ[8]+Ng)關系曲線圖
從圖2(a)可以看出,隨Q[8]的加入,主客體發生相互作用,吸光度均呈下降趨勢,Q[8]與g3在摩爾比達到2∶1時的吸光度降到最低,而Q[8]與g2則是摩爾比在0.5∶1降到最低,表明Q[8]與g3是按照2∶1進行包結,與g2則是按照1∶2進行包結。為了進一步證實形成包結物的主客體物質的量比,采用等摩爾連續變化法(Job法)驗證。由圖2(b)ΔA~NQ[8]/(NQ[8]+Ng)關系曲線圖我們可以看到,當Q[8]與g3約在摩爾比為0.66時ΔA出現最大值,Q[8]與g2約在0.33處出現最大值。即Q[8]與染料客體在相應處作用最為顯著。從而,我們可以推斷Q[8]與g3形成絡合物的包結比為2∶1,Q[8]與g2形成絡合物的包結比為1∶2。兩種方法所得的結果是一致的。參考測定環糊精類包結配合物的K值的計算方法[13],結合我們實驗的具體情況,利用摩爾比法測定瓜環與食用色素g2、g3形成的包結配合物的穩定常數分別為∶KQ[8]-g2=2.02×109(L2/mol2),KQ[8]-g3=1.98 ×1010(L2/mol2)。
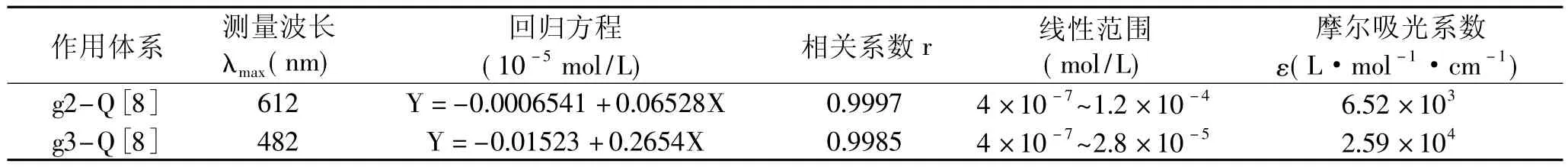
表1 標準曲線的相關參數
2.3 標準曲線
在上述Q[8]-g溶液體系中,由于主客體形成包結配合物,客體的吸光強度明顯變化,利用這一性質有可能建立一種新的分析方法對食用色素進行檢測,因此進行了分析性能的測試。保持瓜環濃度一定且大大過量于包結計量比的實驗條件下,用分光光度法分別測定了各作用體系的客體濃度-吸光強度的校準曲線,實驗證明客體的濃度與測得的吸光強度在一定范圍內呈線性關系,因此在線性范圍內可以求得校準曲線的線性回歸方程及相關系數,見表1。
測定結果表明,Q[8]-g2、g3體系對于食用色素而言,具有很寬的濃度線性范圍,這是良好的分析體系的基本特征,可以作為一種新穎、靈敏的分析檢測gn的方法用于大環化合物與食用色素的相互作用及其在食品添加劑的開發和應用方面的研究。
3 結論
本文采用紫外-可見吸收光譜法研究Q[8]與食用色素靛藍(g2)和日落黃(g3)客體分子的相互作用情況,考察了pH對主客體相互作用的影響。在pH<10.8時,Q[8]與g2能夠發生相互作用,形成作用比為1∶2的穩定配合物;Q[8]與g3則在pH>5.3時,二者能夠形成穩定的配合物,作用比為2∶1。可以設想,通過調節體系的pH,有可能控制主-客體之間的結合狀態,使主-客體形成穩定的配合物或使作用了的客體從主體中游離出來,這對于瓜環對食用色素的包結和緩釋等作用在食品添加劑的開發和應用具有研究價值。
[1]Freeman W A,Mock W L,Shih N Y.Cucurbituril[J].J Am Chem Soc,1981,103(24):7367-7368.
[2]J M Lehn.Supramolecular chemistry-Scope and Perspective,Molecules,Supramolecules,and Molecular Derives[J].Angew Chem Int Ed Engl,1988,27:89-112.
[3]J Kim,I S Jung,S Y Kim,et al.New Cucurbituril Homologues:Syntheses,Isolation,Charac-terization,and X-ray Crystal Structures of Cucurbit[n]uril(n=5,7 and 8)[J].J Am Chem Soc,2000,122:540-541.
[4]A Day,A P Arnold,J B Rodney,et al.Controlling Factors in the Synthesis of Cucurbituril and Its Homologues[J].J Org Chem,2001,66:8094-8100.
[5]J-Zh Zhao,H J Kim,J Oh,et al.Cucurbit[n]uril Derivatives Soluble in Water and Organic Solvents[J].Angew Chem Int Ed,2001,40:4233-4235.
[6]A Day,R J Blanch,A P Arnold,et al.A Cucurbituril-based Gyroscane:A new supramolecular Form[J].Angew Chem Int Ed,2002,41:275-277.
[7]牟蘭,薛賽鳳,陶朱,等.三種瓜環與4,4'-聯吡啶及N,N'-二甲基4,4'-聯吡啶鹽酸鹽相互作用的研究[J].高等學校化學學報,2006,27(4):654-659.
[8]劉育,尤長城,張衡益.超分子化學:合成受體的分子識別與組裝[M].天津:南開大學出版社,2001:385.
[9]侯昭升,譚業邦,黃玉玲,等.季銨化聚4-乙烯吡啶衍生物與葫蘆脲[6]的超分子自組裝及性質研究[J].化學學報,2005,63(7):653-657.
[10]Kim K,Kim D,LeeJW,etal.Growthofpoly (pseudorotaxane)on gold using host-stabilized charge-transfer interaction[J].Chem Comm,2004:848-849.
[11]曾啟華,祝黔江,薛賽鳳,等.七、八元瓜環對萘二胺異構體相互作用的考察[J].化學學報,2006,64(20):2101.
[12]佟玲,牟蘭,薛賽鳳,等.八元瓜環與氧氟沙星、氟羅沙星、加替沙星及司帕沙星相互作用的光譜法研究[J].光譜學與光譜分析,2009,29(2):446-450.
[13]續浩,陳亮.水溶液中環糊精包結物的包結常數的測定方法[J].分析測試技術與儀器,2001,7(3): 152.
Study on the self-assembled inclusion complexes about cucurbit[8]uril with sunset yellow and indigo dye
ZHENG Li-mei1,WANG Qiu-li2,DOU Chao-qun1,ZHAN Hai-jun1,TAO Zhu3
(1.School of Chemistry and Chemical Engineering,Henan University of Technology,Zhengzhou 450001,China; 2.Zhengzhou University,Zhengzhou 450001,China; 3.Institute of Applied Chemistry,Guizhou University,Guiyang 550025,China)
Interaction between Q[8]with sunset yellow and indigo dye have been investigated by using ultravioletvisible absorption spectrophotometry.The influence of pH on the interaction was studied in details.The results showed that the stability of the inclusion complexes was related to the guests and the pH of solution:Q[8]can interact with guest of g3 completely with a ratio of 2∶1 at pH>5.3.However,the inclusion complexes of Q[8]and g2 completely with a ratio of 1∶2 at pH<10.8.Inclusion and release about cucurbit[n]uril and food dye had been researched and this maybe have important values in development and application of food additives.
spectrophotometry;cucurbit[8]uril;sunset yellow;indigo dye;interaction
TS201.2
A
1002-0306(2011)11-0114-03
2010-09-25
鄭利梅(1978-),女,講師,研究方向:分析化學及超分子化學。
國家自然科學基金資助項目(20961002);河南工業大學校基金(10XZR017)。

