昆津病毒復制子
——一種新型病毒載體
李世華,李曉峰,秦鄂德,秦成峰
軍事醫學科學院微生物流行病研究所 病原微生物生物安全國家重點實驗室,北京 100071
昆津病毒復制子
——一種新型病毒載體
李世華,李曉峰,秦鄂德,秦成峰
軍事醫學科學院微生物流行病研究所 病原微生物生物安全國家重點實驗室,北京 100071
病毒復制子 (Replicon) 是指來源于病毒基因組的能夠自主復制的 RNA分子,保留了病毒非結構蛋白基因,而結構蛋白基因缺失或由外源基因替代。昆津病毒 (Kunjun virus) 為黃病毒科黃病毒屬成員,其復制子具有表達效率高、細胞毒性低、遺傳穩定等特點,在病毒基因組復制調控機制、外源蛋白表達、新型疫苗和基因治療等領域得到了廣泛應用。以下就昆津病毒復制子系統的構建、特性及應用方面的研究進展作一綜述。
昆津病毒,復制子,RNA病毒,病毒載體
Abstract:Viral replicon is a kind of self-replicating viral RNA sourced from viral genome, which contains viral non-structural genes that are critical for viral genome replication with structural proteins deleted or replaced by foreign genes. Kunjin virus is a member of the Flavivirida family, Flavivirus genus, and Kunjin virus replicon is the first and the clearly defined flavivirus replicon. Kunjun virus replicon has been regarded as an excellent viral vector on account of its high expression, lower cytotoxicity and genetic stability. These unique characteristics of kunjin virus replicons make them suitable for the study of viral genome replication, recombinant proteins production, vaccine development and gene therapy. In this article, recent progress in the development, properties and applications of kunjin virus replicon system was briefly reviewed.
Keywords:Kunjin virus, replicon, RNA virus, viral vector
復制子是一種基于 RNA病毒的能自主復制的RNA分子,在病毒學研究中有著廣泛的應用。RNA病毒復制子保留了病毒基因組復制所必需的非結構蛋白基因和非編碼區的關鍵順式作用元件,因而能夠在宿主細胞內有效復制;但同時缺失其結構蛋白基因,因此無法形成感染性的病毒顆粒,操作較為安全。目前,絕大多數單股正鏈RNA病毒的復制子已經構建成功,如甲病毒、黃病毒、冠狀病毒、小RNA病毒和副粘病毒等,其中最為成熟的是甲病毒復制子,如塞姆利基森林病毒 (Semliki Forest Virus,SFV) 復制子已成為一種商業化的真核表達載體,基于甲病毒復制子的HIV疫苗也已進入一期臨床研究[1]。黃病毒科黃病毒屬包括70多種病毒,其中超過一半與人類疾病相關,如登革病毒、蜱傳腦炎病毒、乙型腦炎病毒、黃熱病毒、西尼羅病毒和墨累河谷腦炎病毒等。昆津病毒 (Kunjun Virus,KUNV)復制子是構建成功的第一個黃病毒復制子,在基因組結構與功能、外源蛋白表達、復制子疫苗及基因治療等方面得到廣泛的應用。本文就昆津病毒復制子的研究進展作一綜述。
1 昆津病毒復制子
昆津病毒僅見于澳大利亞北部,與西尼羅病毒同屬一個血清亞型。該病毒感染人類后一般不會致病,偶爾會引起輕微的腦炎。昆津病毒的基因組為全長11 022 nt的單股正鏈RNA,含有一個單一開放讀碼框,編碼3個結構蛋白 (C、prM/M和E) 和7個非結構蛋白 (NS1、NS2A、NS2B、NS3、NS4A、NS4B 和 NS5),5′端和 3′端為非編碼區 (Untranslated region,UTR)。結構蛋白參與病毒的組裝,非結構蛋白和兩端的UTRs共同參與病毒的復制翻譯過程。
1996年,澳大利亞Khromykh等在昆津病毒感染性全長cDNA克隆的基礎上首次構建獲得了昆津病毒復制子[2]。昆津病毒復制子保留了病毒RNA復制所需的NS1-NS5非結構基因,以及兩端的UTRs,缺失了C、PrM和E蛋白基因 (圖1)。由于編碼昆津病毒C蛋白的基因中含有一段保守序列 (Cyclization sequence,CS),該序列與3′ UTR的另一個CS參與基因組環化,與病毒RNA的復制和翻譯密切相關。因此,昆津病毒復制子保留了C蛋白氨基端的前20個氨基酸 (C20) 的編碼序列。同時,昆津病毒E蛋白羧基末端含有一段在NS1蛋白成熟過程中發揮重要作用的信號肽序列,所以在昆津病毒復制子的構建過程中還保留了 E蛋白羧基末端 22個氨基酸(E22) 的編碼序列[3]。
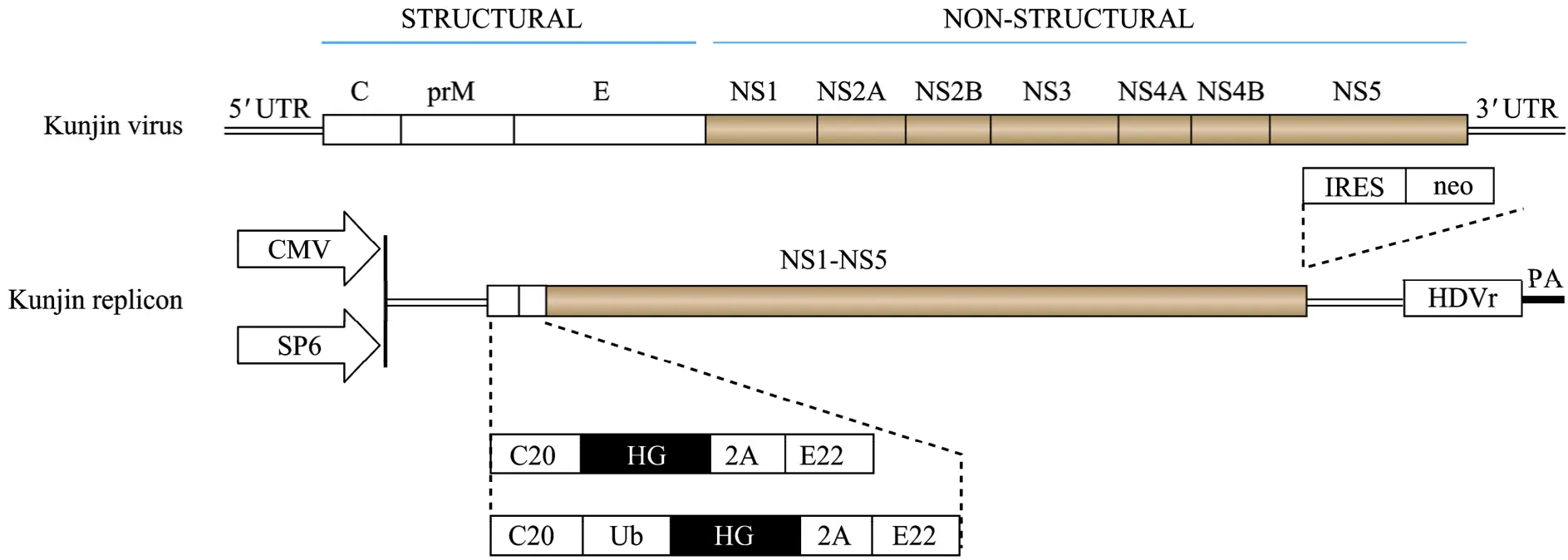
圖1 昆津病毒復制子亞基因組結構示意圖 (由Pijlman GP發表于2006年Biol Ther的文章修改而成[24])Fig. 1 Construction of Kunjin virus replicon genome. neo: neomycin phosphotransferase II gene; HG: Heterologous gene; Ub:Ubiquitin; HDVr: hepatitis delta virus ribozyme; PA: ployadenylation; IRES: Internal ribosome entry site.
為了在體外或者體內啟動復制子的轉錄,復制子的5′ UTR上游必須含有SP6或者CMV啟動子。對于CMV啟動子而言,復制子3′ UTR下游還需引入HDVr (Hepatitis delta virus ribozyme) 的反義基因和多聚腺苷酸 (Ployadenylation,PA) 信號,從而保證獲得完整的病毒基因組 3′末端,有效地起始復制子的復制過程。為保證外源基因插入復制子后獲得正確的表達和加工,外源基因兩端一般還需融合一段具有自我切割功能的序列,如口蹄疫病毒自身水解酶2A序列 (FMDV-2A)[4],或小鼠泛素 (Ubiquitin,Ub) 序列。此外,為了保證病毒非結構蛋白的正確翻譯,需在外源基因的 3′末端添加終止密碼子和內部核糖體進入位點 (Internal ribozyme entry site,IRES) (圖1)。另外,昆津病毒復制子NS5蛋白終止密碼子與3′ UTR之間存在可變區 (Variable region,VR),亦可允許外源基因的插入。如新霉素磷酸轉移酶II (Neomycin phosphotransferase II,neo) 基因被插入該區域以篩選穩定表達昆津病毒復制子的細胞系 (Rep-cell)[2]。
昆津病毒復制子主要以 3種形式進入細胞:第一種是以體外轉錄獲得的RNA形式進入細胞,該方式能迅速增加細胞內復制子RNA的含量,從而大幅提高外源蛋白的表達水平。第二種是將其置于CMV啟動子下游的復制子以質粒DNA的形式轉染細胞,再借助細胞內的 RNA聚合酶Ⅱ進行轉錄來獲得病毒 RNA[5],該方式省去了體外轉錄環節,降低成本的同時也避免了RNA的降解。最后一種是以單輪感染型病毒樣顆粒 (Virus like particle,VLP) 的形式進入細胞。RNA復制子與其結構蛋白仍能形成具有感染性的病毒樣顆粒,但再次侵入細胞后會因其RNA的缺陷而無法生成病毒的結構蛋白,從而無法形成子代病毒樣顆粒,故被稱為單輪感染型 VLP。Khromykh等將昆津病毒復制子和表達其結構蛋白的塞姆利基森林病毒復制子共轉染細胞,獲得了昆津病毒的VLP[6]。Harvey等進一步構建了穩定表達昆津病毒結構蛋白的細胞系,將復制子轉染至該細胞系后也獲得了昆津病毒的單輪感染型VLP[7]。
2 昆津病毒復制子的生物學特性
昆津病毒復制子具有RNA復制子的共有特征:一是復制效率高,可以持續的合成雙鏈RNA,可作為高效的表達載體;二是無整合至宿主基因組的危險;三是免疫效果良好,少量的DNA質粒就能同時誘導粘膜免疫、抗體應答和CTL反應。
除上述特征外,昆津病毒復制子還具有優于其他RNA復制子的特性。其一是細胞毒性低。甲病毒復制子雖是應用最廣泛的RNA復制子,但其細胞毒性強,在細胞內僅能復制幾天即可致細胞凋亡,因此無法持續表達外源蛋白。昆津病毒復制子的細胞毒性則很弱,在細胞內能持續復制數十天之久。其二是產生重組活病毒的概率極低。理論上講,RNA復制子可能與其結構基因的同源序列發生重組,進而產生具有持續感染性的病毒顆粒。但研究顯示,昆津病毒復制子轉染至表達其結構基因的細胞后,并未產生具有感染性的野生型病毒顆粒[8]。此外,研究也未發現其與其他黃病毒復制子間存在重組現象[9]。其三是昆津病毒RNA聚合酶的保真性高,即該病毒的 RNA序列在復制過程中能夠保持較高的穩定性。因此,當昆津病毒復制子作為疫苗載體時,其免疫原性就能保持高度穩定。其四是便于遺傳學操作。昆津病毒復制子的RNA僅為8 000 nt左右,易于對其序列進行改造。正是基于以上優點,昆津病毒復制子已成為一種新型的病毒載體,在病毒復制機制、蛋白表達、新型疫苗及基因治療等方面顯示出巨大的應用潛力。
3 昆津病毒復制子的應用
3.1 黃病毒基因組復制調控機制的研究
由于復制子僅在細胞內完成RNA的復制過程,而不涉及病毒的吸附、侵入、包裝和釋放等階段,因而能直觀地反映病毒基因組復制的特征以及靶細胞的生理變化情況。以昆津復制子為模型,不同學者先后發現了一系列重要的復制調控元件。Khromykh等對昆津病毒復制子5′ UTR和3′ UTR的不同環化序列、保守區和 3′末端的核苷酸進行了突變分析,結果表明這些區段是病毒RNA復制的關鍵序列[2]。這是首次在細胞水平上證明了黃病毒非編碼區在病毒復制中具有重要功能。此外,Liu和Leung等還先后借助昆津病毒復制子證實 NS3和NS2A分別在RNA復制和病毒組裝過程中具有重要作用[10-11]。本實驗室利用登革病毒的復制子系統,發現登革病毒 C蛋白編碼區發夾 (C-coding region hairpin,cHP) 結構對病毒基因組的復制具有重要的調控作用[12]。
此外,昆津病毒復制子在復制機制研究中也有重要的應用。當非結構蛋白缺陷型的全長克隆轉染至復制子細胞系后,復制子將提供具有完整功能活性的非結構蛋白,進而協助缺陷型全長克隆完成復制,最終通過是否形成感染性的病毒顆粒來確定非結構蛋白在病毒復制中的功能。利用上述反式互補系統,Khromykh等研究了非結構蛋白 NS5的功能,在此基礎上提出了黃病毒 RNA復制復合體 (Replication complex,RC) 形成模型以及在其形成過程中 NS3和NS5的作用[13-14]。另外還發現了昆津病毒非結構蛋白編碼區中與復制復合體形成相關的一系列順式和反式作用元件,并研究了其相互作用[15]。上述研究不僅豐富了黃病毒基因組復制機理的相關內容,也為進一步闡明黃病毒復制機制奠定了基礎。
3.2 外源蛋白表達
與其他病毒表達載體相比,昆津病毒復制子載體具有一系列優勢。首先,其細胞毒性低的特點決定了其擁有更廣的宿主范圍;其次,昆津病毒復制子可以隨細胞分裂而分配到子代細胞中,繼續其復制周期,以此持續表達外源蛋白。此外,昆津病毒復制子能夠對外源蛋白進行糖基化等翻譯后修飾,因此能獲得更接近天然活性的目的產物。目前,利用昆津病毒復制子載體已成功表達了報告基因、病毒類抗原、病毒糖類蛋白以及細胞因子等多達20多種外源蛋白[16]。如 Varnavski利用昆津病毒復制子表達系統先后成功表達了氯霉素乙酰轉移酶,綠色熒光蛋白,β-半乳糖苷酶和丙型肝炎病毒NS3蛋白等[17]。除上述的瞬時表達形式外,建立昆津病毒復制子細胞系是另一種持續表達外源蛋白的途徑。含有抗性基因的昆津病毒復制子轉染細胞后,經抗生素篩選后可獲得穩定的復制子細胞系,如Varnavski等利用篩選獲得的 BHK-21細胞系可以穩定表達綠色熒光蛋白和氯霉素乙酰轉移酶達17代以上。
3.3 復制子疫苗
復制子疫苗是近年來新興的疫苗形式。與傳統的疫苗相比,RNA復制子疫苗具有如下優勢:第一,復制效率高,并且能同時誘導體液和細胞免疫反應;第二,只在細胞質中復制,無整合至宿主細胞基因組的危險;第三,病毒樣顆粒形式的疫苗不僅免疫原性強,而且僅能完成單輪感染,安全性高。如前所述,昆津病毒復制子可持久的表達外源蛋白,因此能有效誘發機體產生相應的體液免疫反應。更重要的是,該復制子還能同時誘導CD8+型T細胞免疫反應。Anraku等發現,0.1 μg質粒DNA形式的昆津病毒復制子誘發的T細胞免疫反應效力與100 μg傳統DNA疫苗的 T細胞免疫反應相當[18],這表明昆津病毒復制子在誘導T細胞免疫方面具有明顯的優勢。研究還發現,用含有HIV gag基因的昆津病毒復制子 VLP免疫小鼠后,可以誘發機體產生針對HIV的CD8+型T細胞免疫保護反應,并且持續6~10個月之久[19]。此外,基于該復制子VLP的SIV疫苗在不同的動物模型中進行了免疫保護能力的評價,并證實均具有較好的免疫保護性[20-21]。總之,正是由于昆津病毒復制子能同時誘導體液和細胞免疫,因此成為極具潛力的新型 RNA復制子疫苗候選載體。
3.4 基因治療
基因治療是指通過特定手段將基因類藥物導入病灶中的靶細胞,從而改善或治愈疾病的一種治療手段。昆津病毒復制子靶細胞范圍廣,可持續表達外源產物,而且還能有效誘導干擾素的產生,因此該復制子系統是基因治療領域中理想的遞送系統。粒細胞巨噬細胞集落刺激因子GM-CSF能產生具有抗癌作用的 CD8+型 T細胞反應,Hoang-Le等將GM-CSF通過病毒樣顆粒形式的昆津病毒復制子系統導入腫瘤細胞內,使其在宿主細胞內表達,結果顯示其可以明顯抑制結腸癌細胞 CT26和黑色素瘤細胞B16的增殖[22]。該研究表明,昆津病毒復制子系統可作為理想的抗癌基因導入載體,并將在癌癥的基因治療領域發揮更大作用。
4 小結與展望
同其他RNA復制子一樣,昆津病毒復制子可高效表達外源蛋白。更重要的是,該復制子幾乎無細胞毒性,因此可建立能持續穩定表達復制子的細胞系,進而獲得高產量的 VLP;同時,昆津病毒復制子以基因重組方式產生野生型病毒顆粒的概率極低,故其安全性也很高。正是基于上述優點,昆津病毒復制子在外源蛋白表達、新型疫苗研制以及基因治療等領域得到廣泛應用。盡管目前的研究顯示,VLP是最為有效的復制子遞送方式,但其靶向性還有待進一步提高。此外,盡快研發能夠高效遞送RNA和 DNA形式復制子的技術也是今后亟待解決的問題。目前,澳大利亞的Replikun Biotech公司致力于昆津病毒復制子技術的商品化,并取得了一系列成果,如已成功開發了基于昆津病毒復制子的艾滋病疫苗和腫瘤的治療性疫苗,有些業已進入臨床應用階段。總之,隨著相關研究的不斷深入,有理由相信昆津病毒復制子在更多領域會發揮更為重要的作用,真正為人類造福。
REFERENCES
[1] Davis NL, West A, Reap E, et al. Alphavirus replicon particles as candidate HIV vaccines. IUBMB Life, 2002,53(4/5): 209?211.
[2] Khromykh AA, Westaway EG. Sugenomic replicons of the flavivirus Kunjin: construction and applications. J Virol,1997, 71(2): 1497?1505.
[3] Khromykh AA, Meka H, Guyatt KJ, et al. Essential role of cyclization sequences in flavivirus RNA replication. J Virol, 2001, 75(14): 6719?6728.
[4] de Felipe P. Skipping the co-expression problem: the new 2A ‘CHYSEL’technology. Genet Vaccines Ther, 2004,2(1): 13.
[5] Varnavski AN, Young PR, Khromykh AA. Stable high-level expression of heterologous genes in vitro and in vivo by noncytopathic DNA-based Kunjin virus replicon vectors. J Virol, 2000, 74(9): 4394?4403.
[6] Khromykh AA, Varnavski AN, Westaway EG.Encapsidation of the flavivirus Kunjin replicon RNA by using a complementation system providing Kunjin virus structural proteins in trans. J Virol, 1998, 72(7):5967?5977.
[7] Harvey TJ, Liu WJ, Wang XJ, et al. Tetracycline-inducible packaging cell line for production of flavivirus replicon particles. J Virol, 2004, 78(1): 531?538.
[8] Khromykh AA, Sedlak PL, Guyatt KJ, et al. Efficient trans-complementation of the flavivirus Kunjin NS5 protein but not of the NS1 protein requires its coexpression with other components of the viral replicase.J Virol, 1999, 73(12): 10272?10280.
[9] Lindenbach BD, Rice CM. Trans-Complementation of yellow fever virus NS1 reveals a role in early RNA replication. J Virol, 1997, 71(12): 9608?9617.
[10] Liu WJ, Chen HB, Khromykh AA. Molecular and functional analyses of kunjin virus infectious cDNA cloned demonstrate the essential roles for NS2A in virus assembly and for a nonconservative residue in NS3 in RNA replication. J Virol, 2003, 77(14): 7804?7813.
[11] Leung JY, Pijlman GP, Kondratieva N, et al. Role of nonstructural protein NS2A in flavivirus assembly. J Virol, 2008, 82(10): 4731?4741
[12] Yu XD, Jiang T, Chen SP, et al. Role of cHP element present at the C gene of dengne virus type 4 in viral translation and RNA replication. Bull Acad Mil Med Sci,2008, 32(3): 201?206.
于學東, 姜濤, 陳水平, 等. 登革 4型病毒基因組 cHP發卡結構對病毒復制和翻譯的調控作用. 軍事醫學科學院院刊, 2008, 32(3): 201?206.
[13] Liu WJ, Sedlak PL, Kondratieva N, et al.Complementation analysis of the flavivirus kunjin NS3 and NS5 protein defines the minimal regions essential for formation of a replication complex and shows a requirement of NS3 in cis for virus assembly. J Virol,2002, 76(21): 10766?10775.
[14] Khromykh AA, Kenney MT. Westaway EG.Trans-complementation of flavivirus RNA polymerase gene NS5 by using Kunjin virus replicon-expressing BHK cells. J Virol, 1998, 72(9): 7270?7279.
[15] Khromykh AA, Sedlak PL, Westaway EG. Cis- and trans-acting elements in flavivirus RNA replication. J Virol, 2000, 74(7): 3253?3263.
[16] Pijlman GP, Suhrbier A, Khromykh AA. Kunjin virus replicons: an RNA-based, non-cytopathic viral vector system for protein production, vaccine and gene therapy applications. Expert Opin Biol Ther, 2006, 6(2): 135?145.
[17] Varnavski AN, Khromykh AA. Noncytopathic flavivirus replicon RNA-based system for expression and delivery of heterologous genes. Virology, 1999, 255(2): 366?375.
[18] Anraku I, Harvey TJ, Linedale R, et al. Kunjin virus replicon vaccine vectors induce protective CD8+T-cell immunity. J Virol, 2002, 76(8): 3791?3799.
[19] Harvey TJ, Anraku I, Linedale R, et al. Kunjin virus replicon vectors for human immunodeficiency virus vaccine development. J Virol, 2003, 77(14): 7796?7803.
[20] Anraku I, Mokhonov VV, Rattanasena P, et al. Kunjin replicon-based simian immunodeficiency virus gag vaccines. Vaccine, 2008, 26(26): 3268?3276.
[21] Kent SJ, Rose RD, Mokhonov VV, et al. Evaluation of recombinant Kunjin replicon SIV vaccines for protective efficacy in macaques. Virology, 2008, 374(2): 528?534.
[22] Hoang LD, Anraku1 I, Wang XJ, et al. A Kunjun replicon vector encoding granulocyte macrophage colony-stimulating factor for intra-tumoral gene therapy. Gene Ther, 2009,16(2): 190?199.
Kunjin virus replicon——a novel viral vector
Shihua Li, Xiaofeng Li, E’de Qin, and Chengfeng Qin
State Key Laboratory of Pathogen and Biosecurity, Institute of Microbiology and Epidemiology, Academy of Military Medical Sciences, Beijing 100071, China
Received: June 21, 2010; Accepted: August 6, 2010
Supported by: National Natural Science Foundation of China (No. 30701061), National High Technology Research and Development Program of China (863 Program) (No. 2007AA021501), Beijing Natural Science Foundation (No. 7082063), Doctoral Fund (New Teacher) of Ministry of Education of China (No. 20070023077).
Corresponding author: Jianqiang Kong. Tel: +86-10-63165169; Fax: +86-10-63017757; E-mail: jianqiangk@imm.ac.cn Ping Zhu. Tel: +86-10-63165197; Fax: +86-10-63017757; E-mail: Zhuping@imm.ac.cn
國家自然科學基金 (No. 30701061),國家高技術研究發展計劃 (863計劃) (No. 2007AA021501),北京市自然科學基金 (No. 7082063),教育部博士點新教師基金 (No. 20070023077) 資助。

