鉬摻雜TiO2納米薄膜的制備及其光催化活性研究
竇 焰,曹流圣,秦 潔,李子健,崔 鵬
(合肥工業大學化學工程學院,安徽 合肥 230009)
TiO2光催化氧化技術具有高效、節能、無二次污染的優點,在實際研究和應用方面凸顯了極高的價值。但由于TiO2禁帶(Eg=3.2 eV)比較寬,使其對太陽光(λ<387 nm)的利用率比較低,因此,人們通過金屬離子摻雜、非金屬離子摻雜、表面光敏化等手段對TiO2進行改性,以提高其對太陽光的利用率。由于金屬離子摻雜可能在半導體晶格中引入缺陷位置或改變其結晶度,成為電子或空穴的陷阱而延長壽命;同時能夠降低電子-空穴復合速率、擴寬吸收波長范圍并減小TiO2晶粒粒徑,近年來已成為國內外的研究熱點之一[1~5]。過渡金屬元素鉬,由于價態復雜、制備工藝多樣,其對光催化活性影響因素尚沒有統一的認識。
作者采用Sol-Gel法制備摻鉬納米TiO2溶膠,在玻璃表面制備均勻透明的Mo-TiO2納米薄膜,通過XRD、XPS、SEM等手段對其進行表征。并以羅丹明B為光催化降解體系,通過正交實驗研究了鉬摻雜量、燒結溫度、保溫時間對其光催化活性的影響。
1 實驗
1.1 試劑與儀器
鈦酸四丁酯(化學純)、硝酸、無水乙醇、醋酸、羅丹明B、鉬酸銨等。
KQ218型超聲清洗器,江蘇昆山超聲儀器公司;HH-2型數顯水浴鍋,江蘇常州國華公司;JJ-1型電動攪拌器,江蘇金壇國勝公司;DRZ-4A型燒結爐,天津實驗電爐廠;722S型分光光度計,上海分析儀器廠;PHI-550型多功能電子能譜儀,PHI公司;JSM-6300型掃描電子顯微鏡;D/Max-rB型X-射線衍射儀,Japan-Rigaku公司。
1.2 Mo-TiO2納米薄膜的制備
(1)摻鉬納米TiO2溶膠的制備[2,6]
將鈦酸四丁酯和無水乙醇加入三口燒瓶中混合均勻,加入二次蒸餾水,室溫下攪拌30 min,然后移入90 ℃水浴槽,逐滴加入HNO3,使n(鈦酸四丁酯)∶n(無水乙醇)∶n(水)∶n(HNO3)=9∶1∶85∶5;攪拌1 h后,分別按照鉬鈦原子比0%、0.5%、1.0%、1.5%、1.8%、2.0%將0.1 g·mL-1的鉬酸銨溶液與10 mL HNO3混合后滴入三口燒瓶中,繼續攪拌11 h,得到穩定的摻鉬納米TiO2溶膠。
(2)摻鉬TiO2納米薄膜的制備[6]
將經過水洗、堿洗、酸洗、超聲洗等預處理后的玻璃片浸泡在制得的摻鉬納米TiO2溶膠中,采用浸漬提拉法涂覆于玻璃表面,將干燥后的涂膜玻片放入馬弗爐中,以3 ℃·min-1的速度升溫至所設定的溫度后保溫一段時間,冷卻至室溫,即得摻鉬TiO2(Mo-TiO2)納米薄膜。
1.3 光催化活性測試
將20 mL初始濃度為10 ×10-6的羅丹明B溶液加入到培養皿中,然后在培養皿中放入一片涂有Mo-TiO2納米薄膜的玻片。采用20 W紫外燈為光源進行光催化氧化降解反應,在560 nm波長下測量羅丹明B溶液的吸光度。Mo-TiO2納米薄膜的光催化活性以羅丹明B溶液的脫色率η表示:
2 結果與討論
2.1 XRD分析
圖1為TiO2納米薄膜與摻鉬1.5%(以鈦物質的量計,下同)TiO2納米薄膜在不同溫度下的XRD譜圖,不同溫度處理的Mo-TiO2納米薄膜和TiO2納米薄膜的粒徑、晶型、金紅石相含量見表1。
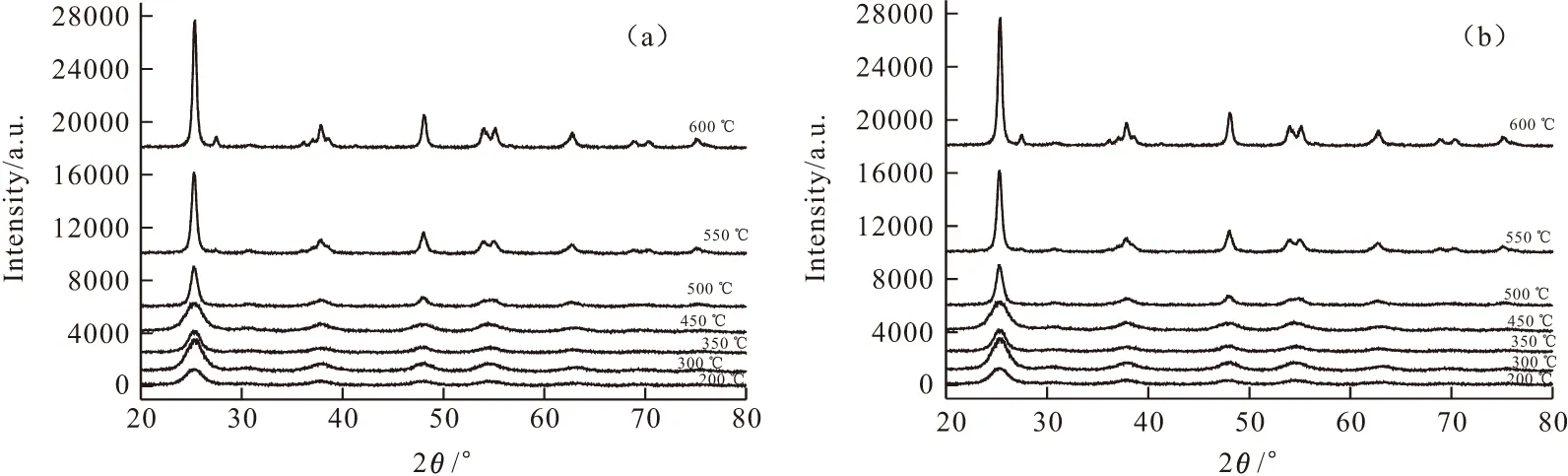
圖1 1.5%Mo-TiO2納米薄膜(a)和TiO2納米薄膜(b)在不同溫度下的XRD圖譜

表1 不同溫度處理的Mo-TiO2納米薄膜與TiO2納米薄膜的粒徑、晶型和金紅石相含量
由圖1可知,制備的薄膜500 ℃以下均為銳鈦礦型,在(101)面具有一定的擇優取向。
由表1可知,經過550 ℃和600 ℃高溫處理,Mo-TiO2納米薄膜比TiO2納米薄膜的金紅石相含量要低,說明摻鉬抑制了TiO2由銳鈦礦相(A)向金紅石相(R)轉變,這與文獻[3]結論相同。研究發現熔點低于TiO2熔點的物質促進A→R的轉變;熔點高的則抑制A→R的轉變。MoO3、TiO2的熔點分別是795 ℃、1590 ℃,摻入MoO3引起A→R相變溫度降低。Mo6+的離子半徑(0.062 nm)和Ti4+的離子半徑(0.068 nm)很接近,可以取代TiO2晶格上的Ti4+,伴隨Mo6+進入TiO2晶格并替代Ti4+的同時,在TiO2能隙中引入能級,擴大了TiO2光譜吸收范圍[7]。
由表1還可知,隨著燒結溫度的升高,TiO2和Mo-TiO2晶粒尺寸均逐漸增大,但純TiO2比Mo-TiO2晶粒長大速度明顯要快;在相同燒結溫度下,Mo-TiO2晶粒尺寸明顯要小。說明鉬摻雜有抑制晶粒長大的作用,Mo6+摻雜引起TiO2晶格畸變,阻止了金紅石相的晶粒生長,從而延緩了TiO2由銳鈦礦相向金紅石相的轉變[8]。
研究表明,鉬摻雜量低的樣品,Mo6+主要取代TiO2晶格中小部分的Ti4+而摻雜在TiO2晶格中,高價的Mo6+成為電子授體,導致TiO2費米能級提高,大大有利于表面吸附的氧成為O2-而提高光催化活性[9];鉬摻雜量超過3%的樣品,實際上是Mo-TiO2和MoO3兩種晶相的復合物,兩種化學上完全不同的晶體之間存在異質結,兩者的價帶和導帶有可能并列連接,使光生電子和孔穴更易于復合,從而導致光催化活性下降。本研究在鉬摻雜量達到2%時已經呈現光催化降解活性下降的趨勢[1,8]。
2.2 XPS分析
1.5%Mo-TiO2粉末的XPS圖見圖2,圖2a、2b、2c分別是Mo3d、Ti2p、O1s的較窄能量范圍掃描圖。
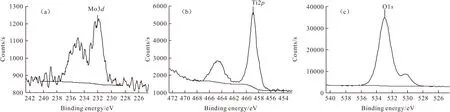
圖2 1.5%Mo-TiO2粉末的XPS圖
由圖2可知,Mo3d3/2的結合能為235.55 eV、Mo3d5/2的結合能為232.4 eV,對應于Mo6+物種。Ti2p具有兩個峰,Ti2p3/2結合能為458.8 eV、Ti2p1/2的結合能為464.7 eV。純TiO2的O1s譜圖有兩個峰,說明有兩個氧物種,分別為晶格氧(與TiO2鍵對應,529.4 eV)與吸附氧(與氧空位濃度有關,530.5 eV)。
根據XPS分析,1.5%Mo-TiO2的C、O、Ti、Mo 4種元素的原子百分比為32.59∶45.58∶19.40∶2.33。n(Mo)/n(Ti)比值遠超過制備時的1.5%,這說明部分鉬以Mo6+的形式進入晶格中以取代晶格中的Ti4+,部分鉬可能以MoO3的形式存在于樣品的表面[2]。
2.3 SEM分析(圖3)

圖3 TiO2納米薄膜(a)和Mo-TiO2納米薄膜(b)的SEM照片
TiO2納米薄膜中晶粒尺寸對其光催化活性有直接決定作用,因為納米顆粒會表現出量子尺寸效應,具有較強的光催化活性。由圖3可知,TiO2納米薄膜和Mo-TiO2納米薄膜的顆粒分布都很均勻,大小分別為10~20 nm和9~10 nm,表明摻鉬對TiO2的粒徑生長有抑制作用,這與XRD分析結果一致。
2.4 光催化活性
固定鉬摻雜量為1.5%、燒結溫度為500 ℃、保溫時間為1 h中的其它條件,制備Mo-TiO2納米薄膜,分別考察鉬摻雜量、燒結溫度、保溫時間對其光催化羅丹明B降解脫色效果的影響,結果見圖4。

圖4 鉬摻雜量(a)、燒結溫度(b)、保溫時間(c)對光催化活性的影響
由圖4a可知,鉬摻雜量對薄膜的光催化活性有重要的影響,隨著鉬摻雜量的增加,其光催化活性不斷提高,鉬摻雜量為1.5%時羅丹明B脫色率達到最大;但隨著鉬摻雜量的繼續增加,其光催化活性反而有所下降。這是因為,當鉬摻雜量較少時,Mo6+取代Ti4+所增加的氧缺陷促進電子空穴分離的作用效果并不明顯,而表面光活性位置由于Mo6+摻雜而減少,從而導致光催化活性的降低;當鉬摻雜量過多時,一方面由于Mo6+以氧化物的形式聚集在TiO2晶體表面而成為光生電子空穴的復合中心,另一方面由于Mo6+是d軌道空的可變價離子,在一定程度上奪取了TiO2本身的電子造成TiO2中空穴濃度增大,光致激發電子空穴效應減弱,使得光催化活性降低[2,6]。
由圖4b可知,燒結溫度為500 ℃時羅丹明B的脫色率最大。燒結溫度升高,一方面能夠增加TiO2的結晶度,有利于提高光催化活性;另一方面,會促使晶粒長大,晶粒尺寸對光催化活性的影響是光吸收和散射效率、載流子動力學和比表面積等對光催化活性影響競爭作用的結果,使燒結溫度存在一個最佳值(500 ℃),在此條件下晶粒尺寸最佳[7]。
由圖4c可知,保溫時間為1 h時羅丹明B的脫色率最大。保溫時間對晶型的影響與燒結溫度的影響是交互的。一般而言,較高的燒結溫度需要的保溫時間較短,而較低的燒結溫度需要的保溫時間較長,一定比例的銳鈦礦相和金紅石相條件下TiO2光催化效果最好,這與很多研究的結論相同。
3 結論
(1)采用Sol-Gel法、浸漬提拉法得到Mo-TiO2納米薄膜,Ti4+被Mo6+取代,Mo6+進入到TiO2的晶格中形成了Mo-TiO2結構,引起晶格畸變,抑制晶粒長大與TiO2由銳鈦礦相向金紅石相轉變。
(2)鉬摻雜到TiO2薄膜中,高溫燒結過程中,燒結溫度和保溫時間相互影響。在鉬摻雜量為1.5%、燒結溫度為500 ℃、保溫時間為1 h條件下得到Mo-TiO2納米薄膜的光催化降解效果最好。
[1] 劉興平,蔣榮英,柳松.TiO2/Mo-TiO2的制備、表征和光催化活性[J].催化學報,2010,31(11):1381-1387.
[2] 陳桂華,閆瑞強,梁華定,等.Mo摻雜TiO2的制備及其光催化性能[J].硅酸鹽通報,2009,28(5):944-950.
[3] Zhu Haiyang,Shen Mingmin,Wu Yong,et al.Dispersion behaviors of molybdena on titania (rutile and/or anatase)[J].J Phys Chem B,2005,109(23):11720-11726.
[4] Mestl G,Srinivasan T K K.Raman spectroscopy of monolayer-type catalyst:Supported molybdenum oxides[J].Catal Rev,1998,40(4):451-570.
[5] Nova I,Lietti L,Casagrande L,et al.Characterization and reactivity of TiO2-supported MoO3De-NoxSCR catalysts[J].Appl Cata(B):Eiviro,1998,17(3):245-258.
[6] 楊瑩,李新軍,陳俊濤,等.Mo的摻雜方式對TiO2光催化活性的影響[J].中國有色金屬學報,2004,14(3):509-514.
[7] 王玉萍,袁俊秀,李杰,等.Mo-TiO2/AC光催化劑的制備及可見光降解L-酸的研究[J].環境科學,2007,28(8):1746-1751.
[8] 侯亞奇,莊大明,張弓,等.反應濺射制備TiO2:MoO3復合薄膜的光催化降解性能[J].硅酸鹽學報,2004,32(6):694-699.
[9] 湛社霞,范山湖,林作梅,等.鉬摻雜TiO2光催化活性的研究[J].中山大學學報(自然科學版),2001,40(2):125-127.

