帕洛諾司瓊及昂丹司瓊預防化療所致惡心、嘔吐的效果對比
(上海市第一人民醫院寶山分院,上海200940)
化療是腫瘤患者最常用的治療手段之一,但其所致惡心、嘔吐等不良反應可影響患者對化療的依從性,進而影響療效。因此,預防和減輕化療所致惡心、嘔吐反應對化療的順利進行及腫瘤患者的預后具有重大意義。2009年5月~2010年5月,我們分別采用帕洛諾司瓊與昂丹司瓊預防化療所致惡心、嘔吐。現將其臨床效果報告如下。
1 資料與方法
1.1 臨床資料 同期于我院行化療的惡性腫瘤患者32例,男18例,女14例;年齡42~72歲,平均58歲。均經病理學或細胞學明確診斷(臨床分期Ⅱ~Ⅳ期),其中肺癌16例、食管癌10例、卵巢癌6例。入組標準:依從性好;預期生存期>3個月,可耐受1周期以上化療;KPS評分>70分;化療前血常規、肝腎功能均無明顯異常;無顱內轉移、顱內壓升高、消化道梗阻等可致惡心、嘔吐的疾病;化療前1 d無嘔吐,未使用止吐藥物。將32例患者隨機分為觀察組和對照組各16例,其一般資料具有可比性。
1.2 治療方法 兩組均采用含順鉑(DDP)的化療方案,其中GP方案15例:吉西他濱1 000mg/m2于第1、8天靜滴,DDP 30mg/m2于第1~3天靜滴;TP方案17例:紫杉醇(PTX)75mg/m2于d1靜滴,DDP用法同上。觀察組于第1天化療前30min靜推帕洛諾司瓊注射液0.25mg,對照組于每日化療前及化療后30min分別靜推昂丹司瓊注射液8mg,均連用3 d。均連續觀察3周(即1個化療周期)。
1.3 相關指標觀察 ①急性期(化療24 h內)及延遲期(化療24 h后)惡心、嘔吐控制效果:無惡心、無嘔吐為完全控制(CR);出現嘔吐1~2次/d,惡心5~12次/d為基本控制(PR);嘔吐3~5次/d,惡心5~12次/d為輕微控制(MR);嘔吐>5次/d,惡心>12次/d為無效(P)。有效控制(RR)率以CR+PR計算。②不良反應發生情況。
1.4 統計學方法 采用SPSS17.0統計學分析軟件進行統計學處理。樣本比較采用χ2檢驗,檢驗水準α=0.05。
2 結果
2.1 惡心、嘔吐控制效果 見表1。
2.2 不良反應 兩組不良反應均較輕微,各分別出現便秘2例、頭痛1例,患者均可耐受,未作特別處理。兩組不良反應發生率均為18.75%。
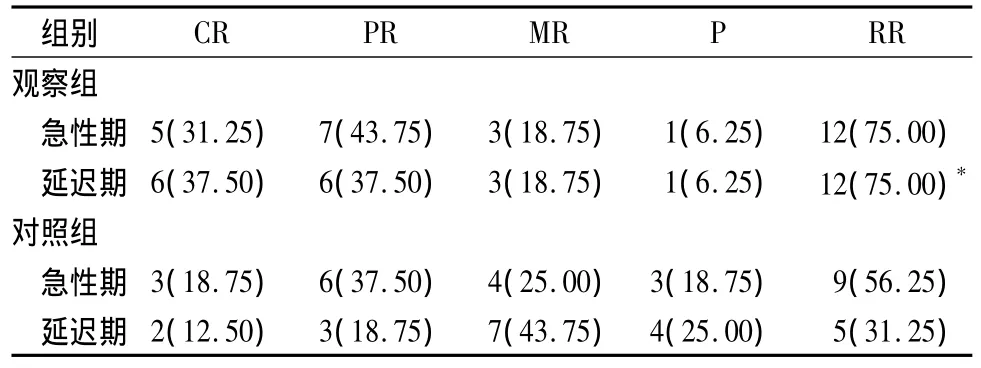
表1 兩組惡心、嘔吐控制情況[n=16,例(%)]
3 討論
據統計,70%~80%的化療患者會出現惡心、嘔吐等消化道反應,處理不當甚至可發生脫水、電解質紊亂等并發癥,從而嚴重影響患者的生活質量并導致其依從性降低[1]。發生機理如下:化療藥物及其代謝產物刺激腸壁尤其是十二指腸腸壁嗜鉻細胞釋放5-羥色胺(5-HT3),5-HT3作用于小腸的5-HT3受體,經迷走神經傳導至化學感受觸發帶(CTZ),進而激活嘔吐中樞引發嘔吐;化療藥物的代謝產物還可通過血液直接刺激延髓網狀組織及CTZ內受體(包括多巴胺受體、血清素受體)導致嘔吐。5-HT3受體拮抗劑可通過選擇性抑制外周神經系統突觸前5-HT3受體興奮性,阻斷嘔吐反射過程中神經介質的化學傳遞,有效預防化療誘發的惡心、嘔吐反應。目前臨床常用的5-HT3受體拮抗劑代表藥物包括昂丹司瓊、托烷司瓊、格拉司瓊,三者均為第一代5-HT3受體拮抗劑。該類藥物對預防化療所致急性期惡心、嘔吐反應效果顯著,聯用地塞米松時完全緩解率達68%~90%,但其預防延遲性反應的完全緩解率僅47%~56%。最近一項Meta分析證實,化療24 h后應用第一代5-HT3受體拮抗劑對預防控制延遲期惡心、嘔吐反應基本無效[2]。
帕洛諾司瓊為第二代5-HT3受體拮抗劑,與上述藥物比較具有體內代謝半衰期長(約40 h)、5-HT3受體親和力強(是第一代的30~100倍[3])的優點,故止吐效力更好。國內外多項多中心、隨機、雙盲臨床研究顯示,帕洛諾司瓊預防化療所致急性期惡心、嘔吐的效果與第一代5-HT3受體拮抗劑相近[4]。國外兩項大樣本研究顯示,帕洛諾司瓊對中度致吐性化療患者延遲期惡心、嘔吐的CR顯著高于昂丹司瓊和多拉司瓊[5,6]。此外,諸多研究表明帕洛諾司瓊不良反應輕微、發生率低,主要為便秘、頭痛、腹痛等,與第一代5-HT3受體拮抗劑相似;因半衰期長,僅需化療首日0.25mg單次靜推(治療中位有效期超過120 h),且1周內無需重復使用[7],可顯著提高患者的順應性[8]。基于此帕洛諾司瓊成為美國FDA批準用于防治化療所致延遲期惡性、嘔吐的惟一5-HT3受體拮抗劑。本研究顯示,兩組急性期RR無顯著差異,觀察組延遲期RR顯著高于對照組;且兩組不良反應發生率無顯著差異,均較輕微。與上述文獻報道一致。
總之,帕洛諾司瓊預防化療所致惡性、嘔吐的安全性與昂丹司瓊相似,但效果優于后者且臨床使用方便。
[1]Tomek R,Vrdoljak E,Vrbanec D,et al.Croatian guidelines for prevention of chemotherapy induced nausea and vomiting[J].Lijec Vjesn,2009,131(3-4):49-53.
[2]Geling O,Eichler HG.Should 5-hydroxytryptamine-3 receptor antagonists be administered beyond 24 hours after chemotherapy to prevent delayed emesis Systematic reevaluation of clinical evidence and drug cost implications[J].J Clin Oncol,2005,23(6):1289-1294.
[3]Ingersoll GL,Wasilewski A,Haller M,et al.Effect of concord grape juice on chemotherapy-induced nausea and vomiting:results of a pilot study[J].Oncol Nurs Forum,2010,37(2):213-221.
[4]Jordan K,Hinke A,Grothey A,et al.Granisetron versus tropisetron for prophy lax is of acute chemotherapy-induced emesis:A Pooled analysis[J].Support Care Cancer,2005,13(1):26-31.
[5]Eisenberg P,Figueroa-Vadillo J,Zamora R,et al.Improved prevention of moderately emetogenic chemotherapy-induced nausea and vomiting with palonosetron,a pharmacologically novel 5-HT3 receptor antagonist:resultsof a phaseⅢ,single-dose trial versus dolasetron[J].Cancer,2003,98(11):2473-2482.
[6]Gralla R,Lichinitser M,Van der Vegt S,et al.Palonosetron improves prevention of chemotherapy-induced nausea and vomiting following moderately emetogenic chemotherapy:results of a doubleblind randomized phaseⅢtrial comparing single does of palonosetron with ondansetron[J].Ann Oncol,2003,14(10):1570-1577.
[7]Siddiqui MA,Scott LJ.Palonosetron[J].Drugs,2004,64(10):1125-1132.
[8]陳映霞,秦書逵,程穎,等.鹽酸帕洛諾司瓊預防化療性惡心嘔吐的多中心雙盲隨機對照臨床研究[J].臨床腫瘤學雜志,2007,12(3):164.

