無污泥外排除磷系統的磷平衡及除磷途徑分析*
周健 栗靜靜 竇艷艷 陳爽 龍熙
(重慶大學城市建設與環境工程學院∥三峽庫區生態環境教育部重點實驗室,重慶400045)
傳統污水生物除磷主要是通過聚磷菌(PAOs)在厭氧條件下釋磷和在好氧條件下過量吸磷,并將磷富集于污泥中,通過排除富磷污泥而實現磷的去除.近年來出現的反硝化除磷是通過反硝化PAOs,在缺氧條件下以硝酸鹽為電子受體進行聚磷,同時將硝酸鹽還原成N2或氮化物,但其除磷機理與傳統PAOs生物除磷類同,仍是通過富磷污泥的外排除磷.富磷污泥的排放增加了污泥處理成本,不利于磷資源的回收.隨著分析檢測條件和技術的提高,磷化氫(PH3)被公認為環境中普遍存在的痕量物質,目前相關研究認為[1-3],PH3可通過微生物還原作用產生,但PH3的微生物形成機理尚不清楚.2009年,重慶大學首次成功構建了超高鹽高磷廢水磷酸鹽生物還原除磷系統[4],在反應器中實現了通過磷酸鹽生物還原將磷以氣態磷化氫的形式去除的途徑.這種新型的除磷途徑不僅無富磷污泥的排放,且有利于磷資源的回收.文中對序批式生物膜反應器(SBBR)在無剩余污泥外排條件下的高效除磷機理進行研究.在考察其除磷效果的基礎上,通過對系統運行期間的磷平衡分析,以及對運行周期內磷的去除規律和污泥中聚合磷酸鹽(ploy-P)和結合態磷化氫(MBP)含量的監測分析,探討其除磷途徑.
1 試驗部分
1.1 試驗水質
采用重慶大學宿舍區未經化糞池處理的生活污水作為試驗用水,其中CODCr為(1000±150)mg/L,、總氮(TN)、、總磷(TP)的質量濃度分別為(75±25)、(130±30)、(6.0±2.0)、(7.5± 2.0)mg/L.
1.2 試驗裝置
試驗裝置見圖1,SBBR反應器的有效容積為10L,內設組合填料、曝氣砂頭等.其中組合纖維填料由維綸制成,比表面積大,物理、化學性能穩定,掛膜密度為45%.試驗通過充氧泵供氧、溫度控制儀控制水溫,采用定時器控制運行程序.

圖1 試驗裝置圖Fig.1 Diagram of experimental equipment
1.3 試驗方法
反應器接種某城市污水處理廠脫水污泥,接種污泥質量濃度為10 g/L,控制反應器水溫30℃,有機負荷為1.0 kg/(m3·d),溶解氧(DO)含量為6mg/L,反應器連續曝氣且不外排污泥,每周期運行時間為12 h,具體運行工況為:瞬時進水—曝氣12h—瞬時排水.反應器運行45 d,試驗期間測試水中TP、的含量、COD以及污泥量、污泥中磷含量、ploy-P及MBP含量等指標.
1.4 測試手段
為了探討反應器在長期不排泥的條件下系統內磷的遷移損失途徑,對反應器自啟動至運行45 d過程中的磷進行物料衡算.測試每個周期進出水中的TP質量濃度及進出水水量,分別統計45d運行中隨液相進入及排出反應器的磷總量,兩者差值即為系統液相中磷的損失量;反應器啟動時測試單位接種污泥中的磷含量及接種污泥總量,以確定運行開始時系統固相中的磷含量;運行45 d后分別測試反應器中生物膜及底部脫落生物膜的污泥量、單位生物膜污泥中磷含量,以確定運行45d后系統固相中的磷含量.系統運行開始時固相中磷含量與運行45d后固相中磷含量的差值即為固相中磷的損失量;系統液相與固相中磷的損失量的總和即為系統中磷損失的總量.
生物膜中污泥量的測定采用張朝升等[5]提出的方法;污泥中TP含量的測定采用過硫酸鉀消解法[6];污泥中ploy-P含量的測定參照豆俊峰等[7]采用的方法;污泥中的MBP含量采用堿消解-溴化硝酸氧化[8]-鉬銻抗分光光度法測定;其它常規指標的測試均采用標準方法[9].
2 結果與分析
2.1 反應器效能分析
由圖2中可知,反應器在不外排污泥、連續曝氣條件下仍能實現磷的高效去除.反應器在前7 d的運行過程中,TP去除率逐漸上升,7 d后反應器的出水TP質量濃度為0.9 mg/L,TP去除率達90.5%;此后,在連續的38 d運行過程中TP去除率基本穩定,出水TP質量濃度為0.8~1.3mg/L,去除率穩定在82.1%~91.8%.反應器在長達45 d的運行過程中,一直未外排污泥,但仍具有良好的TP去除效果.傳統PAOs生物除磷要求富磷污泥及時排出,以獲得良好的除磷效果,而該反應器長期未排污泥仍能取得良好的除磷效果,所以傳統生物除磷途徑無法解釋此現象.
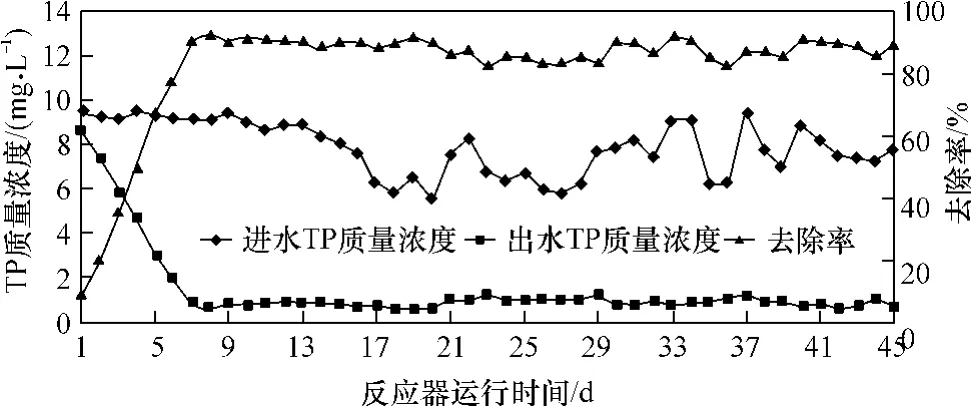
圖2 SBBR內TP去除的逐日變化曲線Fig.2 Daily variation curves of TP removal in sequencing batch biofilm reactor
2.2 反應器內磷平衡分析
反應器自啟動至運行45 d的過程中磷的物料衡算結果如表1所示.反應器在不外排污泥、連續曝氣條件下連續運行45 d的過程中,系統生物量增加36.8g(以干污泥質量計),微生物正常生長時污泥中磷含量(以TP占干污泥的質量百分比計)一般為干重的1.5%~2.3%[10],在滿足微生物正常生長所需的條件下,每天用于微生物生長合成的磷的量為12.3~20.5 mg,遠小于系統每天的外源磷去除量(34.8mg),因此,系統中磷的高效去除不可能是微生物正常合成所致;系統液相中共損失1980.0 mg磷,固相中損失-1450.0 mg磷,整個系統中共損失530.0mg磷.同時,系統固相中磷含量為1.93%,小于傳統PAOs除磷工藝污泥中的磷含量(3%~7%)[11].Dévai等[12]對幾個污水處理廠系統進行磷的物料平衡核算時,發現磷有一定的損失,并在污水廠釋放的氣體中檢測到了磷化氫,且進一步證實損失的磷中25%~50%是以氣態磷形式逸出的.由此判斷,系統中磷可能是通過磷酸鹽生物還原后以氣態磷化氫的形式發生了轉化.Gassmann等[13]于1993年首次將經過酸(堿)消解土壤或沉積物中釋放出的磷化氫定義為MBP,Dévai等[14]的進一步研究表明,85%以上的磷化氫以污泥結合態的形式存在,污泥中MBP的量可直觀反映出反應器中磷發生氣態轉化的可能性.對系統中MBP的測試顯示,反應器啟動時接種濕污泥中的MBP含量(以每千克濕污泥中所含結合態磷化氫質量計)為0,運行45d后生物膜濕污泥中MBP含量高達3.5 mg/kg,進一步證實系統中的磷以磷化氫氣體的形式發生了轉化.

表1 磷平衡計算表Table 1 Calculating table of phosphorus balance
2.3 反應器周期運行期間磷的去除規律分析
由圖3中可知,反應器內液相中TP的質量濃度在反應期間呈現逐步下降的趨勢,從反應起始時的3.6mg/L降至反應結束時的0.3mg/L.從反應開始至反應0.5h的過程中,TP的去除速率為0.65g/(m3·h); 0.5~1.5 h期間的去除速率為2.18 g/(m3·h); 1.5~2.0h期間的去除速率為0.87 g/(m3·h),此時對TP的去除率達到了89.2%;2.0~12.0 h期間TP去除速率為0.03 g/(m3·h),TP質量濃度從0.7mg/L降至0.3 mg/L.從反應開始至反應0.5 h期間,由于基質中部分有機磷轉化為無機磷,液相中的質量濃度有所上升;0.5~2.5 h期間的質量濃度逐步下降,反應2.5h時基質中有機磷基本轉化完全,質量濃度為 0.5 mg/L;2.5~ 12.0h期間的去除規律與TP的一致.

圖3 反應器運行周期內TP與PO34-質量濃度的變化曲線Fig.3 Change curves of mass concentrations of TP and PO34-in a running period of reactor
傳統PAOs生物除磷主要依靠PAOs厭氧釋磷和好氧過量吸磷的特性,因此,在傳統生物除磷周期運行的液相中,呈現出由PAOs特性導致的磷質量濃度先升后降的現象.在本試驗中,并未出現傳統的生物除磷周期中液相磷質量濃度的波動情況,反應器內液相中的TP質量濃度從反應開始的3.6 mg/L至反應結束時的0.3mg/L,一直保持下降的趨勢.
ploy-P是PAOs生物除磷過程中產生并最終儲存在PAOs體內的能量物質,由圖4中可知,反應器運行周期內ploy-P含量(以每克干污泥中所含聚合磷酸鹽質量計)從反應開始至 1.0 h增加了0.006mg/g,1.0~12.0 h期間反應器中ploy-P含量基本保持不變,整個周期內 ploy-P最高含量為0.257mg/g,遠小于PAOs生物除磷中ploy-P的含量(80~83mg/g),這進一步證實了反應器內磷的去除并不是PAOs生物除磷所致.

圖4 反應器運行周期內MBP和ploy-P含量的變化曲線Fig.4 Change curves of MBP and ploy-P contents in a running period of reactor
由圖4中還可知,反應器運行一周期內的MBP含量呈現先逐步降低后逐步上升的趨勢,從反應開始至反應1.0h的過程中反應器中MBP含量的下降速率最快,為0.8mg/(kg·h),1.0~6.0 h期間下降速率放緩,6.0h時MBP含量降至最低(2.9mg/kg).分析認為,由于反應開始至反應6.0 h過程中,污泥中可被磷酸鹽還原菌(PRB)直接利用的活性磷處于轉化過程中,PRB此時沒有足夠的可利用活性磷,使得由于PRB作用生成MBP的速率小于由于曝氣攪動產生磷化氫的脫附率,導致反應器在前6.0h的運行中MBP量逐漸下降;反應6.0 h至反應結束的過程中,隨著PRB可利用活性磷的產生,MBP的產生速率高于磷化氫的脫附速率,使MBP含量逐漸上升,反應結束時MBP含量為3.5mg/kg,遠高于各相關研究在厭氧消化污泥[15]、稻田[16]、湖底或海底沉積物[17]等環境中檢測到的 10-12數量級的 MBP含量.
反應器始終處于曝氣狀態,曝氣擾動越強烈,越有利于磷化氫的脫附.由圖5中可知,從反應開始至反應0.5 h的過程中,DO含量快速升高到了6.27mg/L.反應開始至反應0.5h的過程中,液相環境氧化還原電位(ORP)從-128.7 mV迅速升高至65.5 mV,從反應 0.5 h到反應結束一直以9.52mV/h的平均速率上升,這符合PRB成為優勢菌種的環境要求[18],因此,本研究中磷的去除途徑可能是磷酸鹽的生物還原.

圖5 反應器運行周期內DO含量與ORP的變化曲線Fig.5 Change curves of DO content and ORP in a running period of reactor
2.4 反應器中磷的去除途徑分析
由前文分析可知,反應器在45 d的運行過程中,在未外排污泥的條件下仍能實現磷的高效去除.系統中的磷不可能通過污泥排出,但對反應器自啟動至運行45 d的過程中磷的物料衡算表明,反應器所接種污泥中的磷含量為1.36%,屬正常值,運行45d后污泥中磷含量為1.93%,這與傳統PAOs生物除磷排富磷污泥中的磷含量(3%~7%)相差甚遠,可見系統中的磷并未富集在污泥中.反應器運行周期內液相磷含量一直保持下降與污泥中ploy-P含量基本保持不變的規律,以及系統污泥中極少的ploy-P含量(0.257mg/g)均顯示系統不是傳統的PAOs生物除磷系統;從反應器運行周期內ORP、DO含量的變化規律可見反應器內形成的是一個適合PRB生長的環境,而非PAOs除磷所必需的厭氧好氧工況交替運行的環境,周期內MBP含量的變化規律及其較高的含量(3.5mg/kg)說明系統是一個以PRB為優勢菌種的磷酸鹽生物還原系統;反應器45 d運行過程中磷的物料衡算顯示,系統共損失530.0 mg磷,說明損失的磷可能是通過磷酸鹽的生物還原作用以氣態磷化物的途徑排出的.
3 結語
反應器在不外排污泥、連續曝氣條件下,連續運行45d的過程中,出水TP取得了良好的去除效果,液相中共損失磷1 980.0 mg,整個系統共損失磷530.0mg;在反應器一個周期的運行中,TP的質量濃度一直保持下降的趨勢,MBP呈現先逐步降低后逐步上升的趨勢;污泥中磷含量(1.93%)及ploy-P含量(0.257mg/g)均小于傳統PAOs除磷法污泥中的相應指標含量,且MBP含量高達3.5mg/kg.因此,該系統非PAOs生物除磷系統,系統可能是通過磷酸鹽的生物還原作用以氣態磷化物的途徑實現除磷的.
[1] Barbara V Rutishauser,Reinhard Bachofen.Phosphine formation from sewage sludge cultures[J].Anaerobe,1999,5(2):525-531.
[2] Grady Hanrahan,Salmassi Tina M,Khachikian Crist S,et al.Reduced inorganic phosphorus in the natural environment:significance,speciation and determination[J].Talanta,2005,66(9):435-444.
[3] 韋偉,張可方,張朝升,等.磷化氫在水處理中的研究現狀[J].中國給水排水,2009,25(12):20-23. Wei Wei,Zhang Ke-fang,Zhang Chao-sheng,et al.Research status of phosphine in water treatment[J].China Water&Wastewater,2009,25(12):20-23.
[4] 陳垚,龍騰銳,周健,等.超高鹽高磷廢水磷酸鹽還原系統構建過程中磷系統轉化分析研究[J].環境科學,2009,30(9):2592-2597. Chen Yao,Long Teng-rui,Zhou Jian,et al.Transformation of phosphorus forms in the construction process of phosphate reduction system of hypersaline and high-phosphorus wastewater[J].Environmental Science,2009,30(9): 2592-2597.
[5] 張朝升,榮宏偉,張可方.序批式生物膜反應器的生物膜特性研究[J].中國給水排水,2007,23(1):53-59. Zhang Chao-sheng,Rong Hong-wei,Zhang Ke-fang.Study on characteristics of biofilm in SBBR with biological phosphorus removal ability[J].China Water&Wastewater,2007,23(1):53-59.
[6] 陳國梅.鉬酸銨分光光度法測定城市污泥中的總磷[J].中國給水排水,2006,22(2):85-86. Chen Guo-mei.Ammonium molybdate spectrophotometric method for determination of total phosphorus in municipal sewage sludge[J].China Water&Wastewater,2006,22 (2):85-86.
[7] 豆俊峰,羅固源,劉翔.生物降解除磷過程厭氧釋磷的代謝機理及其動力學分析[J].環境科學學報,2005,25(9):1164-1169. Dou Jun-feng,Luo Gu-yuan,Liu Xiang.The metabolic mechanism of anaerobic phosphorus release and its kinetic analysis during biological phosphorus removal process[J].Journal of Environmental Science,2005,25(9): 1164-1169.
[8] 吳滿昌,寧平,任丙南,等.黃磷尾氣中總磷及磷化氫的測定[J].環境污染與防治,2004,26(4):317-318. Wu Man-chang,Ning Ping,Ren Bing-nan,et al.Determination of total phosphorus and hydrogen phosphide in yellow phosphorus tail gas[J].Environmental Pollution&Control,2004,26(4):317-318.
[9] 國家環境保護局.水和廢水檢測分析方法[M].4版.北京:中國環境科學出版社,2002:211-280.
[10] 許保玖,龍騰銳.當代給水與廢水處理原理[M].2版.北京:高等教育出版社,2000:530-547.
[11] 鄭興燦,李亞新.污水除磷脫氮技術[M].北京:中國建筑工業出版社,1998:192-193.
[12] Dévai István,Felf?ldy Lajos,Wittner Ilona,et al.Detection of phosphine:new aspects of the phosphorus cycle in the hydrosphere[J].Nature,1988,333(26):343-345.
[13] Gassmann Günter,Glindemann Dietmar.Phosphine(PH3) in the biosphere[J].Angewandte Chemie International Edition,1993,32(5):761-763.
[14] Dévai I,Delaune R D,Dévai G,et al.Phosphine production potential of various wastewater and sewage sludge sources[J].Analytical Letters,1999,32(10):1447-1457.
[15] Joris Roels,Herman Van Langenhove,Willy Verstraete. Determination of phosphine in biogas and sludge at pptlevels with gas chromatography-thermionic specific detection[J].Journal of Chromatography A,2002,9(52): 229-237.
[16] Han C,Gu X Y,Geng J J,et al.Production and emission of phosphine gas from wetland ecosystems[J].Science Direct,2010,22(9):1309-1311.
[17] Li J B,Zhang G L,Zhang J,et al.Matrix bound phosphine in sediments of the yellow sea and its coastal areas[J]. Continental Shelf Research,2010,30(4):743-751.
[18] 陳垚.基于磷酸鹽生物還原的超高鹽高磷廢水除磷技術研究[D].重慶:重慶大學城市建設與環境工程學院,2010.

