黃連素對 2型糖尿病中國地鼠肝臟固醇調節元件結合蛋白轉錄調節系統表達的影響
劉栩晗,李國生,黃 瀾,朱 華,劉亞莉,馬春梅
(1.大連市中心醫院內分泌科,遼寧 大連 116003;2.大連醫科大學附屬第一醫院病理科,遼寧 大連 116011;3.中國醫學科學院醫學實驗動物研究所病理科,北京 100021)
黃連素對 2型糖尿病中國地鼠肝臟固醇調節元件結合蛋白轉錄調節系統表達的影響
劉栩晗1,李國生2,黃 瀾3,朱 華3,劉亞莉3,馬春梅3
(1.大連市中心醫院內分泌科,遼寧 大連 116003;2.大連醫科大學附屬第一醫院病理科,遼寧 大連 116011;3.中國醫學科學院醫學實驗動物研究所病理科,北京 100021)
[目的]研究黃連素對2型糖尿病中國地鼠肝臟固醇調節元件結合蛋白(SREBPs)、其調控基因及靶基因表達的影響,探討黃連素治療脂誘性肝胰島素抵抗的分子機制。[方法]以高脂飲食及結合小劑量鏈脲菌素的方法建立胰島素抵抗和 2型糖尿病中國地鼠模型。成模后隨機分成正常對照組、胰島素抵抗組、2型糖尿病組和 2型糖尿病黃連素治療組,治療 9周。應用實時定量PCR方法檢測各組地鼠肝臟 SREBPs、其調控基因及靶基因的表達。[結果]PCR結果顯示模型地鼠脂肪變的肝臟中SREBPs基因、SREBPs切割激活蛋白(SCAP)基因、蛋白酶 S1P和S2P基因和 SREBPs靶基因的表達增加,胰島素誘導基因(Insigs)的表達降低。黃連素有效地改善胰島素抵抗,同時,逆轉了SREBPs、其調控基因及靶基因表達的改變。[結論]SREBPs轉錄調控系統參與黃連素治療 2型糖尿病地鼠脂誘性肝胰島素抵抗。
黃連素;2型糖尿病;固醇調節元件結合蛋白;胰島素抵抗;中國地鼠;肝臟
胰島素抵抗和胰島素分泌受損是 2型糖尿病的重要特征。依據藥物的作用機制,目前用于治療 2型糖尿病的藥物主要分為胰島素增敏性藥物和促胰島素分泌性藥物。黃連素是我國傳統中草藥黃連的主要生物活性成分,具有胰島素增敏性藥物的作用特點及較小的毒副作用。糖尿病脂毒性理論提出:高脂飲食性肥胖發生 2型糖尿病的潛在機制是胰島素敏感組織異位脂沉積造成的脂誘性胰島素抵抗[1,2]。因此,脂誘性肝臟胰島素抵抗在肥胖相關 2型糖尿病形成中發揮重要作用。作者選擇具有糖尿病易感性和脂代謝類人性的中國地鼠[3]建立肥胖胰島素抵抗和2型糖尿病地鼠模型并研究黃連素對糖尿病地鼠肝臟 SREBPs轉錄調控系統表達的影響,探討黃連素治療肝臟脂誘性胰島素抵抗的分子機制。
1 材料和方法
1.1 實驗動物
健康中國地鼠,雌雄各半,60只,清潔級,血糖(4.41±0.59)mmol/L,26周齡,體重 (124.0±10.5)g,購自四川省醫學科學院實驗動物研究所,許可證號:SCXK(川)2004216。單籠飼養,飼以標準的顆粒飼料,自由攝食攝水,12 h光照周期。
1.2 主要藥品試劑及儀器
高脂飼料購自軍事醫學科學院實驗動物中心,配方為:1%膽固醇,0.02%牛膽酸鈉,10%豬油,10%蛋黃粉及 78.98%基礎飼料。鏈脲菌素(STZ)購自 Sigma公司。應用穩豪 One-Touch血糖儀監測血糖。鼠胰島素 ELISA試劑盒(美國 Linco公司)購自吉泰公司。血甘油三酯(TG)試劑盒、游離脂肪酸(FFAs)試劑盒、低密度脂蛋白(LDL)試劑盒、高密度脂蛋白(HDL)試劑盒、總膽固醇(TC)試劑盒(Randox公司)均購自北京九強生物技術有限公司。日立 8060全自動生化分析儀。RNA提取試劑盒(RNeasy Mini Kit,德國 Qiagen公司)和逆轉錄試劑盒(Omniscript Reverse Transcription Kit,德國 Qiagen公司)購自基因有限公司。HotStarTaqTMDNA聚合酶(TaKaRa)購自百靈克公司,Mg2+及緩沖液為 Taq酶自帶 。 RNase inhibitor、Oligo-dT(美國 Promea公司)和實時熒光定量 PCR反應試劑盒(iQ SYBR Green PCR Kit,美國 Bio-rad公司)購自東勝創新公司。實時熒光定量 PCR儀(美國 Bio-rad公司)。紫外分光光度計(美國 Amersham公司)。其余常用試劑購自北京鼎國生物技術公司。黃連素原料藥,批號:200506065,購自東北制藥總廠。
1.3 動物模型制備、分組及治療
參照相關的造模方法[4-6]建立肥胖胰島素抵抗和 2型糖尿病地鼠模型并加以改進。健康地鼠 60只,雌雄各半,隨機分為普食正常對照組和高脂飲食組,前者 10只,飼以普通飼料;后者 50只,飼以高脂飲食。飼養 4周后,高脂飲食喂養的地鼠自發形成肥胖性胰島素抵抗狀態,將這些肥胖性胰島素抵抗地鼠隨機分成 2組,一組(40只地鼠)禁食 12 h后,按 40mg/kg(將 STZ用 0.1mmol/L,pH 4.2的無菌檸檬酸緩沖液配制成 1%STZ溶液,0.2 mm微孔過濾滅菌)的劑量間隔 2 d 2次腹腔注射 STZ,注射后繼續禁食 12 h建立 2型糖尿病模型。另一組(10只)及普食正常對照組(10只)注射等量的 0.1 mmol/L,pH 4.2的無菌檸檬酸緩沖液(注射方式和劑量相同)。處理后,各組地鼠繼續維持原飲食 2周。糖尿病和胰島素抵抗地鼠模型依據空腹血糖(糖尿病地鼠≥9 mmol/L)和口服葡萄糖耐量試驗確定。造模結束時共得到 2型糖尿病地鼠 29只,選擇 20只,隨機分為 2型糖尿病組和黃連素治療的 2型糖尿病組,每組 10只,再將普通飼料組作為對照組,單純高脂飲食選擇 10只作為胰島素抵抗組,共4組。黃連素治療組按每日每只灌服 150 mg/kg黃連素(溶于羧甲基纖維素/PBS溶液)的劑量給藥 9周。對照組、胰島素抵抗組和 2型糖尿病組每日每只灌服相應劑量的羧甲基纖維素/PBS溶液。治療期間對照組喂以普通飼料,其余各組繼續喂以高脂飼料。實驗結束時,各組地鼠禁食 12 h,在禁食 9.5 h時稱重同時給藥,在給藥 2.5 h時,乙醚麻醉,眼內眥靜脈取血并處死,剖開腹腔,迅速取出肝臟、稱重、大部分肝臟液氮速凍并保存于 -80℃備用,少部分肝臟固定于 10%中性甲醛溶液。4℃3000 r/m in離心 20min分離血漿并保存于 -80℃備用。
1.4 口服葡萄糖耐量試驗(OGTT)和糖耐量試驗曲線下面積(AUC)
地鼠禁食 12 h后,給予葡萄糖 2 g/kg灌胃,乙醚麻醉后,在設定的時間點 (0、30、60、120和 180 min)眼內眥靜脈取血測血糖。糖耐量曲線下面積 =1/2空腹測定值 +60 min測定值 +120 min測定值 +1/2 180m in測定值。
1.5 血生化檢測
血漿 FFAs、TC、LDL、HDL和 TG的濃度采用Randox公司試劑盒,應用日立 8060全自動生化分析儀進行檢測。應用穩豪血糖儀檢測血糖。應用Linco公司鼠胰島素 ELISA試劑盒檢測血漿胰島素濃度。
1.6 組織形態學觀察
肝組織固定于 10%中性甲醛溶液,逐級脫水,石蠟包埋,切片,HE染色,光鏡觀察。
1.7 RNA的提取及逆轉錄反應
取凍存肝組織 30 mg,按 RNeasy Mini Kit說明書提取總 RNA。RNA濃度及純度用紫外分光光度計(Amersham)進行檢測。保證 260/280在 1.8~2.0之間,并用 1%瓊脂糖凝膠電泳鑒定完整性。逆轉錄反應:1μg總 RNA,5×iScript Mix 4μL,iScript反轉錄酶 1μL,去核酸酶水 12μL,組成總體積 20 μL的反應體系。反應條件:25℃,5 m in;42℃,30 min;85℃,5min,冷卻至 4℃。
1.8 實時定量 PCR檢測
在實時定量 PCR擴增之前對引物進行普通PCR擴增以得到最適反應條件。實時熒光定量PCR按 iQ SYBR Green Mix Kit說明書操作。建立15μL的反應體系:50 ng總 RNA的逆轉錄產物,上游引物 0.5μL(6μmol/L),下游引物 0.5μL(6 μmol/L),2×iQ SYBRGreen Mix 7.5μL,去離子水5.5μL。使用 iQ Syber Green Supermix和 iCycler iQ Real-Time PCR Detection System擴增。反應條件是:95℃ 3min,95℃ 10 s,59℃45 s,45個循環。擴增之后,做溶解曲線檢測產物的均一性,反應從59℃開始,每個循環 10 s上升 0.5℃,共 80個循環。每個反應均重復 3次。設立陰性對照。擴增之前測定每對引物的擴增效率,經檢測所用引物的擴增效率均接近于 1。樣本目標基因相對含量的計算使用2(-Delta Delta C(T))方法[7]。β-actin作為內參基因。引物序列見表 1。

表 1 實時熒光定量PCR引物列表Tab 1 Primers used for real-time RT-PCR
1.9 統計學方法
實驗數據以均數 ±標準差(mean±SD)表示。統計學差異使用 SPSS13.0進行 t檢驗和單因素方差分析檢驗。P≤0.05為差異有統計學意義。
2 結 果
2.1 胰島素抵抗組、2型糖尿病組和黃連素組地鼠的代謝特征
各組地鼠的表型和代謝特征見表 2。實驗結束時,與對照組相比,胰島素抵抗地鼠和 2型糖尿病地鼠的體重顯著增加(P<0.05),表現肥胖,但兩者之間的體重差異無顯著性意義 (P>0.05)。胰島素抵抗地鼠和 2型糖尿病地鼠的肝臟重量明顯增加(P<0.05),肝重/體重的比值顯著高于對照組(P<0.05),肝臟呈腫大狀態。與對照組相比,除了 HDL水平降低以外,胰島素抵抗地鼠和 2型糖尿病地鼠的血脂(包括 FFAs、TC、LDL和 TG)水平顯著升高(P<0.05)。胰島素抵抗地鼠的血糖雖然有所升高,但未達到糖尿病的血糖標準。與對照地鼠和胰島素抵抗地鼠相比,2型糖尿病地鼠的血糖顯著升高(P<0.05)。與對照組相比,胰島素抵抗地鼠表現明顯的高胰島素血癥,而 2型糖尿病地鼠的胰島素水平與對照組相似。與對照組相比,胰島素抵抗地鼠和 2型糖尿病地鼠 OGTT各指定點的血糖值增高(P<0.05),血漿胰島素的水平異常,OGTT的糖曲線下面積增大(P<0.05),胰島素抵抗地鼠的胰島素曲線下面積增大(P<0.05),而 2型糖尿病地鼠的胰島素曲線下面積與對照組地鼠相近似(圖1)。胰島素抵抗地鼠和 2型糖尿病地鼠的胰島素敏感指數降低(P<0.05),而胰島素抵抗指數升高(P<0.05)(表 2)。經過黃連素治療后,糖尿病地鼠的體重有所降低,但無顯著性意義(P>0.05)。與糖尿病地鼠相比,黃連素治療組地鼠的肝臟重量明顯降低(P<0.05)。除了 HDL水平增高以外,治療組地鼠的血脂(FFAs、TC、LDL和 TG)水平和血糖濃度顯著的降低(P<0.05)。治療組地鼠血漿胰島素水平與對照組地鼠和模型組地鼠血漿胰島素水平相似。與糖尿病地鼠相比,治療組地鼠的 OGTT各指定點的血糖濃度減低(P<0.05),各指定點血漿胰島素的分泌和分泌水平趨近于恢復正常。治療組地鼠糖曲線下面積減少(P<0.05),胰島素曲線下面積與模型組相比無差異(P>0.05)(圖 1)。治療組地鼠胰島素敏感指數增大而胰島素抵抗指數減小(P<0.05)(表 2)。
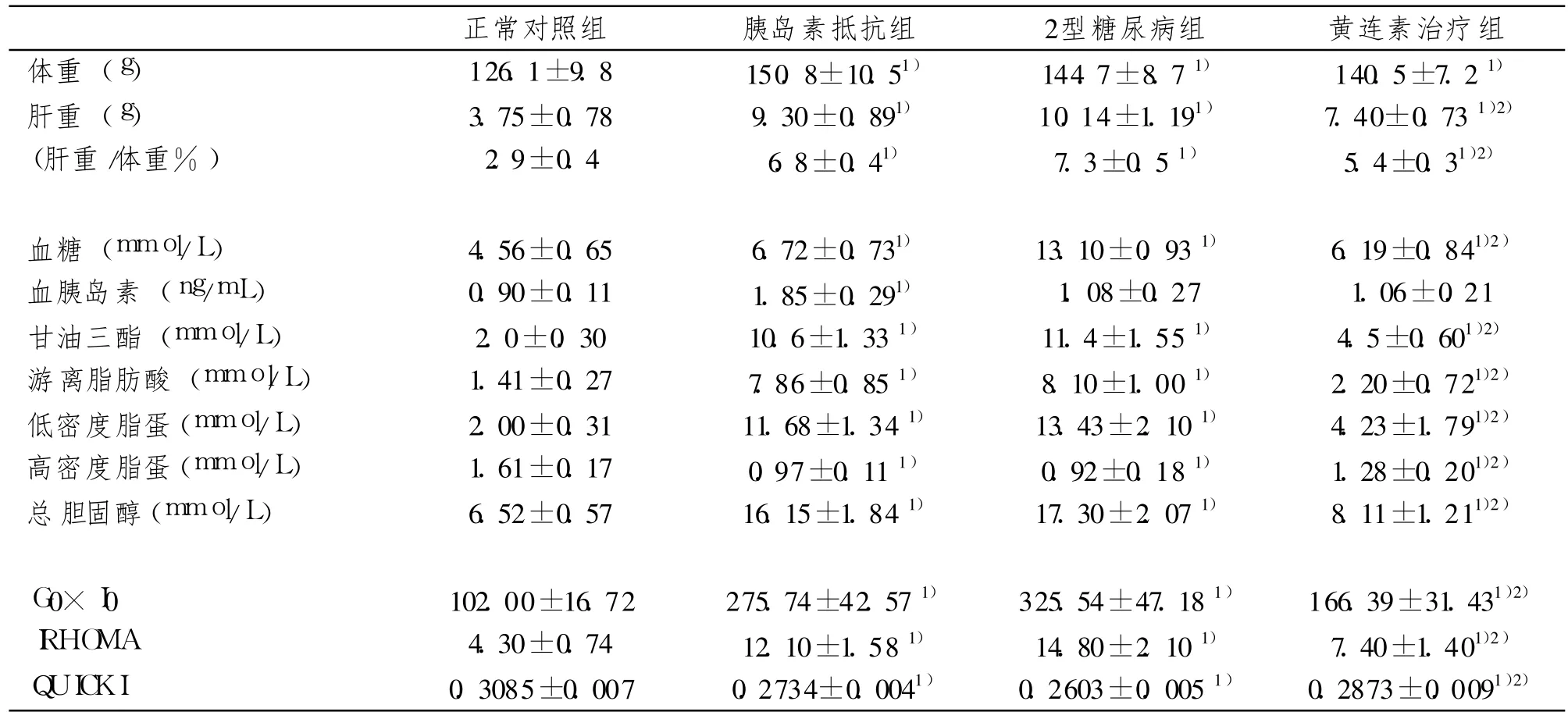
表 2 對照組、胰島素抵抗組、2型糖尿病組和黃連素治療組地鼠的代謝表型特征Tab 2 Basalmetabolic characterization of control,insulin-resistant,diabetic and berberine-treated diabetic groups
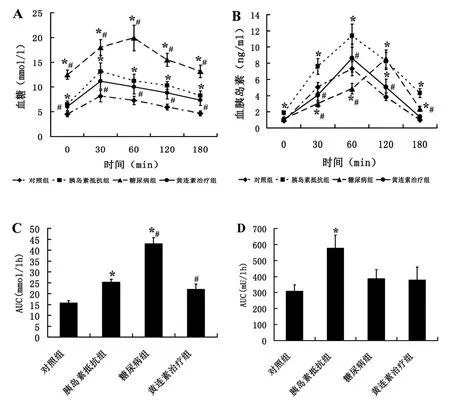
圖1 對照組、胰島素抵抗組、2型糖尿病組和黃連素治療組地鼠口服糖耐量試驗Fig 1Oralglucose tolerance tests(OGTT)in control,insulin-resistant,diabetic and berberine-treated diabetic hamsters口服葡萄糖耐量試驗A:葡萄糖曲線;B:胰島素曲線;C:葡萄糖曲線下面積;D:胰島素曲線下面積*與對照組比較,P<0.05;#2型糖尿病組與治療組比較,P<0.05
2.2 胰島素抵抗組、2型糖尿病組和黃連素治療組地鼠肝臟組織形態改變
組織形態學研究顯示,對照組地鼠肝組織結構和細胞形態正常。胰島素抵抗地鼠和 2型糖尿病地鼠均出現肝臟脂沉積(肝脂肪變性)。胰島素抵抗地鼠的肝細胞內出現中等大小和較大的脂滴并呈現中重度的肝臟脂肪變性。2型糖尿病地鼠的肝細胞內出現中等大小和較大的脂滴并且含有較大脂滴的肝細胞數目稍增多,但亦呈現中重度的肝臟脂肪變性。總體看來,二者肝臟脂沉積程度相似,無本質差異。黃連素治療組地鼠肝臟內也見脂肪沉積。肝細胞內見中小脂滴,有的僅為小脂滴并呈現輕中度的肝臟脂肪變性,與糖尿病地鼠肝臟的病變程度有明顯的差異(圖 2)。
2.3 胰島素抵抗組、2型糖尿病組和黃連素治療組地鼠肝臟中 SREBPs、其調控基因及靶基因表達的改變
實時定量 RT-PCR的結果(RT-PCR產物的瓊脂糖電泳圖見圖 3)顯示與對照組相比,胰島素抵抗地鼠和 2型糖尿病地鼠肝臟中 SREBPs(SREBP-1a、SREBP-1c和 SREBP-2)基因 、SCAP基因、S1P和 S2P基因的表達增加,Insigs(Insig-1和 Insig-2)基因的表達降低。SREBP-1c調節的脂肪酸合成相關靶基因,如脂肪酸合成酶(FAS)、乙酰輔酶 A羧化酶(ACC)和硬脂酰輔酶 A去飽和酶 -1(SCD-1)的表達升高。SREBP-2調節的膽固醇代謝相關靶基因,如羥甲戊二酰輔酶 A合成酶(HMG CoA synthase)、羥甲戊二酰輔酶 A還原酶(HMG CoA reductase)和高密度脂蛋白受體(LDLR)的表達也增加。SREBPs、其調控基因及靶基因表達的改變在胰島素抵抗地鼠和 2型糖尿病地鼠之間差異存在顯著性意義 (P<0.05)。黃連素治療后,與對照組相比,黃連素治療組地鼠肝臟中 SREBPs、SCAP、S1P、S2P、FAS、ACC、SCD-1、HMG CoA synthase、HMG CoA reductase和 LDLR的表達增加,Insigs的表達也增加。但與 2型糖尿病組地鼠相比較,黃連素治療組地鼠肝臟中 SREBPs、SCAP、S1P、S2P、FAS、ACC、SCD-1、HMG CoA synthase、HMG CoA reductase和 LDLR的表達顯著降低,Insigs的表達顯著增加。SREBPs、其調控基因及靶基因表達的改變在黃連素治療組和 2型糖尿病組之間差異存在顯著性意義 (P<0.05)(圖 4)。
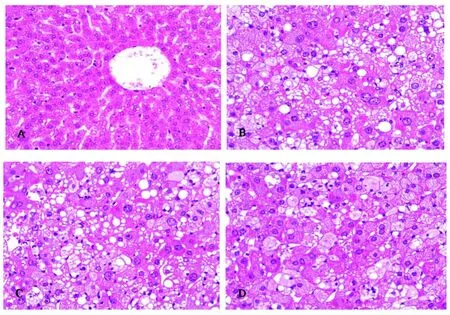
圖2 對照組、胰島素抵抗組、2型糖尿病組和黃連素治療組地鼠肝臟的形態學改變(HE染色,200×)Fig 2 Alteration in morphology of livers from control,insulin-resistant,diabetic and berberine-treated diabetic groups(H&E stain,200×)A:對照組肝臟;B:胰島素抵抗組肝臟;C:2型糖尿病組肝臟;D:黃連素治療組肝臟

圖3 RT-PCR產物的瓊脂糖電泳圖Fig 3 The picture of agarose gel electrophoresis of products of RT-PCR
3 討 論
胰島素抵抗是 2型糖尿病發生的重要誘發因素。糖尿病脂毒性學說提出脂誘性肝胰島素抵抗是飲食誘導的肥胖相關 2型糖尿病重要的發病機制之一。所以,胰島素增敏劑對脂誘性肝胰島素抵抗的治療是治療飲食誘導的肥胖相關 2型糖尿病的重要策略。黃連素是作為糖尿病治療方劑的主要成份之一的中草藥黃連的主要生物活性成份之一,是一種異喹啉生物堿,具有廣泛的藥理學和生物化學效應。實驗研究顯示黃連素具有胰島素增敏劑的藥理學特性,其治療機制可能是受體后效應[8,9]。盡管目前對黃連素降低 2型糖尿病血糖血脂作用的分子機制已有相關研究,但黃連素對 2型糖尿病胰島素抵抗,尤其是對脂誘性肝胰島素抵抗治療作用的分子機制了解甚少。本研究結果顯示 SREBPs、其調控基因及靶基因參與了黃連素治療 2型糖尿病地鼠脂誘性肝胰島素抵抗。
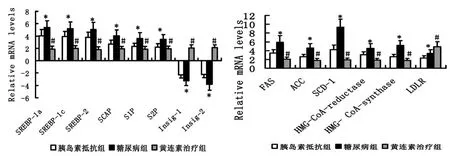
圖4 黃連素對肝臟SREBPs、其調控基因及靶基因表達的影響Fig 4 The effects of berberine on the exp ression of hepatic SREBPs,their regulating genes and their target genes*糠尿病組與胰島素抵抗組比較,P<0.05;#黃連素治療組與 2型糠尿病組比較,P<0.05
SREBPs屬于轉錄因子家族,哺乳動物細胞基因組編碼 3個 SREBP的異構體,分別為 SREBP-1a、SREBP-1c和 SREBP-2。SREBP-1a具有較高的轉錄活性,是所有 SREBP敏感基因的激活者,包括膽固醇、脂肪酸和甘油三酯的合成。SREBP-1優先增強脂肪酸合成基因的轉錄與脂肪酸的合成,而SREBP-2則優先激活膽固醇的合成[10]。SREBPs的轉錄后調節與 SCAP、S1P、S2P、Insigs和細胞內脂的含量及種類相關[11]。本研究結果顯示與對照組相比,胰島素抵抗地鼠和 2型糖尿病地鼠肝臟中SREBPs、SCAP、S1P、S2P及 SREBPs靶基因的表達增加,Insigs(Insig-1和 Insig-2)的表達降低。在黃連素治療地鼠肝臟中上述基因表達相反。這些基因表達改變顯示胰島素抵抗地鼠和 2型糖尿病地鼠肝臟中表達增加的 SCAP基因有助于增強伴侶作用,護送 SREBPs到達高爾基體。表達增加的蛋白酶 S1P和 S2P基因有助于增強切割水解釋放出成熟的 SREBPs(nSREBPs),進而有助于成熟的SREBPs進入核內誘導膽固醇和脂肪酸合成基因的轉錄。當細胞內膽固醇或氧化膽固醇濃度較高時,SCAP/SREBPs復合體駐留在內質網中,當細胞內膽固醇或氧化膽固醇濃度較低或排空時,SCAP護送SREBPs到達高爾基體進行水解[11]。Insigs具有與膽固醇協同抑制 SCAP/SREBPs復合體從內質網到高爾基體的運輸作用[12,13]。本實驗結果顯示降低表達的 Insigs似乎在細胞內膽固醇增高時不能有效地以一個固醇依賴的方式與 SCAP相互作用并形成一個 SCAP/SREBPs/Insigs復合物,使 SCAP/SREBPs復合體駐留在內質網中。因此,胰島素抵抗地鼠和2型糖尿病地鼠肝臟中上述 SREBPs調控基因表達的改變有助于 SREBPs基因表達產物的成熟及其誘導成脂效應的發揮。模型地鼠肝臟增加表達的SREBPs可能主要由高脂飲食[14]或增高的血糖[15]誘導形成并通過此機制加速成熟并發揮成脂效應。同時,本研究結果顯示在胰島素抵抗地鼠和 2型糖尿病地鼠肝臟中 SREBPs的靶基因 FAS、ACC、SCD1、LDLR、HMG CoA synthase和 HMG CoA reductase的表達增加。表達增強的 SREBP-1c將誘導脂合成基因,如 FAS,ACC和 SCD1的表達,增加肝臟甘油三酯的沉積[16],有助于脂誘性胰島素抵抗的形成。另外,增強表達的 SREBP-1c也可以通過直接抑制胰島素受體底物 2基因轉錄而抑制胰島素信號通路,從而引起或加重胰島素抵抗[17]。表達增強的 SREBP-2將誘導 LDLR,HMG CoA synthase和HMG CoA reductase的表達而增加膽固醇的攝取和合成[18]。表達增強的 SREBP-1a似乎可以同時參與脂和膽固醇的合成[19]。因此,表達改變的 SREBPs轉錄調控系統將導致肝臟脂代謝異常和脂沉積,這將有助于胰島素抵抗地鼠和 2型糖尿病地鼠脂誘性肝胰島素抵抗的形成。黃連素逆轉了 SREBPs、其調控基因及靶基因在 2型糖尿病地鼠肝臟中的表達,似乎具有 SREBPs劑量效應調節劑的性質。黃連素降低了糖尿病狀態下表達增加的 SCAP、S1P和S2P的表達。表達降低的 SCAP有助于減弱護送SREBPs到高爾基體的伴侶作用。表達降低的 S1P和 S2P有助于減少 SREBPs的成熟,進而有助于削弱成熟的 SREBPs對膽固醇和脂肪酸合成基因的激活效應。同時,黃連素增加了糖尿病狀態下表達降低的 Insigs的表達。表達增加的 Insigs有助于在細胞內膽固醇增高時有效地抑制 SCAP/SREBPs復合體從內質網的外輸。在黃連素治療地鼠肝臟中表達降低的 SREBPs及其靶基因將有助于降低肝臟的成脂過程、減輕肝脂沉積和改善脂誘性肝胰島素抵抗。這從基因表達水平上解釋了黃連素對肝臟脂代謝的調節效應。然而,結果亦顯示,與對照相比,在黃連素治療地鼠肝臟中 SREBPs及其靶基因的表達仍然處于升高狀態,但即使如此,表達增加的成脂基因似乎并沒有加重脂誘性肝胰島素抵抗和影響黃連素對脂誘性肝胰島素抵抗的治療效應。因此,表達增加的肝臟 SREBPs轉錄調控系統是否是進一步降低血脂所必需的仍需進一步研究。另外,表達增加的肝臟 SREBPs轉錄調控系統是暫時的還是較持久的尚不清楚。因此,黃連素誘導的肝 SREBPs轉錄調控系統表達的改變有助于改善脂誘性肝胰島素抵抗,進而防止肥胖相關糖尿病的進展。
SREBPs轉錄調控系統參與 2型糖尿病脂誘性肝胰島素抵抗的形成及黃連素治療 2型糖尿病脂誘性肝胰島素抵抗的效應。
[1]McGarry JD.Dysregulation of fatty acid metabolism in the etiology of type 2 diabetes[J].Diabetes,2002,51(1):7-18.
[2]Unger RH,Orci L.Lipotoxic diseases of nonadipose tissues in obesity[J].Int J Obes Relat Metab Disord,2000,24(Suppl 4):S28-32.
[3]Wu Q,Ortegon AM,Tsang B,et al.FATP1 is an insulinsensitive fatty acid transporter involved in diet-induced obesity[J].Mol Cell Biol,2006,26(9):3455-3467.
[4]Danda RS,Habiba NM,Rincon-Choles H,et al.Kidney involvement in a nongenetic ratmodel of type 2 diabetes[J].Kidney Int,2005,68(6):256-257.
[5]Luo J,Quan J,Tsai J,et al.Nongenetic mouse models of noninsulin-dependent diabetes mellitus[J].Metabolism,1998,47(6):663-668.
[6]Mu J,Woods J,Zhou YP,et al.Chronic inhibition of dipep tidyl pep tidase-4 with a sitagliptin analog p reserves pancreatic beta-cellmass and function in a rodentmodel of type 2 diabetes[J].Diabetes,2006,55(6):1695-1704.
[7]Livak KJ,Schmittgen TD.Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T))Method[J].Methods,2001,25(4):402-408.
[8]陳其明,謝明智.小檗堿對正常小鼠血糖調節的影響[J].藥學學報,1987,22(4):161-165.
[9]歐陽禮枝,陸付耳,劉文軍,等.小檗堿對胰島素抵抗大鼠肝臟葡萄糖激酶及其調節蛋白的影響[J].世界華人消化雜志,2007,15(3):885-889.
[10]Brown MS,Goldstein JL.The SREBP pathway:regu lation of cholesterolmetabolism by proteolysis of a membranebound transcription factor[J].Cell,1997(89):331-340.
[11]Adams CM,Goldstein JL,Brown MS.Brown cholesterolinduced conformational change in SCAP Insig proteins and m imicked by cationic amphiphiles[J].Proc Natl Acad Sci USA,2003,100(19):10647-10652.
[12]Yang T,Espenshade PJ,W right ME.Crucial step in cholesterol homeostasis:sterols p romote binding of SCAP to INSIG-1,amembrane protein that facilitates retention of SREBPs in ER[J].Cell,2002,110(4):489-500.
[13]Yabe D,Brown MS,Goldstein JL.Insig-2,a second endoplasmic reticu lum protein that binds SCAP and b locks export of sterol regulatory element-binding p roteins[J].Proc Natl Acad Sci USA,2002,99(20):12753-12758.
[14]Finck BN,Kelly DP.PGC-1 coactivators:inducible regulators of energy metabolism in health and disease[J].J Clin Invest,2006,116(3):615-622.
[15]Hasty AH,Shimano H,Yahagi N,et al.Sterol regu latory element-binding protein-1 is regulated by glucose at the transcriptional level[J].J Biol Chem,2000,275(40):31069-31077.
[16]Yahagi N,Shimano H,Hasty AH,et al.Absence of sterol regulatory element-binding protein-1(SREBP-1)ameliorates fatty livers but not obesity or insulin resistance in Lep(ob)/Lep(ob)mice[J].JBiol Chem,2002,277(22):19353-19357.
[17]Ide T,Shimano H,Yahagi N,et al.SREBPs suppress IRS-2-mediated insulin signalling in the liver[J].Nat Cell Biol,2004,6(4):351-357.
[18]Miserez AR,Muller PY,Barella L,et al.Sterol-regu latory element-binding protein(SREBP)-2 contributes to polygenic hypercholesterolaem ia[J].Atherosclerosis,2002,164(1):15-26.
[19]Liang G,Yang J,Horton JD,et al.Dim inished hepatic response to fasting/refeeding and liver X receptor agonists in m ice with selective deficiency of sterol regulatory ele ment-binding protein-1c[J].JBiol Chem,2002,277(11):9520-9528.
Effectsof berberine on expression of hepatic sterol regulatory element-binding protein,its control and target genes in type 2 diabetic Chinese ham sters
LIU Xu-han1,LIGuo-sheng2,HUANG Lan3,ZHU Hua3,LIU Ya-li3,MA Chun-mei3
(1.Departmentof Endocrine,Dalian Municipal Central Hospital,Dalian 116003,China;2.Department of Pathology,the First Affiliated Hospitalof Dalian Medical University,Dalian 116011,China;3.Department of Pathology,Institute of Laboratory Anima l Science,Chinese Academy of Medical Sciences(CAMS)and Peking Union Medical College(PUMC),Beijing 100021,China)
[Objective]To study the effects of berberine on the exp ression of hepatic sterol regulatory element-binding p rotein(SREBPs)and their control and target genes in type 2 diabetic Chinesehamsters and explore the therapeutic molecu larmechanisms of berberineon fat-induced hepatic insulin resistance.[Methods]The insulin-resistantand type 2 diabetic Chinese hamster models were induced by high-fat diet without or with low-dose strep tozotocin.Then,the hamsters were randomly divided into 4groups:normal control,insu lin-resistant,diabetic and berberine-treated diabetic groups.After nine-week treatment,the expression of hepatic SREBPs and their control and target genes from different groups were measured by RT-PCR.[Results]It was indicated that the expression of SREBPs,SCAP,S1P,S2P and SREBPs target genes was increased and the expression of Insigs was decreased in the fatty liver ofhamstermodel.Berberine effectively improved insulin resistance and reversed the altered expression ofhepatic SREBPs and its controland targetgenes in diabetic hamsters.[Conclusion]SREBPs gene transcriptional programs are involved in the therapeutic molecu lar mechanisms of berberine on fat-induced hepatic insu lin resistance in type 2 diabetic hamsters.
berberine;type 2 diabetes;sterol regulatory element-binding p rotein;insu lin resistance;Chinese hamster;liver
R 583.1
A
1671-7295(2011)01-0023-08
2010-11-16;
2010-12-18
劉栩晗(1975-),女,遼寧錦州人,主治醫師,醫學博士。E-mail:xuhanliu281277@yahoo.com.cn
李國生,主治醫師。E-mail:guoshengli998@163.com

