對HPLC法測定格列吡嗪片中含量及含量均勻度流動相的改進
閆韶華
河南省周口市食品藥品檢驗所(466000)
格列吡嗪片為第二代磺酰脲類抗糖尿病藥,適用于經飲食控制及體育鍛煉2~3個月療效不滿意的輕、中度2型糖尿病患者,這類糖尿病患者的胰島β細胞需有一定的分泌胰島素的功能,且無急性并發癥,無嚴重的慢性并發癥。國家藥品標準[1]采用HPLC法測定含量及含量均勻度,本文采用HPLC法,通過對流動相的改進,使格列吡嗪片的檢驗方法更加合理,準確。實驗結果表明,本法簡便、快速、準確,精密度高,可用于含量及含量均勻度的測定。
1 儀器與試藥
LC-1200型高效液相色譜儀(安捷倫公司生產),VWD型紫外檢測器,Agilent化學工作站,普利賽斯電子分析天平。格列吡嗪對照品(批號:100281-200602,中國藥品生物制品檢定所),格列吡嗪片(瑞陽制藥有限公司、輝瑞藥業有限公司),甲醇、乙腈均為MERCK牌色譜純,水為重蒸餾水。
2 方法與結果
2.1 色譜條件
色譜柱:AgilentlC18(250mm×4.6mm,5μm);流動相:甲醇-0.1mol/L磷酸二氫鈉溶液(用2.0mol/L氫氧化鈉溶液調節pH至6.00±0.05)-乙腈(45∶55∶10);檢測波長:225nm;流速:0.8mL/min;柱溫:室溫。理論塔板數不低于2000;分離度>1.5。
2.2 溶液的制備
2.2.1 對照品溶液
精密稱取格列吡嗪對照品,加甲醇溶解后并稀釋制成每mL中含格列吡嗪0.5mg的溶液,搖勻,作為儲備液。精密量取儲備液1.5、2.0、2.5、3.0、4.0mL分別置于25mL容量瓶中,加甲醇10mL,再用0.1mol/L磷酸二氫鈉溶液稀釋至刻度,搖勻。
2.2.2 線性關系考察
精密稱取格列吡嗪對照品0.0264g,按2.2.1項下方法制備對照品溶液,按上述色譜條件,取10μL進樣,記錄色譜圖(圖1),以峰面積Y對對照品進樣量(μg/mL)作線性回歸。結果回歸方程(n=5)為:Y=45.497X+677.92,r=0.9996;線性范圍為:31.68μg/mL-84.48μg/mL。
2.3 重復性實驗
取同一批號樣品適量(約相當于格列吡嗪5mg)3份,精密稱定,按樣品測定項下的方法,測定格列吡嗪片的含量,RSD為0.62%。
2.4 穩定性實驗
配制一份供試品溶液,室溫下在0、2、4、6、8h測定,結果表明,本品的供試品溶液在室溫8h內基本穩定,RSD=0.70%,n=5。
2.5 精密度試驗
取線性關系考察中格列吡嗪濃度為52.80μg/mL的對照品溶液,重復進樣5次,結果RSD為1.02%。
2.6 加樣回收實驗
精密稱取已知含量的樣品適量(約相當于格列吡嗪5mg)5份,分別置于100mL容量瓶中,加甲醇50mL,超聲處理15min使格列吡嗪溶解,用0.1mol/L磷酸二氫鈉溶液稀釋至刻度,搖勻,濾過,精密量取續濾液10mL于25mL容量瓶中,分別精密加入格列吡嗪對照品儲備液1.00mL,加0.1mol/L磷酸二氫鈉溶液稀釋至刻度,照樣品測定項下的方法測定,結果見表1。2.7 樣品含量的測定
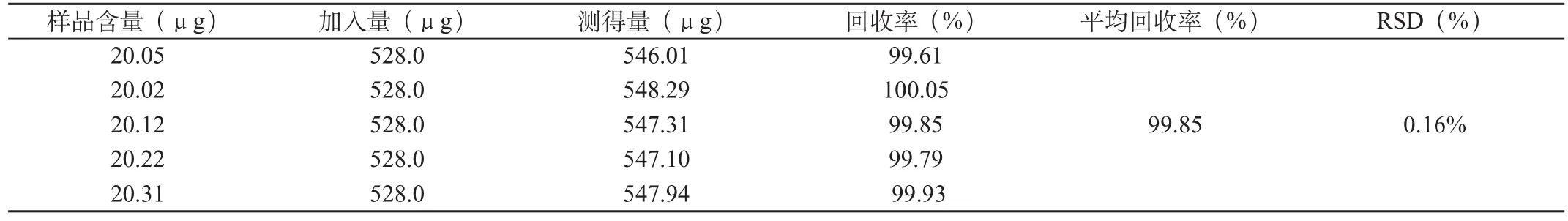
表1 回收率測定結果表(n=5)
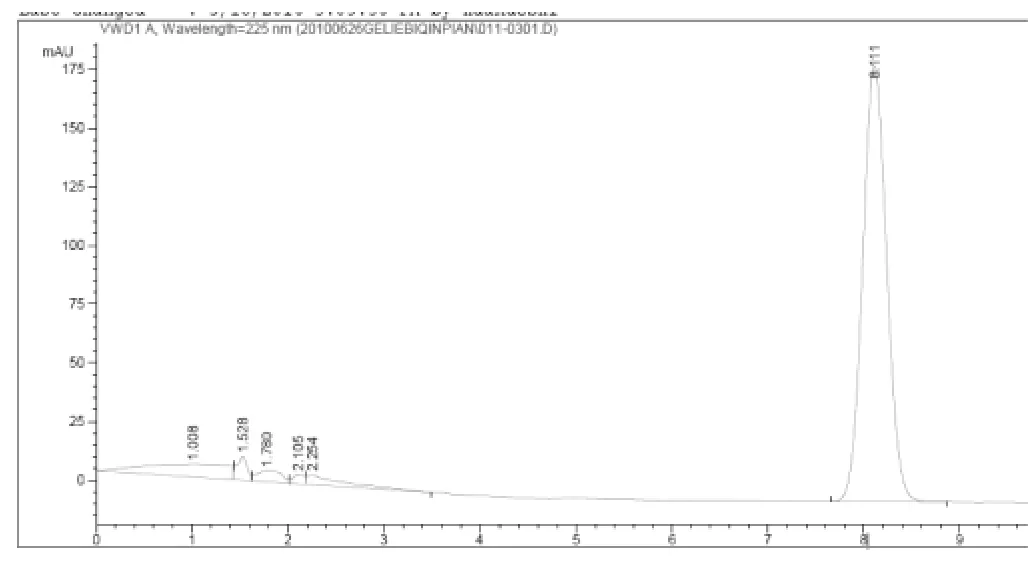
圖1 -1 對照品
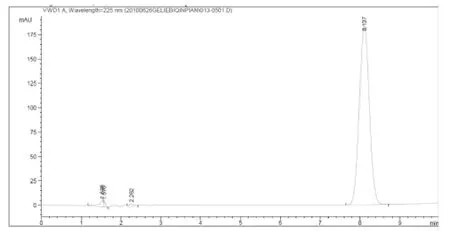
圖1 -2 樣品
取本品20片,精密稱定,研細,精密稱取適量(約相當格列吡嗪5mg),置于100mL容量瓶中,加甲醇50mL,超聲處理15min使格列吡嗪溶解,加0.1mol/L磷酸二氫鈉溶液稀釋至刻度,搖勻,濾過,精密量取續濾液20μL進樣測定,記錄色譜圖,按外標法以峰面積計算,測得結果與國家藥品標準[1]方法比較,結果見表2。

表2 格列吡嗪片含量及含量均勻度測定結果表(n=2)
2.8 樣品含量均勻度的測定
取本品1片,置于50mL容量瓶中,加甲醇25mL,超聲處理15min,加0.1mol/L磷酸二氫鈉溶液稀釋至刻度,搖勻,濾過,按本文色譜條件,精密量取續濾液20μL進樣測定,記錄色譜圖,按外標法以峰面積計算,結果見表2。
3 討 論
3.1 流動相的選擇
采用國家藥品標準[1]方法的流動相,高效液相儀的柱壓不穩定,基線不平穩,保留時間長,出峰時間慢,通過加入乙腈提高了極性,使出峰時間縮短了一倍,且柱壓保持穩定,峰面積或峰高重現性好,偏差較小。
3.2 由于流動相含有鹽成分,可以先把流動相混合,放置30min后,再用0.22μm的濾膜過濾,這樣可以使基線更平穩。
3.3 本法與《中國藥典》2005年版增補本相比較,二者結果無顯著性差別,為藥品標準的提高,保證藥品質量提供了一定的參考。
[1] 國家藥典委員會.中華人民共和國藥典2005年版增補本[S].北京:化學工業出版社,2005:301.

