高低不同轉移特性骨肉瘤亞克隆細胞系的分離與鑒定及其Cofilin信號轉導通路的相關性研究
婁 楠,王 巖,趙建武,王 洋,高忠禮*
(1.吉林大學中日聯誼醫院,吉林長春130033;2.吉林大學病理生物學教育部重點實驗室)
近年來已有學者[1]通過對骨肉瘤的研究,使用單細胞克隆篩選的方法,得到高侵襲的細胞亞群。而我們采用不同方法,先分離得到holoclone后通過多個成骨細胞分化標志物檢測,得到高侵襲及高致瘤的骨肉瘤細胞株。并對這些骨肉瘤細胞株進行了一系列的鑒定試驗。對其中的高侵襲單克隆細胞株在Cofilin信號轉導通路的相關基因表達進行了檢測。
1 材料和方法
1.1 材料
人成骨肉瘤細胞MG-63購自ATCC。高糖DMEM(H-DMEM)Gibico USA 、優等胎牛血清(FBS)Hyclone USA,胰酶Promega USA,DMSO天佳生物科技有限公司 China,DEPC鼎國生物科技有限公司China,Trizol Invitrogen USA、RT-PCR Kit TaKaRa Japan,Triton X-100、PISigma USA,RNA 提取試劑(Trizol-Reagent)Invitrogen USA,RNase free DNase I Promega USA,RT試劑盒TaKaRa Japan,PCR引物由TaKaRa合成。
1.2 克隆篩選
采用有限稀釋法,將對數生長期的骨肉瘤MG-63細胞在96孔板中稀釋成每孔含0.5-1個細胞,在克隆化后3-5 d選出僅含有單個細胞生長的并生長成完全克隆的孔進行標記,待細胞增殖至孔面積1/3時(即細胞數超過600個),將細胞移至24或48孔板中擴大培養,后再轉至6孔板,最后轉入培養瓶,后行細胞功能實驗鑒定。
1.3 生物學特性鑒定
1.3.1 形態學 相差顯微鏡拍攝有限稀釋法分離得到的各單克隆細胞亞系的細胞形態。
1.3.2 腫瘤細胞遷移能力的檢測(劃痕實驗)用0.25%胰蛋白酶消化體外培養的腫瘤細胞,調整細胞濃度為1×105/ml,分別將100 μ l細胞懸液接種于預包被的96孔培養板中。每組平行8個樣本。人工劃痕:在單層培養細胞上,用移液器滴頭沿培養板底部呈“一”字形劃痕,用激光共聚焦顯微鏡攝像,并測量劃痕區距離(A值),培養24小時,觀察并照相。測量遷移距離:用激光共聚焦顯微鏡攝像,并測量相同劃痕區的遷移后的距離(B值),根據下面公式計算出細胞實際遷移距離。相對移動距離=(A-B)/A×100,結果用±s表示。
1.3.3 Boyden小室遷移侵襲實驗 實驗共設3組,包括A3組、D1組和MG63組。包被先將Matrigel置4℃融化,并用無血清培養基將其1∶3稀釋,混勻,60 μ l/孔加至Boyden小室的上室聚碳酸酯膜上,整個操作在冰上及無菌條件下進行,所有器皿及試管均事先預冷。37℃下孵育30 min,此時Matrigel已形成膠。熒光標記細胞,將各組細胞用0.25%胰酶消化,離心,PBS洗一次,離心棄洗液,加入1 mg/ml羅丹明,靜止2-3 min,離心1 000 rpm,5分鐘。PBS洗一次。
上室加入各組細胞5×105個/孔,于37℃5%CO2條件下培養。在細胞接種2小時末,分別在激光共聚焦顯微鏡下,觀察細胞距離孔徑的距離,用以判斷細胞在Matrigel內的遷移速度及侵襲距離。培養4-6小時,棄去上室中的培養液,并用生理鹽水棉簽輕輕檫去Matrigel膠,用激光共聚焦顯微鏡200×視野下任取5個不重復視野照相,并記數細胞數量±s表示。
1.3.4 腫瘤細胞在ECM上粘附的測定 包被基底膜:用滅菌雙蒸水分別配制以下三種溶液:10 g/L BSA;50 mg/L Matrigel 1∶8稀釋液 ;10 mg/L FN,以 50 μ l/每孔分別加入96孔培養板,4℃過夜。水化基底膜:吸出培養板中殘余液體,每孔加入50 μ l含10 g/L BSA的無血清培養液,37℃,30分鐘。接種細胞:用0.25%胰蛋白酶消化體外培養的腫瘤細胞,調整細胞濃度為1×105/ml,分別將100 μ l細胞懸液接種于包被后的96孔培養板中。每組平行16個樣本。培養細胞,根據CCK-8比色法測定經過清洗的各孔細胞的光吸收值并計算平均值,結果用±s表示。
1.3.5 RT-PCR 應用Trizol Reagent提取細胞總RNA,用 RNase free DNase I對所獲樣品進行處理,除去可能污染的DNA分子。應用RT試劑盒將提取的總RNA逆轉錄為cDNA。
1.3.6 統計學分析 數據分析采用SPSS11.5統計軟件包進行t檢驗,P<0.05為有顯著性差異。
2 結果
2.1 細胞單克隆大體形態
96孔板中成功分離單細胞生長的約為60個,其中有23個克隆成功傳至培養瓶中繼續生長,余者皆發生凋亡或無法繼續傳代,在同等培養情況下,傳至8-12代又有3個單克隆細胞亞系出現自發性的死亡,而無法繼續傳代。而分離出各單克隆細胞亞系的細胞大體形態差異顯著(10倍鏡下)。
2.2 細胞形態學
多數克隆與克隆前相似,以短梭形和多邊形為主,細胞排列緊密,胞體大,突起細長,無接觸抑制,易于堆疊,結團,A3形體稍小。另一類呈長梭形(A1,D1)胞體小,胞漿豐富,突起寬而短,有一定接觸抑制,容易形成單細胞層。
2.3 劃痕實驗
我們選取大體形態具有代表性的8個單克隆細胞株進行細胞生長曲線的測定,其中A3的倍增時間明顯短于其他單克隆細胞株,存在明顯差異。選取細胞都在4-16代之間,每次實驗各克隆選取的細胞均為同一代次。而其中D1克隆則隨著代次的增加,細胞增殖速度逐漸加快。
2.4 Boyden小室侵襲實驗
在接種細胞后3 h至6 h,動態觀察細胞侵襲距離,A3組細胞穿行距離明顯大于其他3組。6 h時觀察穿過Matrigel膠侵襲的細胞數,可見A3組侵襲細胞數明顯多于其他3組,其間差異顯著。A3、D1、MG63、A1細胞穿過人工基底膜膠侵襲細胞數分別為185.0±16.5、154.0±11.2、129.2±14.35和73.0±11.2。A3組穿膜侵襲細胞數與MG63比較,差異有統計學意義(P<0.05)。見圖1。
2.5 細胞株黏附能力的測定
統計結果顯示,A3、A1、D1、MG63四系黏附細胞數量無明顯差異(P>0.05)(表1)。細胞鋪展過程觀察顯示:在BSA包被的孔板中,各組細胞均不黏附鋪展,細胞為圓形;在Matrigel及FN包被的孔板中,雖然A3組同其他組的黏附細胞數量比較無統計學差異,但其細胞多數鋪展良好,細胞由圓形變為不規則圓形,鏡下細胞體積大,部分細胞伸出多個突起。
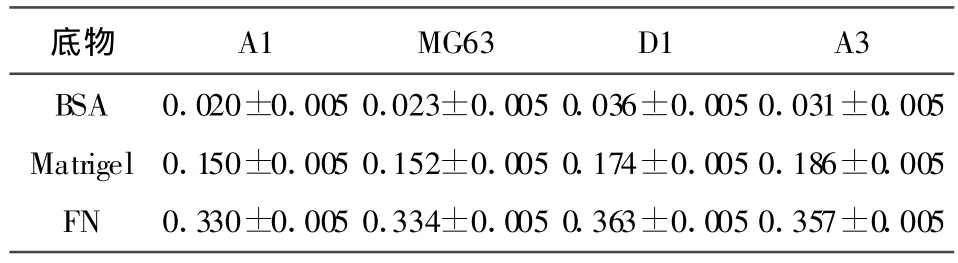
表1 細胞株黏附能力
2.6 RT-PCR表達
A3細胞株LIMK1高表達。D1的SSH1 L表達略高于其它單克隆。見圖2。
3 討論
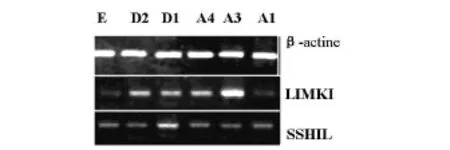
圖1 MG63母系細胞及各單克隆亞系細胞侵襲能力
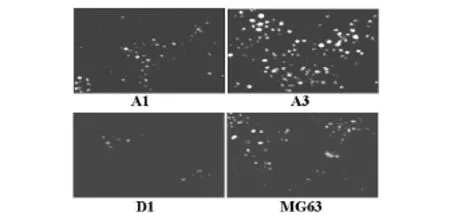
圖2 RT-PCR檢測MG63各單克隆亞系細胞LIMK-1和SSH1L的基因表達
最新研究報道:Cofilin在蛋白質水平的過量表達提高了腫瘤細胞遷移的速率[2],Cofilin表達的抑制能顯著減少腫瘤細胞的入侵。而Cofilin在mRNA水平的過量表達已經在腫瘤細胞(如乳房腫瘤)亞群中檢測到[3]。在本次研究中,通過有限稀釋法得到的骨肉瘤單克隆細胞株雖然在大體形態存在極為顯著的差異,但在蛋白質水平上Cofilin總量表達并無明顯差異,而具有高侵襲和遷移能力的A3細胞株P-Cofilin表達較其他單克隆顯著增高,即Cofilin的磷酸化程度增高。這也能夠說明Cofilin相關的信號通路介導了骨肉瘤細胞的侵襲及轉移,
近年來LIMK-1在腫瘤發生中的意義引起了廣泛關注[4,5]。有研究發現,LIMK-1在人乳腺癌生長、血管發生和侵襲中起重要作用[6]。另有報道,LIMK-1在前列腺腫瘤和前列腺癌細胞株中有過度表達,并且轉移的前列腺癌細胞中也有高濃度磷酸化的Cofilin;抑制LIMK-1后能使細胞靜止在G/M期從而改變細胞增殖、細胞形態,遏制轉移性前列腺癌細胞的侵襲性[7]。在李振華[8]等人的研究表明通過RNAi技術,抑制LIMK-1在骨肉瘤細胞中的表達則直接導致骨肉瘤細胞遷移及侵襲能力的下降,而在我們本次研究中高侵襲力單克隆細胞株A3 LIMK-1表達量明顯高于其他單克隆細胞株,我們推斷A3細胞株正是MG63骨肉瘤異質成分中高侵襲力的部分,而LIMK-1在骨肉瘤侵襲的過程中扮演了相當重要的角色。通過對其侵襲能力的抑制就能夠達到對骨肉瘤早期轉移和侵襲的有效預防和治療,而通過抑制LIMK1活性來抑制骨肉瘤細胞的轉移和侵襲,無疑具有廣闊的研究前景。在我們的研究中D1細胞株SSH1L表達較其他克隆略高,可推斷其Cofilin的磷酸化程度必然降低,即P-Cofilin表達水平降低。通過侵襲試驗我們發現其侵襲能力低于母系,說明Cofilin通路關鍵基因的改變確與骨肉瘤細胞株侵襲力的高低有著非常密切的關系。而軟瓊脂集落試驗中此細胞株具有非常強的成瘤能力,明顯高于母系及其他細胞株。梅紅[9]等研究表明包括雌激素在內的很多刺激因子可以通過PI3K/AKT/SSH1L信號傳導通路下調SSH1L,促進hMSCs的增殖和成骨分化,而D1細胞株SSH1L的表達異常是否也與成骨肉瘤細胞的多項分化潛能有關,我們也將就此進行更為深入細致的研究。
[1]石曉兵,陳安民.不同轉移特性人成骨肉瘤MG2 63細胞亞系的建立及特征[J].中國矯形外科雜志,2004,12(21):1675.
[2]Yamaguchi H,Condeelis J.Regulation of the actin cytoskeleton in cancer cell migration and invasion[J].Biochim Biophys Acta,2007,1773(5):642.
[3]Yap CT,Simpson TI,et al.The motility of glioblastoma tumour cells is modulated by intracellular cofilin expression in a concentration-dependent manner[J].Cell Motil Cytoskeleton,2005,60(3):153.
[4]Horita Y,Ohashi K,et al.Suppression of the invasive capacity of rat ascites hepatoma cells by knockdown of Slingshot or LIM kinase[J].J Biol Chem,20 08,283(10):6013.
[5]Heredia L,Helguera P,et al.Phosphorylation of actin-depolymerizing factor/cofilin by LIM-kinase mediates amyloid beta-induced degeneration:a potential mechanism of neuronal dystrophy in Alzheimer's disease[J].J Neurosci,2006,26(24):6533.
[6]Nishimura Y,Yoshioka K,et al.LIM kinase 1:evidence for a role in the regula-tion of intracellular vesicle trafficking of lysosomes and endosomes in human breast cancer cells[J].Eur J Cell Biol,2004,83(7):369.
[7]Bagheri-Yarmand R,Mazumdar A,et al.LIM kinase1 increases tumor metastasis of human breast cancer cells via regulation of the urokinasetype plasminogen activator system[J].Int J Cancer,2006,118(11):2703.
[8]李振華.LIMK1表達對人成骨肉瘤細胞生物學活性影響的體外研究[J].2008,04:01.
[9]梅紅.雌激素在hMSCs成骨和成脂肪誘導分化中的作用及機制研究[J].吉林大學,2008(04):01.

