優化實驗設計 啟迪學生思維
王秀秀
文章編號:1005-6629(2009)07-0030-03中圖分類號:G633.8文獻標識碼:B
在實驗教學過程中,教師要善于從多種角度優化實驗設計,使學生學會“手腦并用”,讓學生的思維火花在“設疑→實驗→質疑→頓悟”的教學進程中一次次閃耀,體驗學習的快樂和科學知識的魅力,并有利于知識的同化和靈活運用,逐步形成科學思維的習慣。
1 改變反應物的用量,促進求異思維
初中科學教材中很多實驗具有“量變引起質變”的辯證內涵,教師若有意識地改變實驗中藥品的用量,與教材中規定用量的實驗現象進行對比,會達到“出其不意”的效果。
如華師大《科學》九上第二章有一個實驗活動:“用新制的Cu(OH)2檢驗葡萄糖”。在學完九下化學內容后,安排一個學生分組探究活動,重做這個實驗。
原課本要求:用2 mL 10 % NaOH滴加 4~5滴 5 %CuSO4溶液制成 Cu(OH)2再加入2 mL 10%葡萄糖加熱煮沸,通過觀察Cu(OH)2顏色變化,檢驗葡萄糖的存在。
分組實驗:每組第一次按課本藥品用量及步驟進行實驗,加熱煮沸觀察Cu(OH)2顏色變化。
設疑:增大NaOH溶液濃度,滴入CuSO4溶液量增多,現象仍一樣嗎?
實驗:第2次用4 mL 10% NaOH滴加8~10滴5% CuSO4溶液制成 Cu(OH)2, 再加入 2 mL 10%葡萄糖(Cu(OH)2過量), 加熱煮沸,觀察Cu(OH)2顏色變化,并與第一次的實驗現象進行比較。
質疑:不同的實驗現象引發學生的思考,紛紛提出問題:“第一次實驗 Cu(OH)2加熱煮沸后變成紅色。第2次實驗Cu(OH)2加熱煮沸后為什么一部分變成黑色,一部分變成紅色?”
教師趁勢引導:“同學們,根據第一次實驗現象你能得出什么結論?你們猜想第二次實驗中生成的黑色物質是什么?紅色物質是什么?說出你們猜想的理由。”
學生提出多種猜想:有的認為黑色物質是碳,紅色物質是Cu。猜想理由是Cu(OH)2使C6H12O6脫水碳化生成了碳;有的認為黑色物質是CuO, 紅色物質是Cu。猜想理由Cu(OH)2是不溶性堿加熱能分解成CuO和H2O;還有的認為黑色物質是CuO,紅色物質是Cu和Cu2O。他的理由 Cu(OH)2不可能使C6H12O6脫水碳化,否則第一次實驗中Cu(OH)2也能使C6H12O6脫水碳化生成黑色物質;對紅色物質猜想是Cu和Cu2O,理由是從H2還原CuO實驗了解到紅色生成物可能是Cu和Cu2O的混合物。以上學生的猜想及理由似乎都有道理,教師不急于評價對錯或拋給學生答案,而是讓學生通過設計實驗來驗證黑色物質是C還是CuO,紅色物質是Cu還是Cu2O。學生又提出了多種實驗方案:1.取黑色物質加入少量的稀硫酸微熱看溶液是否變成藍色,若變藍色說明黑色物質是CuO而不是C。2.用石棉網灼熱黑色物質,用內壁附有澄清石灰水的小燒杯罩住,觀察內壁是否變渾濁,若渾濁說明黑色物質是C。3.將黑色物質灼熱后,立即放入盛滿氫氣的集氣瓶,看是否變成紅色,若變紅色說明黑色物質是CuO。4.在紅色物質中滴加稀硫酸微熱,若不能反應則紅色物質是Cu,若能反應則是Cu2O。”
又如:探究“空氣中氧氣的體積分數”實驗中,白磷足量或不足量充分燃燒后,鐘罩內水面上升刻度不同,從而啟發學生思考影響氧氣體積分數偏小的各種原因。還如探究“用H2O2溶液和MnO2催化劑制取氧氣”實驗時, 讓學生用溶質質量分數分別為2%、5%、8%的H2O2溶液和等質量的MnO2混合制取氧氣,可以觀察到各實驗中產生氧氣的速率明顯不同,從而激發學生探究“影響化學反應速率可能與哪些因素有關?”。再如探究“Na2CO3溶液與鹽酸反應”實驗時,若在 Na2CO3溶液中滴加少量稀鹽酸,與加入足量稀鹽酸時觀察到產生氣泡現象不同,從而激發學生探究“Na2CO3與少量稀鹽酸反應生成產物是什么?”這些事例中滲透了“量變到質變”的辨證思想,學生的學習也更積極主動,課堂充滿了活力。
2 改變實驗器材,培養發散思維
在實驗教學中,教師要有強烈的課程資源整合意識。同一實驗中,要善于改變實驗器材,采用多種方法的實驗設計,開闊學生的視野,啟迪學生的發散性思維。
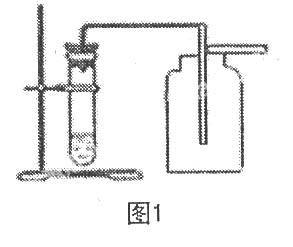
如在已學過實驗室制取O2的基礎上,學習“實驗室制取CO2氣體”時,教師故意創設如下情景:“用如圖1所示帶單孔橡皮塞的小試管和集氣瓶制取CO2氣體,在取石灰石藥品時,挑出來的石灰石大多放不進小試管口,只好取小顆粒與稀鹽酸反應,實驗時發現反應速率太快,驗滿時發現集氣瓶中CO2未滿而反應已停止。”學生看在眼里急在心里,七嘴八舌議論紛紛。此時教師提出問題:“如你想制取3瓶CO2氣體,用于檢驗CO2性質,你認為此裝置有何不足?”學生紛紛動腦一起討論解決困難,有的說此反應裝置太小;有的說此裝置不能控制反應速率;有的說此裝置不能隨時控制反應停止和進行。教師又問“為了解決以上問題,應如何改進裝置,請設計裝置草圖。”學生設計了多種反應裝置,如圖2所示:
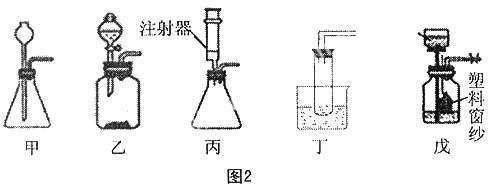
接著讓學生當裁判評價哪種設計方案最佳, 說出理由,并評選最佳設計獎和最佳評論員。在這過程中學生參與的熱情高漲,順利解決了發生裝置的問題。教師再提出關于收集裝置的問題:“我們生活中有哪些器材可以收集CO2氣體?”學生方法很多,除了課本中常見的收集裝置外,有的說用扁癟的氣球或塑料袋收集較方便不用排空氣,而且使用時只要插入管子通過擠壓就可把氣體導出;有的說用洗氣瓶收集氣體比常見的排空氣法方便,可以直接在導管口驗純不用浪費整瓶氣體,可節約藥品;有的說用針筒跟帶橡皮管的導管相連收集更方便。
又如探究噴泉形成原因時,若讓學生設計實驗難度太高,教師可以展示多種形成噴泉的實驗裝置,讓學生逐個分析這些裝置形成噴泉的原理,并讓學生歸納要形成噴泉可采用方法。經過分析歸納學生得出形成噴泉可采用方法有:1.利用氣體和溶液反應改變裝置壓強差。2.利用溶解性極大的氣體溶于水形成壓強差。3.利用物理方法通過改變裝置內溫度改變裝置壓強差。
實驗教學中,改變器材的設計方法有:1.同一實驗讓學生設計不同的裝置進行實驗。2.通過教師展示不同實驗裝置讓學生分析各裝置的實驗原理,進行總結歸納,等等。但教師在引導學生解決問題的過程中應始終堅持不急于指思路、拋答案,而是要給出相關信息激發學習熱情、挑戰他們的思維。課堂教學目的不只是使學生獲得知識,更重要的是培養學生科學思維的能力和科學研究方法。
3 改變實驗操作步驟,培養學生逆向思維
在實驗過程中,教師可有意“顛倒或改變實驗操作順序,或省略必須的操作步驟。”使實驗結果出錯,讓學生在找錯改錯中,培養學生嚴謹求實的科學態度,提高學生逆向思維能力。
如在學習濃硫酸稀釋時,如果教師讓學生由濃硫酸的性質,推測出稀釋時應將濃硫酸倒入水中,再讓學生實驗。這樣的實驗,學生照方抓藥顯得被動、缺乏思維。我試著改變實驗操作步驟,為保證實驗安全,選用一只大燒杯下面墊一塊50 cm×50 cm的正方形玻璃板,以免酸液飛濺到桌面。先向大燒杯中滴入幾滴紫色石蕊試液,倒入一定量的濃硫酸,學生觀察到石蕊試液變紅——馬上說出這是酸與指示劑的作用,不一會兒,紅色褪去——學生想到濃硫酸使石蕊脫水,接著向該燒杯中加入水,看到酸液劇烈飛濺,大燒杯內、外濺滿了液滴。學生既驚慌又興奮,積極性受到極大的調動,幾乎都異口同聲地說:“不能將水倒入濃硫酸中。”學生思維積極,不但問題分析得好,并且印象深刻。
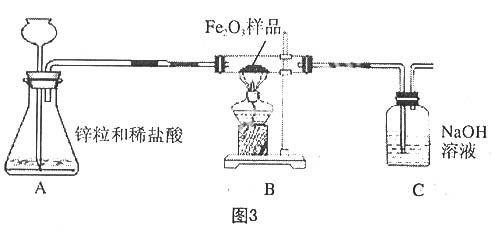
又如:在探究“Fe2O3樣品中Fe2O3的質量分數”實驗時,教師出示如圖3裝置,并提出問題:“通過哪些方法可以求得Fe2O3樣品中Fe2O3的質量分數?”
學生考慮出如下三種方案:1.待完全反應后,通過C裝置反應前后增加的二氧化碳質量,求得Fe2O3質量;2.通過B裝置反應前后減少的氧元素質量,得到Fe2O3質量;3.把反應后的鋅粒洗滌烘干,根據反應前后鋅粒質量改變量求得氫氣,再求得Fe2O3質量。
接著教師讓學生當裁判評價上述三種方案求得樣品中Fe2O3的質量是否準確,若不準確,請分析原因及應如何改進實驗?教師在解決問題的過程中應始終堅持不急于指思路、拋答案,而是要給出相關信息激發學習熱情、挑戰學生的思維。課堂教學目的不只是使學生獲得知識,更重要的是培養學生科學思維的能力和科學研究方法。
4 制造實驗“假象”,培養邏輯思維能力
古人云:“疑者,覺悟之機。”無智者往往被實驗“假象”所蒙蔽, 智者往往能識破“假象”, 去偽存真。在實驗教學中, 教師也不妨制造實驗“假象”,營造積極思維的氛圍,培養邏輯思維能力,讓學生爭做火眼金睛的智者,體驗科學探究的樂趣。
如在探究“鋁和鋅與酸反應的速率大小”時,用久置在空氣中的鋁片和存放在試劑瓶中鋅粒分別和同質量分數、相等質量的稀鹽酸反應,讓學生觀察不同時間段金屬表面產生氣泡的速率變化。學生觀察的結果是實驗剛開始時鋅粒表面產生氣泡速率遠遠大于鋁片,一段時間后發現鋁片表面產生氣泡速率且遠遠大于鋅粒表面。在這實驗過程中,學生觀察到了兩種截然不同的現象感到非常好奇,從而激發他們探究產生實驗“假像”的可能原因。又如在復習唾液淀粉酶對淀粉的消化作用時,教師故意設計了這樣一個實驗:向淀粉糊中滴加幾滴唾液,再滴入碘液結果發現試管內物質變藍色。教師讓學生分析老師實驗失敗的原因,并讓他們比比誰“火眼金睛”最厲害。學生分析出了多種形成假象的原因:1.淀粉糊太濃或太多。2.滴入唾液太細或太少。3.試管內物質溫度太低或太高。4.原試管沒清洗干凈殘留酸性或堿性物質影響酸的活性。5.操作時沒有振蕩等等。
在探究原理、規律性實驗時,教師可有意讓實驗“假象”和“真相”同時出現,這樣不僅可以使學生從實驗真相中得出實驗結論,還可以通過實驗“假象”激發學生質疑,促進思維,提高他們利用所學知識解決問題的能力。在拓展性實驗中教師可直接展示實驗“假象”使其與學生原認知結構中的實驗現象產生矛盾,從而激發學生的探究熱情。

